
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы получения. в лабораторных условиях эфиры получают по Вильямсону взаимодействием галогенопроизводных, способных вступать в реакцию Sn2 и алкоксид- и феноксид-ионами
|
|
|
|
· по Вильямсону
в лабораторных условиях эфиры получают по Вильямсону взаимодействием галогенопроизводных, способных вступать в реакцию Sn2 и алкоксид- и феноксид-ионами. Реакция протекает гладко с галогенметаном и первичными галогеналканами. В случае вторичных галогеналканов реакция может быть осложнена побочной реакцией элиминирования.
10) Алкадиены (диены) – непредельные алифатические углеводороды, молекулы которых содержат две двойные связи.
Общая формула алкадиенов СnH2n-2.
Классификация и номенклатура
Алкадиены
- ненасыщенные углеводороды, содержащие две двойные связи и образующие гомологический ряд с общей формулой CnH2n-2, откуда можно сделать вывод, что они изомерны алкинам.
Названия диенов строятся все по тому же принципу, заменяя суффикс –ан в соответсвующем алкане на –ен, поскольку, согласно определению, они содержат две двойные связи, то нужно добавить еще ДИ- (что означает два, две двойные связи), тогда получается –ДиЕн.
Примеры: CH2=CH-CH2-СН=CH2 пентаДиЕН-1,4 (или 1,4-пентадиен, или пента-1,4-диен), цифрами указывается положение двойных связей.
СН2=СН-СН=СН-СН3 пентадиен-1,3
СН2=С=С-СН2-СН3 пентадиен-1,2
Как видно двойные связи могут располагаться у разных атомов углерода, именно по принципу расположения двойных связей диены делятся на три группы:
· изолированные – двойные связи разделены двумя или более одинарными связями, т.е. между ними есть n(СН2)- группы: 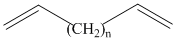 ;
Простейшим соединением с изолированными двойными связями является пентадиен. Такие соединения обладают теми же свойствами, что и алкены, содержащие одну двойную связь.
· сопряженные – двойные связи разделены одной одинарной: ;
Простейшим соединением с изолированными двойными связями является пентадиен. Такие соединения обладают теми же свойствами, что и алкены, содержащие одну двойную связь.
· сопряженные – двойные связи разделены одной одинарной: 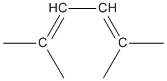 . Простейшее соединение – бутадиен-1,3 (дивинил);
· кумулированные (аллены, 1,2-диены)– двойные связи находятся при одном и том же атоме углерода: . Простейшее соединение – бутадиен-1,3 (дивинил);
· кумулированные (аллены, 1,2-диены)– двойные связи находятся при одном и том же атоме углерода: 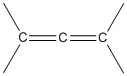 . Простейшиу кумуллен – пропадиен-1,2 (или аллен). Данные соединения наиболее интересны из всего класса диенов, т.к. центральный атом углерода С= С =С имеет sp- гибридизацию, в отличие от остальных, поэтому двойные связи ориентированы друг относительно друга в двух взаимно перпендикулярных плоскостях: . Простейшиу кумуллен – пропадиен-1,2 (или аллен). Данные соединения наиболее интересны из всего класса диенов, т.к. центральный атом углерода С= С =С имеет sp- гибридизацию, в отличие от остальных, поэтому двойные связи ориентированы друг относительно друга в двух взаимно перпендикулярных плоскостях: 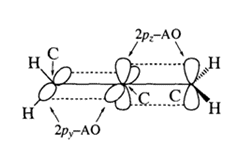 . Поэтому фрагмент . Поэтому фрагмент  является неплоским. В соответствие с этим 1,3-дизамещенные аллены не имеют элементов симметрии и могут существовать в виде энантиомеров. В качестве примера могут быть рассомотрены два энантиомера пента-2,3-диена: является неплоским. В соответствие с этим 1,3-дизамещенные аллены не имеют элементов симметрии и могут существовать в виде энантиомеров. В качестве примера могут быть рассомотрены два энантиомера пента-2,3-диена:
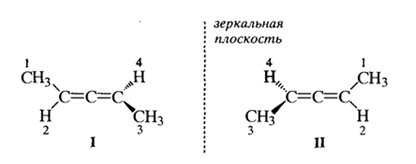 В данных энантиомерах отсутствует хиральный центр.
В данных энантиомерах отсутствует хиральный центр.
|
1. Изомерия алкадиенов
1.1 Структурная изомерия
1.1.1. Изомерия углеродного скелета
H2C CH CH CH CH3 H2C CH C CH2
CH3
пентадиен-1,3 2-метилбутадиен-1,3
(изопрен)
. Пространственная изомерия
АЛКАДИЕНЫ
Диены с сопряженными двойными связями проявляют большое своеобразие свойств, благодаря присущему им эффекту сопряжения. Отдельные р электроны не закреплены попарно в определенных связях, а делокализованы, то есть распределены по всем находящимся в сопряжении связям. Взаимное влияние в сопряженных связях проявляются и в изменении межядерных расстояний длина центральной связи становится несколько короче, а длина двойных связей несколько больше их обычной длины. То есть три связи соединяющие 4 атома углерода не являются ни истинно двойными ни истинно простыми. В следствии этого диеновые углеводороды с сопряженными связями способны присоединять различные вещества как по одной из двойных связей, так и к крайним атомам системы с перемещением двойной связи в центр системы.
Способы получения дивинил
Бутадиен-1,3, или дивинил, СН2=СН—СН=СН2 представляет собой газ, конденсирующийся при —4,5° С. Вследствие громадного технического значения бутадиена-1,3 как одного из важнейших исходных мономеров для производства синтетических каучуков было разработано много способов его получения, в том числе и промышленных.
Бутадиен образуется при термическом разложении различных органических веществ; в небольших количествах содержится в газах, получаемыхпиролизом нефтепродуктов и каменного угля. Он может быть получен пиролизом циклогексана и других углеводородов нефти, пиролизомциклогексанола, дегидратацией 1,3-бутиленгликоля, а также конденсацией альдегида и спирта в присутствии глинозема как катализатора (И. И. Остромысленский). В последнем случае, вероятно, промежуточно образуется 1,3-бутиленгликоль
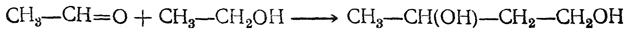
который сразу же дегидратируется. Другой способ получения бутадиена из спирта состоит в окислении этанола в ацегальдегид, который конденсируют вальдоль; восстановление альдоля дает 1,3-бутиленгликоль.
Первым технически целесообразным путем получения бутадиена из спирта является способ С. В. Лебедева, впервые осуществленный впромышленных масштабах вСССР в1932 г. и в дальнейшем получивший широкое распространение. По С. В. Лебедеву спирт непосредственно превращается в бутадиен при пропускании его паров при 400—500° С над катализатором, обладающим одновременно дегидрирующим и дегидратирующим действием. Суммарно процесс выражается уравнением
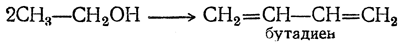
Вероятно, механизм этой реакции (М. Я.Каган, Ю. Д. Горин) таков:
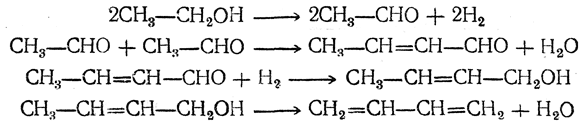
Можно получать дивинил, в том числе и впромышленном масштабе, наоснове ацетилена. Более старый метод синтеза из ацетилена может быть представлен следующей схемой:
1. Получение ацетальдегида из ацетилена по реакции Кучерова (в присутствии солей ртути):
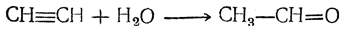
2. Щелочная конденсация альдегида вальдоль:
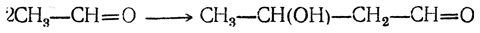
3. Восстановление альдоля в1,3-бутиленгликоль:
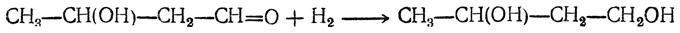
4. Дегидратация гликоля над фосфатным катализатором:
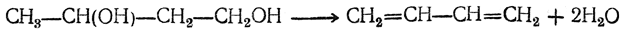
Позднее был предложен следующий путь: 1. Получение 1,4-бутиндиола конденсацией ацетилена и формальдегида (с Сu2Сl2 в качествекатализатора):
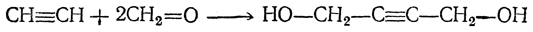
2. Гидрирование 1,4-бутиндиола в 1,4-бутандиол:
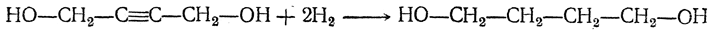
3. Дегидратация 1,4-бутандиола в дивинил либо непосредственно
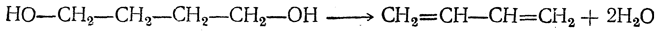
либо с промежуточным выделением тетрагидрофурана
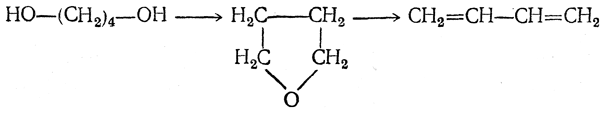
В настоящее время самым эффективным методом получения дивинила является каталитическое дегидрирование природного бутана, а такжебутиленов, содержащихся в газах термической переработки нефти. Реакция проводится над различными алюмо-хромовыми катализаторами при 500—650° С. В зависимости от применяемых катализаторов бутан может быть превращен в бутадиен либо сразу, либо в две стадии
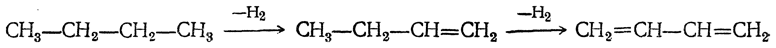
причем для каждой стадии требуются свои катализаторы и условия реакции. Эти методы, разрабатывавшиеся одновременно в СССР и в США, в настоящее время осуществляются как промышленные.
Хлорпроизводное дивинила — 2- хлорбутадиен -1,3, или хлоропрен, СН2—СН—ССl=СН2 может быть получен присоединением молекулы хлористого водорода к винилацетилену, получаемому при пропускании ацетилена через солянокислые растворы медных солей. Хлоропрен — жидкость с характерным эфирным запахом, несколько напоминающим запах бромистого этила; т. кип. 59,4°С, относительная плотность 0,9533 (при 20°С). Подобно дивинилу, но значительно легче, хлоропрен полимеризуется в каучукоподобные вещества — синтетические каучуки, выпускаемые в СССР под названием наирит, а в США — под названием неопрен.
Полихлоропреновые каучуки обладают рядом ценных физико-химических свойств — стойкостью к атмосферным воздействиям, к солнечному свету, к различным маслам и химическим агентам, а также негорючестью, благодаря чему они нашли очень широкое применение.
11) Понятие сопряжения было введено в химию в конце XIX века для объяснения некоторых особых свойств молекул, содержащих систему чередующихся двойных и простых связей. [ 2 ]
Очевидно, чтопонятие сопряжения не ограничивается кратными углерод-углеродными связями. [ 3 ]
| Принцип хемиосмотиче - роль сопрягающей системы. |
Не пользуясь непосредственно представлениями неравновесной термодинамики, Митчелл оперируетпонятием сопряжения, необходимым при рассмотрении открытых систем. Очевидно, что сопряженные процессы универсальны в живой природе. [ 4 ]
Этот результат представляет чрезвычайно большое значение для теоретической химии в смысле необходимости уточненияпонятия сопряжения. [ 5 ]
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 2252; Нарушение авторских прав?; Мы поможем в написании вашей работы!