
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Особенности кристаллизации и вторичные превращения в сталях
|
|
|
|
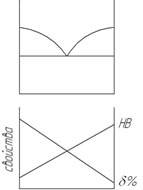
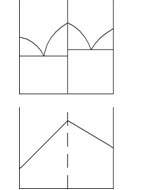
Связь между характером взаимодействия компонентов в двойных сплавах и их свойства (закон Курнакова).
Свойства сплавов зависят от взаимодействия компонентов, т.е. структуры. Диаграмма состояния характеризует взаимодействие компонентов и показывают, какая структура получается в зависимости от состава сплава.
Следовательно, существует связь между свойствами и типом диаграммы состояния.


16 Диаграмма состояния сплавов «железо-углерод». Характер взаимодействия железа с углеродом. Основные линии диаграммы.
Диаграмма состояния– это графическое изображение фазового состояния сплавов в зависимости от температуры и концентрации компонентов в условиях равновесия.
Компоненты системы – железо Fe и углерод С (рис. 7.1).

Рис. 7.1. Диаграмма состояния «Железо – карбид железа» (Fe – Fe3C)
Особенности диаграммы определяются полиморфизмом железа и углерода, а также ферромагнетизмом железа:
- от 1539 – 1392 оС железо имеет решетку ОЦК, такая модификация железа называется d (Fe);
- от 1392 – 911 оС железо имеет решетку ГЦК, такая модификация железа называется g(Fe);
- ниже 911 оС железо имеет решетку ОЦК, такая модификация называется a(Fe);
- при температуре 768 оС железо теряет магнитные свойства, и эта температура называется точкой Кюри.
В каждой модификации железа растворяется строго определенное количество углерода с образованием твердых растворов внедрения:
- d - феррит – раствор углерода в d(Fe) с ОЦК решеткой. Максимальная растворимость углерода в d(Fe) составляет 0,1 % при температуре 1499 оС;
- аустенит – твердый раствор углерода в g(Fe) с ГЦК решеткой. Максимальная растворимость углерода в g(Fe) составляет 2,14 % при температуре 1147 оС;
- a - феррит – твердый раствор углерода в a(Fe) с ОЦК решеткой. Максимальная растворимость углерода в a(Fe) составляет 0,025 % при температуре 727 оС.
Кроме указанных выше твердых растворов в системе Fe – С образуются две высокоуглеродистые фазы:
- цементит – химическое соединение Fe3С со сложной орторомбической решеткой, которое содержит 6,67 % углерода и имеет температуру плавления Тпл = 1260 оС. Эта фаза метастабильная, способная к распаду (Fe3С ® 3Fe + Сгр);
- графит – модификация углерода с ГПУ решеткой. Эта фаза стабильная, состоит на 100 % из углерода и имеет температуру плавления Тпл = 3600 оС.
В дополнение к фазам в виде твердых растворов на диаграмме имеются области существования механических смесей:
- перлит – механическая смесь (эвтектоид) феррита и цементита, содержащая 0,8 % С (рис. 7.1, точка S);
- ледебурит – механическая смесь (эвтектика) аустенита и цементита в интервале температур 1147 – 727 оС или перлита и цементита при температурах ниже 727 оС, содержащая 4,3 % углерода (рис. 7.1, точка С).
Сплошными линиями изображена диаграмма Fe – Fe3C, штриховыми – диаграмма Fe – С (рис.7.1). Основной является диаграмма Fe – Fe3С. Однофазные области диаграммы:
- выше линии ABCD (линия ликвидус) – жидкость (L);
- область AHN – область d - феррита;
- область NJESG – область аустенита;
- область GPQ – область a - феррита;
- линия LD или KD – область цементита Fe3C.
Остальные области диаграммы (рис. 7.1) – двухфазные: ледебурит, перлит и их комбинации.
7.1. Характеристика линий и точек диаграммы Fe – Fe3C
Линия АВСD - линия ликвидус – линия начала кристаллизации сплава и состоит она из трех частей:
- AB – начало образования d- феррита;
- BC – начало кристаллизации аустенита;
- CD – начало кристаллизации цементита Fe3C.
Линия AHJECF – линия солидус – линия конца кристаллизации сплава и состоит она из нескольких частей:
- AH – конец кристаллизации d- феррита;
- JE – конец кристаллизации аустенита;
- HJB - линия перитектического превращения:
Жв + FedH 1499 ® FegJ или ЖВ + ФH 1499® A аусJ
- ECF – линия эвтектического превращения:
Жс 1147® gЕ + Fe3CF или Жс 1147® АЕ + ЦI
Остальные линии соответствуют превращениям в твердом состоянии:
- NH и NJ (А4) – линии начала и конца полиморфного превращения Fed «Feg;
- GS (А3) и GP – линии начала и конца полиморфного превращения Feg «Fea;
- ES(Аст) – линия выделения вторичного цементита из аустенита (Fe3CII) за счет изменения растворимости углерода в g-железе. Эта линия называется линия сольвиус;
- PQ – линия выделения третичного цементита (Fe3CIII) за счет изменения растворимости углерода в a- железе;
- PSK (А1) – линия эвтектоидного превращения во всех сплавах независимо от содержания углерода:
FegS 727 ® FeaP + Fe3Ck или Ауст ® ФР + ЦII
- KD – линия существования химического соединения Fe3C (цементит);
- MO (А2) – 768 оС - линия магнитного превращения феррита (потеря магнитных свойств железа).
Физический смысл точек диаграммы:
- A – температура плавления и кристаллизации чистого железа;
- B – перитектическая точка;
- C – эвтектическая точка;
- D – температура плавления и кристаллизации цементита;
- N и G - температуры полиморфных превращений чистого железа;
- H – предельная растворимость углерода в d - железе;
- E – предельная растворимость углерода в g - железе;
- S – эвтектоидная точка;
- P и Q – точки предельной растворимости углерода в a - железе;
- M – точка магнитного превращения железа (точка Кюри).
А1, А2, А3, А4 – принятые условные обозначения фазовых превращений.
Важнейшей особенностью кристаллического состояния является упорядоченное расположение частиц вещества. Если вписать кристаллическую решетку в систему координат, то по расстоянию между ближайшими частицами в кристалле и углам между осями координат можно рассчитать взаимное расположение частиц в твердом теле. Для дальнейшего изучения кристаллического строения в кристаллической решетке можно выделить элемент объема из минимального количества частиц (атомов), многократным переносом (трансляцией) которого в пространстве можно построить весь кристалл.
В сталях основными являются три структуры: аустенит – твердый раствор углерода в γ – Fe [Fe γ(С)]; мартенсит – пересыщенный, частично упорядоченный твердый раствор углерода в α – Fe [Fe γ(С)]; перлит – эвтектоидная смесь феррита и цементита [Feα + Fe3 С]. Переход из одной структуры в другую характеризует основные превращения при термической обработке:
- первое превращение – это превращение перлита в аустенит, которое происходит при нагреве: П→А
- второе превращение – это превращение аустенита в феррито-цементитные смеси разной дисперсности в зависимости от скорости охлаждения: А→Ф+Ц;
- третье превращение заключается в превращении аустенита в мартенсит А→М при быстром охлаждении (при закалке);
- четвертое превращение заключается в разложении мартенсита при отпуске закаленной стали (М → продукты распада).
Любой технологический процесс термической обработки состоит из определенных комбинаций этих четырех превращений.
|
|
|
|
|
Дата добавления: 2015-04-23; Просмотров: 1148; Нарушение авторских прав?; Мы поможем в написании вашей работы!