
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общие химический свойства металлов
Ответ: Химические свойства металлов (смотри лабораторную работу №2 «Отношение металлов к воде, кислотам и щелочам”).
Металлы взаимодействуют с простыми и сложными веществами. Во всех реакциях металлы (простые вещества) выполняют роль восстановителей, при этом они окисляются до положительно заряженных ионов (катионов):
Металлы обладают разной химической активностью. Это проявляется как при окислении металлов газообразными или твердыми веществами (хлором, кислородом, серой), так и в реакциях с водой и водными растворами кислот, солей, щелочей. Поведение металлов в разбавленных водных растворах прогнозируется на основе ряда активности металлов. Этот ряд был составлен в результате многочисленных экспериментов русским ученым Николаем Николаевичем Бекетовым в 1865 году и назван им «вытеснительным рядом». Позднее ряд Н.Н. Бекетова получил теоретическое подтверждение на основе сравнения ЭДС гальванического элемента, составленного из пар разных металлов. Каждый металл (а точнее система металл0/металлn+, то есть металл, погруженный в раствор электролита, обычно соли, содержащий его катионы) характеризуется определенной величиной стандартного электродного потенциала. Ряд металлов, расположенных в порядке возрастания величин стандартных электродных потенциалов, называется электрохимическим рядом напряжений металлов.
Ряд активности (или электрохимический ряд напряжений) металлов отражает химическую (восстановительную) активность металлов в разбавленных водных растворах при комнатной температуре (25 OС). Чем более отрицателен электродный потенциал металла, то есть чем левее он расположен в ряду активности, тем больше его восстановительная способность. Более конкретные выводы таковы: 1)все металлы, стоящие левее водорода в ряду активности, т.е. имеющие отрицательный стандартный потенциал (стандартный потенциал водорода принят за 0), вытесняют водород из растворов кислот (за исключением азотной HNO3), т.е. восстанавливают катионы водорода; 2)металл, расположенный левее в ряду активности, вытесняет из растворов солей (восстанавливает) любой металл, стоящий в ряду активности правее; 3)восстанавливать водород из чистой воды (нейтральная среда) могут при комнатной температуре только наиболее активные (щелочные и щелочно-земельные) металлы, стоящие в самом начале ряда. Положение металлов в электрохимическом ряду напряжений позволяет объяснять коррозионное поведение металлов в различных агрессивных средах, а также прогнозировать электродные процессы при электролизе растворов электролитов.
Сильные восстановители: Me0-ne->Men+. 1)Реакции с неметаллами: С кислородом: 2Mg+O2->2MgO; С серой: Hg+S->HgS; С галогенами: Ni+Cl2->Ni+2Cl2; С азотом:3Ca+N2->Ca3N2; С фосфором: 3Ca+2P->Ca3P2. С водородом (реагируют только щёлочные и щёлочно-земельные металлы): 2Li+H2->2LiH; Ca+H2->CaH2. 2)Реакции с кислотами. Металлы, стоящие в электрохимическом ряду напряжений до H восстанавливают кислоты-неокислители до водорода:  3)Взаимодействие с водой. Активные (щёлочные и щёлочно-земельные металлы) образуют растворимое основание и водород:
3)Взаимодействие с водой. Активные (щёлочные и щёлочно-земельные металлы) образуют растворимое основание и водород: 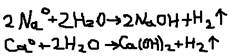 Металлы средней активности окисляют водой при нагревании до оксида:
Металлы средней активности окисляют водой при нагревании до оксида: 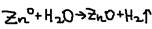 Неактивные (Au, Ag, Pt) – не реагируют. Вытеснение более активными металлами менее активных металлов из растворов их солей:
Неактивные (Au, Ag, Pt) – не реагируют. Вытеснение более активными металлами менее активных металлов из растворов их солей:  .
.
42)Лёгкие конструкционные материалы. Алюминий. Свойства, получение, применение в технике, важнейшие соединения.
Ответ: Металлические материалы играют значительную роль в народном хозяйстве и во многом определяют экономический потенциал страны. В настоящее время основным металлом в технике остается железо, производство которого в мире значительно превосходит производство других металлов. Стали и чугуны находят разнообразное применение в различных областях. Особенно велика их роль как конструкционных материалов, широко применяемых в машиностроении, строительстве, для изготовления полотна железных дорог и т.д. Роль железа как основного промышленного металла в ближайшем будущем, очевидно, будет сохраняться. Одновременно в последние десятилетия значительно возросла роль в современной технике и ряда других металлов. К их числу следует отнести и такой металл, как магний.
Интерес к магнию и сплавам на его основе обусловлен, с одной стороны, сочетанием в них важных для практического использования свойств, а с другой стороны, большими сырьевыми ресурсами магния. Основными достоинствами магниевых сплавов является малый удельный вес при сравнительно высоких прочностных свойствах, что определяет интерес к ним как легким конструкционным материалам. Благо-даря этому магниевые сплавы нашли важное применение в различных летательных аппаратах [1, 2]. Их применение для этих целей позволяет снизить собственный вес летательных конструкций и тем самым повысить полезный вес, уменьшить расход топлива. В легких конструкционных материалах, к числу которых относятся магниевые сплавы, заинтересованы и другие отрасли промышленности, в первую очередь наземный транспорт, в котором применение легких конструкционных материалов должно улучшить экономические характеристики эксплуатации. Велика сфера использования магния и магниевых сплавов как материалов со специальными химическими свойствами, например в источниках тока и для протекторов при защите стальных сооружений от коррозии [3]. В СНГ, как и за рубежом, имеются большие запасы минерального сырья магния, удобные для его извлечения. Это месторождения твердых солей, содержащих магний, а также рассолы ряда соляных озер. Кроме того магний может извлекаться из морской воды. Таким образом, для магния пока не стоит проблема истощения сырьевых ресурсов, которая приобретает все большее значение для многих других промышленно важных металлов. Хотя магний является одним из основных промышленных металлов, но объем его производства продолжает заметно уступать объему производства алюминия и стали. Хотите купить недвижимость на Украине? Тогда квартира Черновцы будет для вас идеальным вариантом. Квартиры, комнаты, дома, участки и другая недвижимость на любой вкус.
Магниевые сплавы в основном находят применение в качестве легких конструкционных материалов. Они отличаются высокой удельной прочностью, вследствие чего главным образом используются в различных летательных аппаратах. В большинстве сплавов, предложенных для этих целей, содержатся в качестве легирующих добавок редкие и дорогие элементы. В настоящее время магниевые сплавы представляют интерес для широкого использования в других отраслях современного машиностроения: в текстильной, автомобильной промышленности и других видах наземного транспорта. Для применения в этих целях важным является не только малый удельный вес магния, но и легкость его обработки. Кроме того, для этих отраслей должна быть обеспечена как можно более низкая стоимость магниевых сплавов.
Алюминий — мягкий, легкий, серебристо-белый металл с высокой тепло- и электропроводностью. Температура плавления 660°C. По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов. К достоинствам алюминия и его сплавов следует отнести его малую плотность (2,7 г/см3), сравнительно высокие прочностные характеристики, хорошую тепло- и электропроводность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов. Алюминий и его сплавы делятся по способу получения на деформируемые, подвергаемые обработке давлением и литейные, используемые в виде фасонного литья; по применению термической обработки — на термически не упрочняемые и термически упрочняемые, а также по системам легирования.
Получение: Впервые алюминий был получен Гансом Эрстедом в 1825 году. Современный метод получения разработали независимо друг от друга американец Чарльз Холл и француз Поль Эру. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке. Применение: Алюминий широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — легкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной пленкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки. Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий). Электропроводность алюминия сравнима с медью, при этом алюминий дешевле. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Правда, у алюминия как электротехнического материала есть неприятное свойство - из-за прочной оксидной пленки его тяжело паять. Благодаря комплексу свойств широко распространен в тепловом оборудовании. Внедрение алюминиевых сплавов в строительстве уменьшает металлоемкость, повышает долговечность и надежность конструкций при эксплуатации их в экстремальных условиях (низкая температура, землетрясение и т.п.). Алюминий находит широкое применение в различных видах транспорта. На современном этапе развития авиации алюминиевые сплавы являются основными конструкционными материалами в самолетостроении. Алюминий и сплавы на его основе находят все более широкое применение в судостроении. Из алюминиевых сплавов изготовляют корпусы судов, палубные надстройки, коммуникацию и различного рода судовое оборудование. Идут исследования по разработке пенистого алюминия как особо прочного и легкого материала. Драгоценный алюминий: В настоящее время алюминий является одним из самых популярных и нашедших широкое применение металлов. С самого момента открытия в середине XIX века его считали одним из ценнейших благодаря удивительным качествам: белый как серебро, легкий по весу и не подверженный воздействию окружающей среды. Стоимость его была выше цен на золото. Не удивительно, что в первую очередь алюминий нашел свое применение в создании ювелирных изделий и дорогих декоративных элементов. В 1855 г. на Универсальной выставке в Париже алюминий был самой главной достопримечательностью. Изделия из алюминия располагались в витрине, соседствующей с бриллиантами французской короны. Постепенно зародилась определенная мода на алюминий. Его считали благородным малоизученным металлом, используемым исключительно для создания произведений искусства. Наиболее часто алюминий использовали ювелиры. При помощи особой обработки поверхности ювелиры добивались наиболее светлого цвета металла, из-за чего его часто приравнивали к серебру. Но в сравнении с серебром, алюминий обладал более мягким блеском, чем обуславливалась еще большая любовь к нему ювелиров.
Так как химические и физические свойства алюминия сначала были слабо изучены, ювелиры сами изобретали новые техники его обработки. Алюминий технически легко обрабатывать, этот мягкий металл позволяет создавать отпечатки любых узоров, наносить рисунки и создавать желаемой формы изделия. Алюминий покрывался золотом, полировался и доводился до матовых оттенков. Но со временем алюминий стал падать цене. Если в 1854-1856 годах стоимость одного килограмма алюминия составляла 3 тысячи старых франков, то в середине 1860-х годов за килограмм этого металла давали уже около ста старых франков. Впоследствии из-за низкой стоимости алюминий вышел из моды. В настоящее время самые первые алюминиевые изделия представляют большую редкость. Большинство из них не пережило обесценивания металла и было заменено серебром, золотом и другими драгоценными металлами и сплавами. В последнее время вновь наблюдается повышенный интерес к алюминию у специалистов. Этот металл стал темой отдельной выставки, организованной в 2000 году Музеем Карнеги в Питсбурге. Во Франции расположен Институт истории алюминия, который в частности занимается исследованием первых ювелирных изделий из этого металла. В Советском союзе из алюминия делали общепитовские приборы, чайники и т.д. И не только. Первый советский спутник был выполнен из алюминиевого сплава. Другой потребитель алюминия — электротехническая промышленность: из него делаются провода высоковольтных линий передач, обмотки моторов и трансформаторов, кабели, цоколи ламп, конденсаторы и многие другие изделия. Кроме того, порошок алюминия применяют во взрывчатых веществах и твердом топливе для ракет, используя его свойство быстро воспламеняться: если бы алюминий не покрывался тончайшей оксидной пленкой, то мог бы вспыхивать на воздухе. Последнее изобретение — пеноалюминий, т.н. «металлический поролон», которому предсказывают большое будущее.
|
|
Дата добавления: 2015-04-24; Просмотров: 1160; Нарушение авторских прав?; Мы поможем в написании вашей работы!