
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фізичні властивості. Промислові способи отримання простих речовин залежать від того, в якому вигляді відповідний елемент знаходиться в природі
|
|
|
|
Отримання
Промислові способи отримання простих речовин залежать від того, в якому вигляді відповідний елемент знаходиться в природі, тобто що може бути сировиною для його отримання. Так, кисень, наявний у вільному стані, отримують фізичним способом — виділенням з рідкого повітря. Водень практично весь знаходиться у вигляді сполук, тому для його отримання застосовують хімічні методи. Зокрема, можуть бути використані реакції розкладу. Одним із способів отримання водню є реакція розкладання води від дією електричного струму.
Основний промисловий спосіб отримання водню — реакція метану, який входить до складу природного газу, з водою. Вона проводиться при високій температурі:
СН4 + 2Н2O = CO2 ↑ + 4Н2 −165 кДж
Зазвичай в лабораторії водень отримують взаємодією цинку з соляною кислотою.


Лінійчатий спектр видимого випромінювання атома водню
Водень — найлегший газ, він легший за повітря в 14,5 разів. Очевидно, що чим менше маса молекул, тим вище їх швидкість при одній і тій же температурі. Як найлегші, молекули водню рухаються швидше молекул будь-якого іншого газу і тим самим швидше можуть передавати теплоту від одного тіла до іншого. Звідси випливає, що водень має найвищу теплопровідність серед газоподібних речовин. Його теплопровідність приблизно в сім разів вище теплопровідності повітря.
Молекула водню складається з двох атомів Гідрогену — Н2. За нормальних умов, водень — це газ без кольору, запаху і смаку з густиною 0,08987 г/л (н.у.), температурою кипіння −252,76 °C, теплота згорянна 120,9 Дж/кг. Водень малорозчинний у воді — 18,8 мл/л. Але він добре розчиняється у багатьох металах (Ni, Pt, Pd тощо), особливо в паладії (850 об'ємів на 1 об'єм Pd). З розчинністю водню в металах пов'язана його здатність дифундувати через них; дифузія через вуглецевий сплав (наприклад, сталь) іноді супроводжується руйнуванням сплаву внаслідок взаємодії водню з вуглецем (так звана декарбонізація). Практично не розчинний в сріблі.
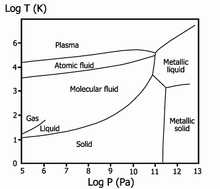

Фазова діаграма водню
Рідкий водень існує в дуже вузькому інтервалі температур від −252,76 до −259,2 °C. Це безбарвна рідина, дуже легка (густина при −253 °C — 0,0708 г/см3) і текуча (в'язкість при −253 °C — 13,8 пуаз). Критичні параметри водню дуже низькі: температура −240,2 °C і тиск 12,8 атм. Цим пояснюються труднощі при зрідженні водню.
Твердий водень має температуру плавлення −259,2 °C, густину 0,0807 г/см3 (при −262 °C) — білосніжна маса з кристалами гексагональної сингонії, просторова група — P 6/ mmc, з параметри комірки a = 0,378 нм і c = 0,6167 нм. При високому тиску водень переходить в металевий стан.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 426; Нарушение авторских прав?; Мы поможем в написании вашей работы!