
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Восстановленные формы этих кофакторов способны транспортировать водород и электроны к дыхательной цепи митохондрий или иных энергосопрягающих мембран
|
|
|
|
Организация и функционирование дыхательной цепи. В клетках эукариот дыхательная цепь расположена во внутренней мембране митохондрий, у дышащих бактерий – в цитоплазматической мембране и специализированных структурах – мезосомах, или тилакоидах. Компоненты дыхательной цепи митохондрий в порядке убывания окислительно-восстановительного потенциала можно расположить, как показано в 
Молярные соотношения компонентов дыхательной цепи являются постоянными, ее компоненты встроены в митохондриальную мембрану в виде 4 белково-липидных комплексов: НАДН-КоQН2-редуктаза (комплекс I), сукцинат-КоQ-редуктаза (комплекс II), КоQН2-цитохром c-редуктаза (комплекс III) и цитохром а-цитохромоксидаза (комплекс IV).
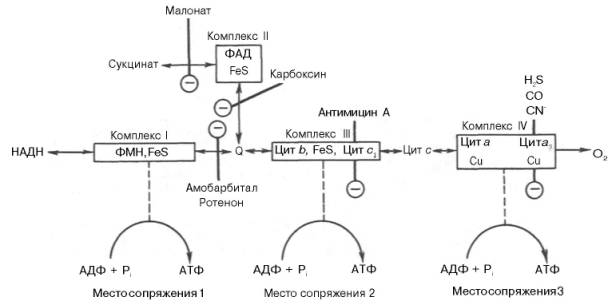
Если субстратом окисления служат α-кетокислоты, в переносе электронов на НАД+ участвуют липоатсодержащие дегидрогеназы. В случае окисления пролина, глутамата, изоцитрата и других субстратов перенос электронов происходит непосредственно на НАД+. Восстановленный НАД в дыхательной цепи окисляется НАДН-дегидрогеназой, содержащей железосерный белок (FeS) и ФМН и прочно связанной с дыхательной цепью.
KoQ (убихинон), необходимый компонент дыхательной цепи – способен находиться и в восстановленном, и окисленном состоянии. Это свойство определяет его роль в дыхательной цепи - служить коллектором восстановительных эквивалентов, поставляемых в дыхательную цепь через флавиновые дегидрогеназы. Содержание его значительно превосходит содержание других компонентов дыхательной цепи.
Дополнительным участником дыхательной цепи является железосерный белок FeS (негемовое железо). Он участвует в окислительно-восстановительном процессе, протекающем по одноэлектронному типу. Первый участок локализации FeS находится между ФМН и KoQ, второй - между цитохромами b и c1. Это соответствует тому факту, что со стадии ФМН путь протонов и электронов разделяется: первые накапливаются в митохондриальном матриксе, а вторые идут на гидрофобные переносчики - KoQ и цитохромы.
Цитохромы в дыхательной цепи выстроены в порядке возрастания окислительно-восстановительного потенциала. Они представляют собой гемопротеины, в которых простетическая геминовая группа близка к гему гемоглобина (у цитохрома b идентична). Ионы железа в составе гема при получении и отдаче электронов обратимо изменяют свою валентность.
В процессах тканевого дыхания наиболее важную роль играют цитохромы b, с1, с, а и а3. Цитохром а3 представляет собой терминальный участок дыхательной цепи – цитохромоксидазу, которая осуществляет окисление цитохрома с и образование воды. Элементарный акт представляет собой двухэлектронное восстановление одного атома кислорода, т.е. каждая молекула кислорода одновременно взаимодействует с двумя электрон-транспортными цепями. При транспорте каждой пары электронов во внутримитохондриальном пространстве может накапливаться до 6 протонов.
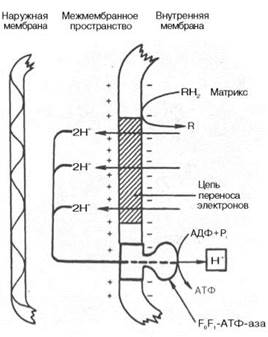
Окислительное фосфорилирование и дыхательный контроль. Функция дыхательной цепи – утилизация восстановленных дыхательных переносчиков, образующихся в реакциях метаболического окисления субстратов (главным образом в цикле трикарбоновых кислот). Каждая окислительная реакция в соответствии с величиной высвобождаемой энергии «обслуживается» соответствующим дыхательным переносчиком: НАДФ, НАД или ФАД. Соответственно своим окислительно-восстановительным потенциалам эти соединения в восстановленной форме подключаются к дыхательной цепи. В дыхательной цепи происходит разделение протонов и электронов: в то время как протоны переносятся через мембрану, создавая ΔрН, электроны движутся по цепи переносчиков от убихинола к цитохромоксидазе, генерируя разность электрических потенциалов, необходимую для образования АТФ протонной АТФ-синтазой. Таким образом, тканевое дыхание «заряжает» митохондриальную мембрану, а окислительное фосфорилирование «разряжает» ее.
Разность электрических потенциалов на митохондриальной мембране, создаваемая дыхательной цепью, которая выступает в качестве молекулярного проводника электронов, является движущей силой для образования АТФ и других видов полезной биологической энергии. Механизмы этих превращений описывает хемиосмотическая концепция превращения энергии в живых клетках. Она была выдвинута П. Митчеллом в 1960 г. для объяснения молекулярного механизма сопряжения транспорта электронов и образования АТФ вдыхательной цепи и быстро получила международное признание. Согласно хемиосмотической концепции, движение электронов по дыхательной цепи является источником энергии для транслокации протонов через митохондриальную мембрану. Возникающая при этом разность электрохимических потенциалов (ΔμH+) приводит в действие АТФ-синтазу, катализирующую реакцию
АДФ + Рi = АТФ
В дыхательной цепи есть только 3 участка, где перенос электронов сопряжен с накоплением энергии, достаточным для образования АТФ, на других этапах возникающая разность потенциалов для этого процесса недостаточна. Максимальная величина коэффициента фосфорилирования, таким образом, составляет 3, если реакция окисления идет с участием НАД, и 2, если окисление субстрата протекает через флавиновые дегидрогеназы. Теоретически еще одну молекулу АТФ можно получить в трансгидрогеназной реакции (если процесс начинается с восстановленного НАДФ):
НАДФН + НАД+ = НАДФ+ + НАДН + 30 кДж/моль. (4)
Обычно в тканях восстановленный НАДФ используется в пластическом обмене, обеспечивая разнообразные синтетические процессы, так что равновесие трансгидрогеназной реакции сильно сдвинуто влево.
Эффективность окислительного фосфорилирования в митохондриях определяется как отношение величины образовавшегося АТФ к поглощенному кислороду: АТФ/О или Р/О (коэффициент фосфорилирования). Экспериментально определяемые значения Р/О, как правило, оказываются меньше 3. Это свидетельствует о том, что процесс дыхания не полностью сопряжен с фосфорилированием. Действительно, окислительное фосфорилирование в отличие от субстратного не является процессом, в котором окисление жестко сопряжено с образованием макроэргов. Степень сопряжения зависит главным образом от целостности митохондриальной мембраны, сберегающей разность потенциалов, создаваемую транспортом электронов.
Несопряженное дыхание (свободное окисление) выполняет важные биологические функции. Оно обеспечивает поддержание температуры тела на более высоком уровне, чем температура окружающей среды. В процессе эволюции у гомойотермных животных и человека сформировались специальные ткани (бурый жир), функцией которых является поддержание постоянной высокой температуры тела за счет регулируемого разобщения окисления и фосфорилирования в митохондриальной дыхательной цепи. Процесс разобщения контролируется гормонами.
В норме скорость митохондриального транспорта электронов регулируется содержанием АДФ. Выполнение клеткой функций с затратой АТФ приводит к накоплению АДФ, который в свою очередь активирует тканевое дыхание. Таким образом, клеткам свойственно реагировать на интенсивность клеточного метаболизма и поддерживать запасы АТФ на необходимом уровне. Это свойство называется дыхательным контролем.
За сутки человек потребляет около 550 л (24,75 моля) кислорода. Если считать, что в тканевом дыхании за этот период восстанавливается 40 г атомов кислорода (20 молей), а величину Р/О принять за 2,5, то в митохондриях должно синтезироваться 100 молей, или около 50 кг АТФ! При этом часть энергии окисления субстратов расходуется на совершение полезной работы, не превращаясь в АТФ.
Свободное окисление. Одна из задач свободного (несопряженного) окисления – превращения природных или неприродных субстратов, называемых в этом случае ксенобиотиками (ксено – несовместимый, биос – жизнь). Они осуществляются ферментами диоксигеназами и монооксигеназами. Окисление протекает при участии специализированных цитохромов, локализованных чаще всего в эндоплазматическом ретикулуме, поэтому иногда этот процесс называют микросомальным окислением.
В реакциях свободного окисления участвуют также кислород и восстановленные дыхательные переносчики (чаще всего НАДФН). Акцептором электронов является цитохром Р-450 (иногда цитохром b5). Окисление субстрата протекает по следующей схеме:
SH + O2–> SOH.
Механизм действия оксигеназ включает изменение валентности входящих в их состав ионов двухвалентных металлов (железа или меди). Диоксигеназы присоединяют к субстрату молекулярный кислород, активируя его за счет электрона атома железа в активном центре(железо при этом становится трехвалентным). Оксигенация протекает как атака субстрата образующимся супероксид-анионом кислорода. Одной из биологически важных реакций такого типа является превращение β-каротина в витамин А. Монооксигеназы требуют участия в реакции НАДФН, атомы водорода которого взаимодействуют с одним из атомов кислорода, поскольку только одинэлектрон связывается с субстратом. К широко распространенным монооксигеназам относятся разнообразные гидроксилазы. Они принимают участие в окислении аминокислот, оксикислот, полиизопреноидов.
В процессе свободного окисления вследствие особенностей используемых цепей передачи электронов не происходит образованияАТФ; биологическая роль этих процессов заключается в метаболизме ряда природных и ксенобиотических субстратов. В последнем случае свободное окисление выполняет важную функцию модификации чужеродных соединений. К последним относятся лекарственные средства, гербициды, продукты загрязнения окружающей среды, в возрастающем количестве попадающие в организм сводой, пищей и атмосферным воздухом. Как правило, они имеют гидрофобные свойства. Многие из них являются канцерогенными. Их гидроксилирование в ходе свободного окисления облегчает последующую деструкцию и выведение из организма.
|
|
|
|
Дата добавления: 2015-05-08; Просмотров: 585; Нарушение авторских прав?; Мы поможем в написании вашей работы!