
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Адиабатный процесс газа
|
|
|
|
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС ГАЗА.
Изотермический процесс – процесс сообщения или. отнятия теплоты при постоянной температуре (t — const)
Для изотермического процесса идеального газа зависимость между начальными и конечными параметрами определяется формулами:
При постоянной температуре объём газа изменяется обратно пропорционально его давлению.
На pv- диаграмме изотермы идеального газа представляются равносторонней гиперболой. Площадь под кривой процесса численно выражает механическую работу в данном процессе. 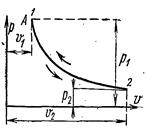
Работа 1 кг идеального газа находят из уравнений:
Так как в изотермическом процессе t = const, то для идеального газа
Изменение энтропии в изотермическом процессе
выразится следующей формулой:
Процесс протекающий без подвода и отвода теплоты, т.е. при отсутствии теплообмена с окружающей средой, называют адиабатным, а кривая этого процесса –адиабатой. Условия процесса: dq=0, q=0.
Т.к. dq=0, то согласно первому закону термодинамики:
и
Таким образом совершаемая рабочим телом механическая работа в адиабатном термодинамическом процессе равна уменьшению внутренней энергии тела, техническая работа при этом пропорциональна изменению (уменьшению) энтальпии. В обратимом диабатном процессе энтропия термодинамического тела не меняется: S=Const.
Уравнение адиабаты в системе координат pv – диаграммы при постоянной теплоёмкости () для идеального газа: где - показатель адиабаты
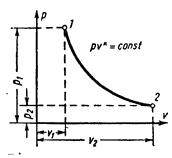
Зависимости между начальными и конечными параметрами процесса: между р и v,
между T и v
между р и T
Работу 1 кг газа находят по следующим формулам
Изменение внутренней энергии газа и работа адиабатного процесса равны по величине и противоположны по знаку..
Изменение внутренней энергии идеального газа в адиабатном процессе может быть также выражено уравнением
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 674; Нарушение авторских прав?; Мы поможем в написании вашей работы!