
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Равновесие жидкости и насыщенного пара
|
|
|
|
Рассмотрим процесс сжатия вещества при постоянной температуре. Первоначально вещество предполагается газообразным. Вначале, по мере уменьшение объема, давление газа будет расти (рис.1.9). По достижении объема V г давление перестает изменяться, а вещество перестает быть однородным – часть газа конденсируется в жидкость. Происходит расслоение вещества на две фазы: жидкую и газообразную. По мере дальнейшего уменьшения объема всё большая часть вещества переходит в жидкую фазу, причем переход осуществляется при постоянном объеме р н.п (давление насыщенного пара). После того как процесс конденсации заканчивается (это происходит при достижении объема V ж), дальнейшее уменьшение объема начинает сопровождаться быстрым ростом давления.
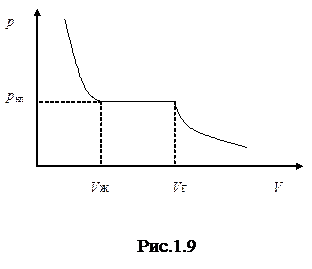 На рис.1.9 V г есть объем, занимаемый веществом в газообразном состоянии при давлении р н.п, V ж – объем вещества в жидком состоянии при том же давлении. При любом промежуточном значении объема часть вещества с массой mж будет находиться в жидком, а mп – в парообразном состоянии. Найдем отношение
На рис.1.9 V г есть объем, занимаемый веществом в газообразном состоянии при давлении р н.п, V ж – объем вещества в жидком состоянии при том же давлении. При любом промежуточном значении объема часть вещества с массой mж будет находиться в жидком, а mп – в парообразном состоянии. Найдем отношение  . Назовем удельным объемом
. Назовем удельным объемом  объем единицы массы вещества. Тогда, если масса вещества равна m, удельные объемы насыщенного пара и жидкости при давлении насыщенного пара будут равны:
объем единицы массы вещества. Тогда, если масса вещества равна m, удельные объемы насыщенного пара и жидкости при давлении насыщенного пара будут равны:
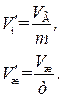 (1.76)
(1.76)
В состоянии, при котором масса жидкой фазы равна m ж, а масса пара m п, на долю жидкости будет приходиться объем V’ ж m ж, а на долю насыщенного пара – объем V’ п m п. В сумме оба эти объема должны быть равны объему V
V=V’ ж m ж +V’ п m п.
Подставив сюда выражение (1.76) для удельных объемов и заменив массу m суммой m ж + m п получим:
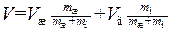 ,
,
отсюда
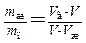 . (1.77)
. (1.77)
Таким образом, отношение масс жидкости и насыщенного пара в двухфазном состоянии равно отношению отрезков, на которые делит горизонтальный участок изотермы точка, изображающая состояние.
Отметим, что при температурах, далеких от критической, различий между объемами жидкости и пара бывает намного больше. Например, удельный объем насыщенного водяного пара при 100˚C в 1600 раз превышает удельный объем жидкой воды при той же температуре.
Итак, на диаграмме состояниям равновесия между жидкостью и насыщенным паром соответствует горизонтальный участок изотермы. Этот результат является общим для всех двухфазных состояний. Соотношение, аналогичное (1.77), имеет вид:
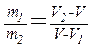
(m1 и m2 – массы вещества в первой и второй фазах).
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 1089; Нарушение авторских прав?; Мы поможем в написании вашей работы!