
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Показатели качества сточных вод
|
|
|
|
Температура. Кроме влияния на процессы осаждения температура является также важным технологическим параметром биологических процессов очистки, так как от нее зависят скорость биохимических реакций и растворимость в воде кислорода, необходимого для жизнедеятельности микроорганизмов.
Определяют температуру так же, как и в анализе природных вод. Как правило, температура сточных вод выше, чем природных.
Окраска. Бытовые сточные воды, как правило, окрашены слабо. Интенсивная окраска показывает наличие производственных сточных вод, особенно от предприятий легкой промышленности, где в большом количестве используются разнообразные красители. Окраска определяется в фильтрованных пробах в цилиндрах из бесцветного стекла и описывается на основе визуального наблюдения: розовая, слабо-желтая, буроватая и т.п. Интенсивность окраски характеризуют степенью разбавления исследуемой воды дистиллированной, при которой окраска исчезает. Результат записывают отношением, например 1:500 (те 1 — 1ч. исследуемой пробы, 500 — сумма 499 ч. разбавляющей воды и 1 ч. исследуемой).
Запах. Запах бытовых стоков довольно характерен и представляет собой смесь запахов фекалий и разложений органических веществ. Запах производственных стоков весьма разнообразен и зависит от вида производства. Для сточных вод описание запаха наиболее важно при появлении новых, ранее не встречавшихся оттенков, а также при резком возрастании интенсивности запаха, что свидетельствует о залповом сбросе концентрированных сточных вод отдельными производствами.
Запах определяется так же, как и при анализе природных вод. Сначала определяют характер запаха, затем по пятибалльной системе оценивают его интенсивность.
Прозрачность — показатель степени общей загрязненности воды. Прозрачность городских сточных вод обычно не превышает 3—5 см. Сточные воды после биологической очистки имеют прозрачность более 15 см. Прозрачность сточных вод определяется по шрифту.
Реакция среды. Сточные воды, сбрасываемые в систему водоотведения города, должны иметь значение рН в пределах 6,5—8,5. Требование обусловлено тем, что кислые и щелочные сточные воды разрушающе действуют на материал коллекторов и могут нарушать биохимические процессы очистки сточных вод.
Сухой и плотный остатки. В отличие от анализа природных вод сухой остаток сточных вод определяют из натуральной (нефильтрованной) пробы, поэтому он является показателем суммарного содержания загрязнений во всех агрегатных состояниях.
Плотный остаток определяется из фильтрованной пробы и показывает содержание веществ в коллоидном и истинно растворенном состоянии. В сточных водах, поступающих на сооружение биологической очистки, плотный остаток не должен превышать 10 г/л, так как жизнедеятельность микроорганизмов в более минерализованной среде нарушается. Определения проводят, как и в анализе природных вод.
Взвешенные вещества — одна из важнейших характеристик состава сточных вод. Этот показатель используется для расчета первичных отстойников и для определения количества образующихся осадков.
Концентрация взвешенных веществ в городских сточных водах составляет 100-500 мг/л. С достаточной степенью точности этот показатель может быть определен как разность сухого и плотного остатков.
Оседающие вещества — часть взвешенных веществ, которые оседают на дно отстойного цилиндра за 2 ч отстаивания в покое. Длительность отстаивания, равная 2 ч, определена на основании экспериментальных наблюдений, которые показали, что дальнейшее увеличение продолжительности процесса практически не изменяет результата, достигнутого за это время. В городских сточных водах оседающие вещества составляет 65—75% взвешенных веществ по массе.
В повседневной контрольной практике для определения оседающих веществ используют цилиндры Лисенко объемом 0,5 или 1 л. Нижняя часть цилиндра представляет собой пробирку с тонкой градуировкой до 0,1 мл. Количество оседающих веществ в городских сточных водах обычно не превышает 6—7 мл/л. После 2 ч отстаивания верхнюю часть отстоявшейся жидкости декантируют, а нижнюю с осевшими веществами переносят в стакан и определяют оседающие вещества по массе, так же как и взвешенные вещества. Таким образом, концентрацию оседающих веществ выражают по объему (мл/л) и по массе (мг/л).
Потери при прокаливании, зольность твердых примесей. Для многих технологических целей нужно знать содержание органической и минеральной частей твердой фазы воды. В этом случае высушенная твердая фаза любого определения (взвешенных веществ, оседающих веществ, сухого или плотного остатка) подвергается прокаливанию. Прокаливание проводят при температуре "красного" каления (500—600°С). Выгорают, т.е. улетучиваются в виде оксидов, углерод, водород, азот, сера и другие примеси. Остаток, называемый золой, после охлаждения взвешивают. Результаты выражают либо в абсолютных цифрах, либо в процентах. Потери при прокаливании — это абсолютное количество улетучившихся примесей; показатель выражается в мг/л. Зольность — отношение массы остатка после прокаливания к массе первоначально взятого твердого образца, выражается в процентах. Зольность взвеси городских сточных вод обычно находится в пределах 25—35%.
Химическая окисляемость определяет общее содержание в воде восстановителей — органических и неорганических, реагирующих с окислителями. В сточных водах преобладают органические восстановители, поэтому, как правило, всю величину окисляемости относят к органическим примесям воды.
Химическую окисляемость определяют с использованием в качестве окислителей бихромата калия К2Сr2O7 (бихроматная окисляемость) или иодата калия КIO3 (йодатная окисляемость). Бихроматную и йодатную окисляемость иначе называют химической потребностью в кислороде или ХПК. Это название точно отражает сущность определения окисляемости, так как оценивается количество кислорода, необходимое для окисления примесей воды, т.е. для перевода С в СO2, Н в Н2О, N в NH3 и т.д.
Различают ХПК теоретическую, вычисляемую по стехиометрическому уравнению окисления (для чего должен быть известен химический состав примесей), и экспериментальную, определяемую с использованием бихромата или йодата калия.
Теоретическая или расчетная ХПК органического вещества CxHyOzN подсчитывается следующим образом: составляется уравнение окисления и затем рассчитывается количество кислорода, требуемое для окисления 1 мг вещества (мг O2/мг):
CxHyOzN + (x+y/4 - z/2 - 3/4) O2 = xCO2 + [(y-3)/2] H2O + NH3
ХПК = (x+y/4 - z/2 - 3/4)32 / 12x + 1y + 16z + 14
Экспериментальная ХПК часто меньше теоретической, поскольку ряд органических веществ (красители, СПАВ, сложные углеводороды и др.) либо вовсе не окисляются бихроматом и йодатом в условиях определения, либо окисляются не до конца. Например, расчетная ХПК толуола С6Н5СН3 (мг О2/мг):
С6Н5СН3 + 9O2 = 7CO2 + 4H2O
ХПКС6Н5СН3 = (9 · 32) / (12 · 7 + 1 · 8) = 3,14
Экспериментальная ХПК толуола составляет 1,86 мг O2/мг. Расхождение объясняется тем, что в условиях определения бензольное кольцо не разрушается до конца.
Биохимическая окисляемость определяет содержание в воде органических примесей, которые могут быть окислены биохимическим путем. Окисление осуществляют аэробные гетеротрофные бактерии. По аналогии с ХПК окисляемость с использованием окислительной способности бактерий называют биохимической потребностью в кислороде, или БПК.
Значительное число бактерий — облигатных аэробов и факультативных анаэробов — способно существовать за счет использования загрязнений (примесей) воды в качестве источника питания. При этом часть использованных органических веществ расходуется на энергетические нужды, а другая часть — на синтез тела клетки. Часть вещества, расходуемая на энергетические потребности, окисляется клеткой до конца, т.е. до СO2, Н2O, NH3. Продукты окисления — метаболиты — выводятся из клетки во внешнюю среду. Реакции синтеза клеточного вещества идут также с участием кислорода. Количество кислорода, требуемого микроорганизмам на весь цикл реакции синтеза и получения энергии, и есть БПК.
В результате жизнедеятельности бактерий сточная вода очищается от исходных органических примесей, однако в ней остаются некоторые органические вещества, малодоступные или совсем недоступные бактериям для усвоения, и, кроме того, вода получает новые загрязнения — органические и неорганические — метаболиты.
Существует несколько способов аналитического измерения БПК — метод разведения, нитратный, хлораторный, распирометрический и др. На практике чаще всего применяют метод разведения. 1 часть сточной воды смешивают с n частями разбавляющей воды, смесь до предела насыщают растворенным кислородом путем продувки или встряхивания, разливают в инкубационные склянки и тщательно их герметизируют. Склянки оставляют в термостате при температуре 20°С на 5 сут или более. В склянке развивается сообщество микроорганизмов; величина уменьшения кислорода в склянке, умноженная на степень разведения, дает численную величину БПК.
Максимально возможное растворение кислорода в воде определяется в основном температурой. При температуре 20°С в дистиллированной воде растворяется 9,17 мг О2/л. Присутствие относительно небольшого количества различных примесей в инкубируемой смеси практически не снижает этого предела.
Определение БПК считают правильным, если к концу периода инкубации в склянке остается от 3 до 5 мг О2/л. Если к концу инкубации поглощено меньше 4 мг/л кислорода, то в последующих определениях разбавление уменьшают, если больше 6 мг/л, — увеличивают. Когда ожидаемая БПК приблизительно известна, степень разбавления нетрудно установить примерным расчетом. Можно принять, что в среднем потребление кислорода должно составлять 5 мг/л. Делением ожидаемой БПК на 5 получают необходимую степень разбавления исследуемой пробы. Для очень чистой воды с БПК менее 5 мг/л разбавление не требуется. Величина БПК указывается с индексом внизу, который означает длительность инкубации. Например, БПК5 — количество кислорода, потребленное за 5 сут инкубации; БПКt — то же, за t сут. Иногда указывается степень разбавления (что очень полезно для контроля правильности ее подбора) в виде отношения 1:(n+1). Например, запись БПК5(1:100) означает, что определена пятисуточная БПК при разведении одной части сточной воды 99 частями разбавляющей воды.
Разбавляющую воду готовят на основе дистиллированной воды, в которую добавляют фосфорные и аммонийные соли, хлорное железо, хлористый кальций и сернокислый магний. В сумме все соли составляют устойчивую буферную систему, которая позволяет поддерживать постоянное значение рН в течение любого периода инкубации, не изменяющееся от выделения в раствор СО2. Фосфорные и аммонийные соли, кроме того что они создают буферную среду, необходимы и в качестве элементов питания, если анализируются производственные стоки или природные воды, в которых эти элементы отсутствуют.
Существенный элемент разбавляющей воды — так называемая бактериальная затравка. Бактериальная затравка — это жидкость, содержащая культуру или смесь культур бактерий, способных разлагать органические вещества исследуемой воды. Когда анализируют городские сточные воды, внесения бактериальной затравки не требуется, поскольку в этих водах всегда содержится большое число сапрофитов, способных развиваться за счет примесей. При исследовании же растворов чистых химических веществ, производственных сточных вод или же природных и глубоко очищенных сточных вод искусственное заражение требуется. Обычно в качестве заражающей воды используют более или менее очищенную бытовую сточную воду из расчета 0,5 — 1 мг на 1 л разбавляющей воды. Расход кислорода на окисление внесенных с затравкой дополнительных загрязнений вычитается из общего расхода кислорода и в величину БПК исследуемой воды, таким образом, не входит.
Еще одним элементом разбавляющей воды является ингибитор процесса нитрификации. Расход кислорода на нитрификацию (т.е. на окисление азота аммиака) в величину БПК не включается. Однако при анализе слабозагрязненных сточных вод, когда концентрация С-содержащих веществ мала, к концу 5-суточного периода инкубации пробы эти вещества оказываются полностью израсходованными и в склянке усиленно развиваются процессы N-окисления, осуществляемые автотрофной микрофлорой. Расход кислорода на N-окисление достаточно велик и при малом расходе кислорода на С-окисление вследствие малой концентрации С-содержащих веществ ошибка за счет нитрификации может оказаться существенной.
Чтобы избежать этой ошибки, в инкубационную склянку вводят такие вещества, которые, не препятствуя развитию С-окисляющей микрофлоры, ингибируют развитие N-окисляющей микрофлоры (Nitrosomonas, Nitrobacter). В качестве ингибиторов используют метиленовую синюю, тиомочевину и другие вещества. Однако известно, что нет такого ингибитора N-окисления, который не оказывал бы одновременно угнетающего действия и на С-окислителей. Следствием этого являются заниженные результаты БПК пробы, поскольку в склянках слабо развиваются бактерии, ведущие С-окисление. В связи с этим нередко пользуются проведением эксперимента без введения ингибитора, изучают динамику изменения БПК по времени и рассчитывают требуемую величину с использо-ванием графика.
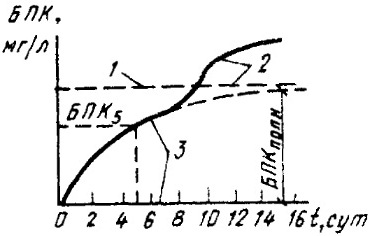
1 — БПКполн; 2 — потребление кислорода на N-окисление; 3 — то же, на С-окисление
Этот график позволяет определить величину БПКполн, т.е. суммарное потребление кислорода бактериями на получение энергии и синтез клеточного вещества.
Величина БПКполн замечательна тем, что она практически точно совпадает с истинным расходом кислорода на процесс очистки в действующих сооружениях. В склянках процесс длится несколько суток, в сооружениях — несколько часов, что объясняется различной концентрацией микроорганизмов в этих системах, В склянках она составляет микроколичества, а в сооружениях — макроколичества. Разница в концентрациях бывает в несколько миллионов раз.
Таким образом, величина БПКполн — важнейшая технологическая характеристика процесса биологической очистки воды в любых биоокислителях.
Экспериментально БПКполн определяют по появлению следов нитритов или нитратов. Для получения БПКполн требуется длительный период инкубации, продолжительность которого зависит от характера исследуемых примесей, концентрации бактерий, степени их адаптации. Обычно он больше 5 сут и может доходить до 30—40 сут. Для городских сточных вод он достигает примерно 8—15 сут. Поскольку вести оперативный контроль за работой сооружений, получая результаты анализов только через 8—15 дней, крайне неудобно, то выполняют определение БПК5, которая принята в качестве по стандартной характеристики почти во всем мире (в Финляндии — БПК). Следует помнить, что БПКполн — объективная величина, характеризующая степень загрязнения воды. Продолжительность периода инкубации, обеспечивающего получение БПКполн, зависит от условий инкубации, но величина БПКполн от этих условий не зависит. В то же время БПК5 — лишь неопределенная часть БПКполн, зависящая от характера окисляемых веществ и условий инкубации пробы.
Математическое описание процесса потребления кислорода при определении БПК. Кривые зависимости БПК от времени инкубации имеют сложный характер. Для удобства проведения технологического контроля используется наиболее простое математическое описание этой кривой (до начала нитрификации) по уравнению
БПКt = БПКполн (1 - 10-kt),
где k — константа скорости реакции, сут-1; t — длительность инкубации, сут.
Уравнение можно переписать относительно t:
t = 1 / k lg (БПКполн / БПКполн - БПКt)
Определим из уравнения время достижения БПКполн при условии БПКt = БПКполн:
t = 1 / k lg (БПКполн / 0) → ∞
Таким образом, исходя из формулы невозможно получить БПКполн за какое-то определенное время, а это противоречит экспериментальным наблюдениям и является результатом недостаточно точного математического описания процесса.
Для практического использования уравнений вводят ограничение, по которому за БПКполн принимают 90% ее величины. За время достижения БПКполнпринимается время, в течение которого процесс закончился на 99%:
БПКt = 0,99БПКполн;
t = 1 / k БПКполн (БПКполн - 0,99БПКполн) = 2 / k.
Время достижения БПКполн есть функция константы скорости процесса окисления; зависимость обратно пропорциональная и имеет вид гиперболы. Экспериментальные наблюдения показали, что k зависит от характера окисляемых веществ: для городских сточных вод она, как правило, изменяется от 0,15 до 0,25 сут-1, а для биологически очищенных — от 0,08 до 0,12 сут-1.
Время достижения БПКполн в зависимости от величины имеет следующие значения:
| k, сут-1 | 0,05 | 0,1 | 0,15 | 0,2 | 0,25 | 0,3 | 0,4 |
| Время достижения БПКполн, сут | 13,3 | 6,7 |
В практике очистки сточных вод весьма прочно укоренилось неверное представление о том, что БПКполн всегда равна БПК20. Это справедливо лишь в одном частном случае при k = 0,1 сут-1. Такое значение константы может иметь уже очищенная вода.
Если характер сточной воды изучен подробно и величина к известна из экспериментальных наблюдений, то можно вычислить коэффициент пересчета БПК5 в БПКполн:
K = БПКполн /БПК5 = 1 / 1 - 10-5k
Если принять для городских сточных вод k, равной 0,17, а для очищенных сточных вод — 0,08, то коэффициент пересчета будет: для городских сточных вод
K = 1 / 1 - 10-5·0,17 = 1,16
для очищенных сточных вод
K = 1 / 1 - 10-5·0,08 = 1,67
Важным показателем, характеризующим способность загрязнений сточных вод к биохимическому окислению, является отношение БПКполн/ХПК. Чем выше это отношение, тем большая часть органических примесей сточной воды может быть изъята в процессе биологической очистки. Считается, что применение биологических методов целесообразно при БПКполн/ХПК≥0,5.
Соединения азота и фосфора. При анализе сточных вод определяют азот общий, аммонийный, нитритный, нитратный. Показатель "азот общий" определяет содержание в воде органического и неорганического азота. Окисленные формы азота в неочищенных городских водах отсутствуют и появляются только в случае глубокой биологической очистки сточных вод.
Определению азотных и фосфорных соединений в сточных водах придается очень большое значение, поскольку азот и фосфор — важнейшие элементы питания бактерий. Как известно, одним из основных способов очистки сточных вод является биологический, осуществляемый микроорганизмами (бактериями, простейшими, водорослями и т.п.), которым создаются оптимальные условия для их существования и развития: по количеству подаваемого питания, температуре, кислородному режиму, степени смешения и др. Достаточность элементов питания для бактерий в биологических сооружениях определяется отношением основных показателей анализа БПКполн:М:Р. Здесь буквой N обозначен азот в аммонийной форме, а буквой Р — фосфор в виде растворенных фосфатов. В каждом конкретном случае это соотношение индивидуально, так как оно определяется составом продуцируемых клеток, который в свою очередь, зависит от состава очищаемой воды.
Если азота и фосфора меньше, чем требуется для очистки воды определенного состава, то их добавляют в виде фосфатов и хлористого аммония. Добавление солей для биологической очистки может быть необходимо только при обработке производственных сточных вод. В бытовых же водах, доступных бактериям, азота и фосфора всегда достаточно. Аммонийный азот образуется в большом количестве при гидролизе мочевины; кроме того, азот белковый в результате процесса аммонификации также переходит в аммонийную форму.
Что касается соединений фосфора, то следует заметить, что в физиологических выделениях человека его достаточно много. В последние годы количество фосфатов в сточных водах резко возросло в связи с тем, что в составе многих синтетических поверхностно-активных веществ (СПАВ) до 40% их массы составляют полифосфаты.
Сульфаты и хлориды. Концентрация сульфатов в городских сточных водах обычно находится на уровне 100- 150 мг/л, хлоридов — 150—300 мг/л. В сооружениях аэробной очистки эти показатели не претерпевают каких-либо изменений и их количество не имеет существенного значения, если общее солесодержание не превышает установленного предела. Концентрацию хлоридов важно знать при определении ХПК, так как хлориды окисляются бихроматом калия до молекулярного хлора. Поэтому при концентрации хлоридов более 200 мг/л требуется их предварительное осаждение или введение поправки к результату анализа ХПК.
Синтетические поверхностно-активные вещества. СПАВ — группа химических соединений, присутствие которых в сточных водах особенно угрожает санитарному состоянию водоема (водоприемника) и резко отрицательно сказывается на работе очистных сооружений. Появляются СПАВ в сточных водах в результате широкого применения их в быту и промышленности в качестве моющих средств, а также смачивающих, эмульгирующих, выравнивающих, дезинфицирующих препаратов. Наибольшее применение СПАВ находят в нефтяной, текстильной и кожевенной промышленности. В бытовых моющих средствах содержание активного агента достигает 20—30%.
Большинство СПАВ — органические вещества, состоящие из двух частей: гидрофобной и гидрофильной. Гидрофобная часть СПАВ соединена обычно с одной гидрофильной группой. В зависимости от физико-химических свойств гидрофильной части СПАВ делятся на три основных типа: анионоактивные, катионоактивные, неионогенные. Каждый тип в свою очередь делится на классы в зависимости от химического состава гидрофобной части.
Примерно 75—80% всех СПАВ, применяемых в быту и промышленности, составляют анионоактивные. Важнейшим из них являются: алкилсульфаты с общей формулой R—O—SO3Na (где R — углеводородный радикал с числом углеродных атомов от 10 до 20); алкилсульфонаты R—SO3Na (с числом углеродных атомов 12—15) и алкиларилсульфонаты R—C6Н4—SO3Na (с числом углеродных атомов в радикале 5—18).
Катионоактивные СПАВ в основном представлены нитрилами, аминами и четвертичными основаниями аммония. Например, поверхностно-активный амин может иметь формулу
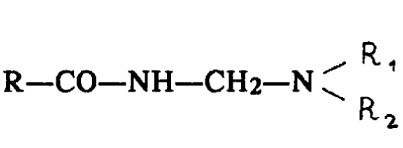
На втором месте по выпуску и использованию после анионоактивных веществ находятся неионогенные СПАВ. Поверхностно-активные вещества этого типа получают конденсацией окиси этилена с жирными кислотами, алкилфенолами, жирными спиртами, меркаптанами и т.д. Если гидрофобной частью является жирная кислота, СПАВ имеет формулу R—COO(С2Н4O)nH.
Присутствие СПАВ в сточных водах снижает способность взвешенных веществ к оседанию, тормозит биохимические процессы, способствует возникновению пены в сооружениях и водоемах. Наличие СПАВ в водоемах ухудшает процессы их самоочищения от остаточных загрязнений, вносимых с очищенными водами. Содержание анионных СПАВ в природной воде допускается не более 0,5 мг/л.
Вне зависимости от типа СПАВ рассматривают в трех категориях по отношению к степени биохимической окисляемости этих веществ: "мягких" СПАВ — с удалением и окислением в биологических сооружениях 75—85%, "промежуточных" — 60% и "жестких" — менее 60%. Нормами предусматривается, что на сооружения биологической очистки может поступать вода с содержанием "мягких" и "промежуточных" СПАВ не более 10—20 мг/л; сброс в канализацию "жестких" СПАВ не допускается.
Растворенный кислород. В загрязненных сточных водах либо растворенного кислорода не бывает совсем, либо его концентрация не превышает 0,5—1 мг/л. Определение количества растворенного кислорода имеет смысл при характеристике очищенных сточных вод и оценке степени насыщения растворенным кислородом биоокислителя. Минимальное содержание кислорода для нормальной жизнедеятельности микроорганизмов составляет 2 мг/л.
Очищенные сточные воды, выпускаемые в водоем, обычно содержат 4—8 мг/л растворенного кислорода.
Токсичные вещества. К группе токсичных элементов относятся тяжелые металлы: железо, никель, медь, свинец и цинк, а также мышьяк, сурьма, бор, алюминий, хром. Особенно важно контролировать содержание этих элементов в производственных сточных водах, поступающих на сооружения биологической очистки. Предельно-допустимые концентрации (ПДК) этих элементов очень низки. Так, для свинца ПДК для сооружений аэробной очистки составляет 1 мг/л, а для меди — 0,5 мг/л. При совместном присутствии нескольких токсичных элементов допустимая концентрация их рассчитывается по уравнению.
Кроме неорганических соединений в некоторых видах производственных сточных вод оказываются токсичные органические примеси, такие, как нефтепродукты, фенолы, красители и т.д. Допустимые концентрации этих веществ, не нарушающие работу очистных сооружений также регламентируются "Правилами приема производственных сточных вод в системе канализации населенных пунктов".
Биологические загрязнения. Микрофлора бытовых сточных вод представлена в основном микроорганизмами, выделяемыми из кишечника человека, смываемыми с тела и окружающих предметов. С физиологическими выделениями человека в сточную воду поступает несколько триллионов микробов в сутки. Среди них значительное число составляют кишечные палочки, лактобациллы, энтерококки, грибы, простейшие. При спуске в городскую канализацию некоторых производственных отходов в сточных водах оказываются специфические микроорганизмы (грибы, актииомицеты, дрожжи и т.д.), используемые в промышленности.
Для полной санитарно-эпидемиологической оценки сточных вод кроме микробного числа и коли-теста определяют третий показатель — содержание яиц гельминтов.
Содержание яиц гельминтов в сточной воде характеризует общую и видовую пораженность населения гельминтозами и позволяет оценить уровень санитарного состояния населенного пункта. В сточной воде наиболее часто встречаются яйца аскарид. На их долю приходится около 92% общего числа яиц гельминтов, остальные 8% составляют яйца власоглава, остриц, широкого лентеца.
Увеличение водопотребления наряду с повышением общей культуры населения приводит к постоянному снижению содержания яиц гельминтов в сточных водах. Так, в сточных водах московской канализации количество яиц гельминтов понизилось с 10 шт/л в 1960 г. до 0,5 шт/л в 1987 г.
|
|
|
|
Дата добавления: 2015-05-10; Просмотров: 3148; Нарушение авторских прав?; Мы поможем в написании вашей работы!