
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ЛД50 - летальная (смертельная) доза вещества, мг/кг живой массы, вызывающая гибель 50% подопытных животных
|
|
|
|
Пестициды
Пестицид – вещество (или смесь веществ) химического либо биологического происхождения, предназначенное для уничтожения вредных насекомых, грызунов, сорняков, возбудителей болезней растений и животных, а также используемое в качестве дефолианта, десиканта и регулятора роста.
Их классифицируют по следующим признакам:
- токсичности;
-названию групп вредных организмов, для уничтожения которых применяются (биологический принцип);
- характеру отравляющего действия ядов на организм вредителя (физиологический принцип);
- названию путей проникновения ядов в организм вредителя (физико-механический принцип);
- химическому составу, свойствам, способу получения (химический принцип).
По токсичности пестициды подразделяют на чегыре группы:
- сильнодействующие (ЛД50* < 50 мг/кг массы тела животного);
- высокотоксичные (ЛД50 = 50-200 мг/кг);
- среднетоксичные (ЛД50 = 200-1000 мг/кг);
- -малотоксичные (ЛД50 > 1000 мг/кг).
По биологическому принципу пестициды подразделяют на:
- акарициды (борьба с клещами);
- инсектициды (воздействие на насекомых);
- бактерициды (борьба с бактериями);
- гербициды (для уничтожения вредных растений);
- фунгициды (борьба с низшими растениями и грибами);
- лимациды (борьба с моллюсками);
- нематоциды (борьба с круглыми червями);
- зооциды (борьба с грызунами);
- адициды (борьба с тлей) и др.
К пестицидам относят также антисептики, применяемые для предохранения неметаллических материалов от разрушения их микроорганизмами; дефолианты, употребляемые для предуборочного удаления листьев; десиканты - для подсушивания растений; протравители - для предпосевной обработки семян, а также вещества для замедления прорастания овощей.
По физиологическому принципу пестициды подразделяют на:
- дыхательные;
- нервные;
- общетоксичные;
- протоплазменные;
- прямого физического воздействия на организм.
По физико-механическому принципу пестициды подразделяют на:
- контактные, вызывающие гибель насекомых при контакте вещества с любой его частью;
- кишечные, вызывающие отравление насекомых при попадании яда с пищей в организм;
-системные, способные передвигаться по сосудистой системе растений и отравлять поедающих их насекомых;
- фумиганты, действующие на насекомых в газообразном или парообразном состоянии через органы дыхания.
По химическому принципу пестициды подразделяют на:
- хлорорганические;
- фосфорорганические;
- карбаматы и т.д.
Приведенная классификация носит условный характер, так как ядохимикаты бывают комплексного действия.
К пестицидам предъявляют следующие основные требования. Они должны:
- обладать высоким специальным эффектом, одновременно быть нетоксичными и не оказывать побочного действия на обрабатываемые растения и животных;
Кристаллизующие реагенты – вызывают искусственную кристаллизацию переохлажденных облачных капель путем испарения (неорганические реагенты – AgI, PbI, CuI, органические реагенты – метальдегид, флороглюцин и др.). Искусственную кристаллизацию переохлажденных облачных капель можно вызвать путем испарения в облаке хладоагента или ввода в него кристаллизующих реагентов. В качестве хладоагента используются фреоны, твердая углекислота, жидкий пропан и др.
Искусственную кристаллизацию переохлажденных облачных капель можно вызвать путем испарения в облаке хладоагента или ввода в него кристаллизующих реагентов. В качестве хладоагента используется жидкий пропан, твердая углекислота и т.д. При испарении частичек твердой углекислоты температура окружающей среды понижается до минус 30 – 40°С, в результате чего происходит сублимационное образование зародышей ледяных кристаллов из комплекса молекул водяного пара. При испарении 1 г твердой углекислоты, сброшенной в облако, образуется от 5·1012 до 4∙1014 ледяных кристаллов (в зависимости от температуры окружающего воздуха и размера частиц). Применение хладоагентов особенно целесообразно при температуре облака, близкой к 0°С, когда большинство реагентов неэффективны. Несмотря на это, вследствие трудности хранения и доставки твердой углекислоты, предпочтение при борьбе с градом отдается кристаллизующим реагентам, вводимым в облако в аэрозольном состоянии. Реагент может быть получен в результате химического взаимодействия непосредственно в процессе обработки облака или использован в готовом виде и при обработке облака переведен в аэрозольное состояние.
В случае применения реагента в готовом виде его диспергирование может быть осуществлено распылением (дроблением), возгонкой и абляцией. Распыление осуществляется обычно за счет заряда взрывчатого вещества. Преимуществом этого метода является возможность использования веществ, не способных к возгонке и с низкой термической устойчивостью, недостатком - образование сравнительно крупных частиц, а значит, незначительного количества центров кристаллизации. Возгонка осуществляется в специальных генераторах или за счет сгорания термических смесей. Реагент может быть перемешан с компонентами термической смеси (пиротехнические составы) или находиться отдельно (метод абляции). При использовании его в пиротехнических составах он попадает в зону горения, подвергается воздействию окислительных или восстановительных элементов и высоких температур. В этих условиях реагент не должен разлагаться и терять своей активности. Поэтому в пиротехнических составах использование реагента с низкой термической устойчивостью не представляется возможным.
Основными параметрами, характеризующими кристаллизирующую способность веществ, являются температурный порог кристаллизации и выход активных частиц (N, ч/г вещества или состава).
Температурный порог кристаллизации - это наивысшая температура, при которой наблюдается появление ледяных кристаллов в переохлажденном водяном тумане при введении в него кристаллизующего реагента. Чем выше порог, тем лучше реагент.
Аэрозолеобразующие огнетушащие составы (АОС)
Пожары и взрывы природного и техногенного характера, приносящие существенные бедствия человечеству, к сожалению, не сокращаются как по числу, так и по масштабам человеческих жертв и материальных потерь. Поэтому проблема борьбы с этими катастрофами сохраняет свою актуальность как в настоящее время, так и в обозримом будущем. На протяжении длительной истории борьбы человека с огнем самым распространенным и наиболее эффективным средством пожаротушения была вода. Следует сказать, что и в настоящее время это положение, пожалуй, сохраняется. Да и в будущем, учитывая доступность воды и ее высокую пожаротушащую эффективность, определяемую эндотермическим эффектом испарения, вода сохранит свою приоритетность как пожаротушащее средство широкого назначения.
Однако для защиты от пожаров многих, в первую очередь технических, объектов вода и водосодержащие агенты или неприменимы, или по эффективности существенно уступают другим способам пожаротушения. Сюда относятся многочисленные электротехнические, нефтегазовые и др. объекты (электростанции, электрошкафы, автомобили, тепловозы, электровозы и пр.).
Для этих объектов применяются безводные способы пожаротушения: газовый, пенный, порошковый. В настоящее десятилетие довольно широкое распространение получило аэрозольное пожаротушение, основанное на ингибировании основных реакций горения.
Среди известных способов пожаротушения (поверхностное и объемное) использование аэрозолеобразующих пиротехнических составов является наиболее эффективным способом объемного пожаротушения за счет создания в защищаемом объеме помещения огнетушащего аэрозоля, не поддерживающего горение веществ и материалов.
В настоящее время разработан ряд пиротехнических аэрозолеобразующих огнетушащих составов (АОС) и зарядов для объемного тушения, при горении которых образуется аэрозоль, состоящий из инертных газов и ультрадисперсных твердых частиц химически активных соединений с развитой поверхностью, обладающих высоким ингибирующим действием на процессы горения органических веществ в кислороде воздуха. Конденсированная фаза аэрозоля состоит из частиц оксида, гидрооксида и солей калия размером от 0,4 до 4,0 мкм, газовая фаза – из азота, диоксида углерода и паров воды. Пожаротушащий эффект аэрозолей пиротехнических составов основан на ингибирующем, флегматизирующем, охлаждающем и кислородосвязывающем механизмах действия. Проблемой АОС является их сильное коррозионное действие на металлические поверхности.
Разработки широкого спектра пожаротушащих генераторов этого типа базировались на исследованиях механизма горения твердых ракетных топлив (ТРТ) и найденных закономерностях регулирования основных параметров процесса (скорости горения, температуры и т.д.). В частности, способ ингибирования двух основных экзотермических реакций (CO2+O2; H2+O2) горения углеводородного топлива был положен в основу разработки аэрозольгенерирующих составов ингибирующего типа.

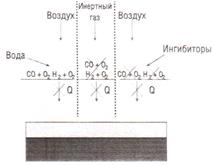
Принципиальная схема пожаротушения углеводородных веществ:
а - упрощенная схема горения;
б - принцип пожаротушения теплоемкими жидкостями, инертными газами и ингибиторами
Аэрозолеобразующие составы представляют собой специальные рецептурные композиции, основой которых являются горючие гетерогенные конденсированные смеси кислородосодержащих и горючих компонентов (базовых) с добавками (или без них) целевых и технологических компонентов.
К основным компонентам относятся:
– окислители (КNO3, KClO4, NaNO3, Ba(NO3)2
–технологические, отверждающие добавки, катализаторы и ингибиторы горения, стабилизаторы химической стойкости – суммарно
– модификаторы горения, обеспечавающие устойчивость процесса при давлениях, близких к атмосферному (эпоксидная и фенолоформальдегидная смола – идитол (С13Н11О2), дивинилнитрильные, бутадиеннитрильные, бутадиеновые (иногда в смеси с натуральным) каучуки.).
- газообразователи – дициандиамид (ДЦДА (C2H4N4)) (практически не выпускается промышленностью), меламин, уротропин и другие азотсодержащие полимеры.
Окислители АОС должны представлять собой твердое вещество с температурой плавления не ниже 60 °С и обладать следующими качествами:
содержать максимальное количество кислорода;
легко отдавать кислород при горении АОС;
содержать по возможности максимальное количество щелочного металла и инертного газа (например, азота);
не разлагаться взрывообразно при нагревании;
представлять собой химическое соединение,
устойчивое в интервале температур ±50... ±70 0С
и не разлагающееся под действием воды;
быть минимально гигроскопичным;
не оказывать токсического действия на человека; быть недефицитным и по возможности дешевым.
Таблица – Физико-химические свойства неорганических солей, применяемых в качестве окислителей в рецептурах современных АОС
| Окислитель | М | ρ, г/см3 | Тпл, 0С | Тразл, 0С | % [О] | % [N] | Реакция разложения |
| КClO4 | 2,5 | 525-588 | 530-619 | – | КСlO4 = КС1 + 2O2 | ||
| NaNO3 | 2,2 | 304-310 | 320-753 | 16,5 | 2NaNO3 = Na2O + N2 + 2,5O2 | ||
| KNO3 | 2,1 | 332-337 | 360-805 | 14,6 | 2KNO3 = К2O + N2 + + 2,502 | ||
| Ba(NO3)2 | 3,2 | 555-692 | 10,7 | Ba(NO3)2 =BaO + N2 + + 2,502 |
Горючие компоненты АОС должны удовлетворять следующим основным требованиям:
иметь теплоту горения, обеспечивающую получение высокоэффективного огнетушащего аэрозоля при давлении, близком к атмосферному;
достаточно легко окисляться за счет кислорода окислителя или воздуха;
при сгорании выделять большое количество газовой смеси, по возможности "инертной" (азот, углекислый газ, пары воды) и не содержащей токсичных, коррозионно-активных и озоноразрушающих соединений;
потреблять при сгорании минимальное количество кислорода; иметь по возможности минимальные взрывчатые свойства; быть химически и физически стойкими до ±70 °С, по возможности устойчивыми к действию слабых растворов кислот и щелочей;
быть малогигроскопичными (негигроскопичными); обладать по возможности одновременно свойствами связующих-цементаторов (или/и флешатизаторов, стабилизаторов) и другими специальными технологическими и эксплуатационными свойствами; легко измельчаться;
не оказывать токсического действия на человеческий
организм;
быть недефицитными и по возможности дешевыми.
Штатный состав 51-35-1. Состав разработан на ОАО «ЧПО им В.И. Чапаева»
Характеристики представлены в таблице.
| Шифр состава | Разработчики | Рецептура, % | Показатели | Технология изготовления | |
| 51-35-1 | НИИПХ | KNO3 70 Идитол 11 ДЦДА 19 | Тг=14400С САОС=40 г/м3 | Глухое прессование |
Окислитель - нитрат калия (KNO3),
Дициандиамид (ДЦДА) – полимер-газообразователь,
идитол – горючее связующее.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 1625; Нарушение авторских прав?; Мы поможем в написании вашей работы!