
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Поверхневі явища
|
|
|
|
Поверхневий натяг, як вільна поверхнева енергія на межі розділу двох фаз.
Натяг який виникає між 2 різними рідинами (рідина – рідина) називається граничним, на межі розділу рідина – тверде тіло, або рідина газ називається поверхневим.
Розглянемо молекулу яка знаходиться в середині рідкої фази:
Оскільки вона рівно оточена такими ж самими за природою молекулами рідини. Які знаходяться на строго однаковій відстані то сили притягання і відштовхування до сусідніх молекул будуть рівномірно скомпенсовані до центра цих молекул. Тому дана молекула залишається в стані спокою, а сума сил рівна 0.
В іншому положенні знаходиться молекула на межі розділу фаз (рідина – газ). Вона зазнає нерівноцінної дії сил притягання збоку сусідніх молекул газової фази і рідини. Так як молекула в газовій фазі розміщується на значно більших відстанях порівняно з розміром самої молекули, тому сили її притягання до поверхневої молекули настільки малі, що ними можна знехтувати. Тому вона не в змозі компенсувати силу притягання з боку молекули рідкої фази. Відповідно поверхнева молекула зазнає сил втягування, у нижні шари рідини, проте оскільки об’єм зайнятий іншими молекулами, які щільно розташовані, то вони виштовхують дану молекулу на поверхню молекули рідини. Таким чином у поверхневої молекули лишається надлишок незкомпенсованої енергії, яка називається вільною, оскільки її можна перевести в корисну роботу. Саме вона є причиною виникнення поверхневого натягу. Вільна поверхнева енергія прямо пропорційна площі поверхневого розділу фаз.
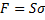 (1)
(1)
Де σ (сигма) – коефіцієнт пропорційності який називається поверхневим натягом, і залежить від природи речовини.
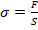 (2)
(2)
Отже, поверхневий натяг – це вільна поверхнева енергія, яка припадає на одиницю площі поверхні розділу фаз.
Вимірюється в:
[ 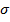 ]=[ Дж*м/м2]
]=[ Дж*м/м2]
В несистематичній системі одиниць:
[ 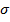 ]=[дим/см]
]=[дим/см]
Але поверхневий натяг можна розглядати як роботу яку необхідно затратити зовні для утворення нової одиниці площі поверхні розділу фаз:
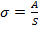 (3)
(3)
Тоді одиниці вимірювання поверхневого натягу:
[ 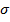 ]=[Дж/м2]
]=[Дж/м2]
В сгс: [ 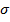 ]=[ерг/см2]
]=[ерг/см2]
Фактори які впливають на величину поверхневого натягу:
à Природа досліджуваної речовини (від розміру молекул та густини речовини) При збільшенні розміру молекули рідини відстань її до поверхневої молекули зменшується, так як об’єм залишається не змінним, тому сили притягання молекули поверхні до нижньої молекули речовини збільшується, надлишок нескомпенсованої поверхневої енергії зростає, і поверхневий натяг збільшується.
При збільшенні густини речовини зростає кількість самих молекул рідкої фази,тому відстань до поверхневої молекули зменшується, сили притягання зростають, поверхнева енергія збільшується,поверхневий натяг зростає.
à Температура. По мірі зростання температури збільшується величина кінетичної енергії молекул рідини. Відповідно швидкість хаотичного рух молекул зростає. Тому сили притягання поверхневої молекули і нижньої молекули рідкої фази зменшуються, надлишок нескомпенсованої поверхневої енергії зменшується,і величина поверхневого натягу знижується. При досягненні певної критичної температури, сили притягання між поверхневою молекулою і молекулою рідкої фази зникають так як відстань між ними стає більшою за розміри самих молекул, тому поверхнева молекула переходить в стан спокою. Надлишок нескомпенсованої поверхневої енергії зникає і поверхневий натяг теж зникає. Це відповідає перетворенню рідкої фази в газоподібну, тому критична температура відповідає температурі кипіння даної рідини. Оскільки поверхня розділу фаз зникає, тому і поверхневий натяг стає рівний 0.
à Тиск насиченої пари. ТНП
При збільшенні ТНП збільшується кількість самих молекул у газоподібній фазі (над поверхнею рідини), тому відстань між ними в парі починає зменшуватись,відповідно молекула газоподібної фази підходить на най блищу відстань до поверхневої молекули, тому між ними виникають невеликі сили притягання які частково починають компенсувати силу притягання поверхневої молекули до нижньої молекули рідини. Відповідно надлишок поверхневої енергії зменшується, і величина поверхневого натягу знижується. При подальшому зростанні тиску насиченої пари, при досягненні його критичного значення кількість молекул в газоподібній фазі стає настільки великою що відстань між ними і до поверхневої молекули стають рівні відстані між поверхневою молекулою і молекулою рідини. В результаті відбувається повна компенсація сил притягання з боку обох сусідніх молекул, тому надлишкова (нескомпенсована) поверхнева енергія зникає і поверхнева молекула переходить в стан спокою,а величина поверхневого натягу стає рівна 0. Це відповідає моменту повної конденсації пари у рідку фазу в результаті чого поверхня розділу фаз зникає і поверхневий натяг зникає.
à Концентрація розчину
До другого фактору
Кожна індивідуальна рідина намагається знизити надлишок нескомпенсованої поверхневої енергії до 0. Тому в природі це призводить до самовільного випадання атмосферних опадів, та утворення туману,хмар. Це зумовлено тим що найменшою площею поверхні володіє правильна сферична куля, тому рідина завжди випадає в формі крапель.
Тому сусідні краплі рідини починають самовільно зливатись утворюючи краплю більших розмірів яка володіє меншою площею поверхні ніш сума двох попередніх менших крапель. Проте при подальшому самовільному злитті розмір крапель стає настільки великий, що сила земного тяжіння ваги краплини перевищує вільно поверхневу енергію і рідина випадає на поверхню землі.
За впливом на поверхневий натяг чистої рідини всі речовини які існують у природі поділяють на 2 групи:
1. Поверхнево-активні речовини (ПАР)
2. Поверхневоінактивні речовини (ПНР)
ПАР – це речовини при додаванні яких до чистої рідини величина поверхневого натягу знижується. До них належать речовини дифільної будови(полярної або подвійної будови).
Їх молекули складаються з двох груп:
· Гідрофільної – яка споріднена за будовою до молекули води.(-OH,
-COH, -COOH, -SO3H, -SO2OH). Сама гідрофільна група позначається О.
· Гідрофобна – це група яка повністю відрізняється від молекули води.
До неї належать всі вуглеводневі радикали.
Схематично вона позначається:
малий радикал.
u eG1sTI9BTsMwEEX3SNzBGiQ2FXUaaGlDnApVYgMLoHAAJx6SCHscYjd1b890BcunP/rzfrlNzooJ x9B7UrCYZyCQGm96ahV8fjzdrEGEqMlo6wkVnDDAtrq8KHVh/JHecdrHVnAJhUIr6GIcCilD06HT Ye4HJM6+/Oh0ZBxbaUZ95HJnZZ5lK+l0T/yh0wPuOmy+9wen4Pn1bXbK02r2c7+sd2la2/QSrFLX V+nxAUTEFP+O4azP6lCxU+0PZIKwzItb3hIV5BsQ5zzfLEHUzPkdyKqU/wdUvwAAAP//AwBQSwEC LQAUAAYACAAAACEAtoM4kv4AAADhAQAAEwAAAAAAAAAAAAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNd LnhtbFBLAQItABQABgAIAAAAIQA4/SH/1gAAAJQBAAALAAAAAAAAAAAAAAAAAC8BAABfcmVscy8u cmVsc1BLAQItABQABgAIAAAAIQCoifYi8AEAAOsDAAAOAAAAAAAAAAAAAAAAAC4CAABkcnMvZTJv RG9jLnhtbFBLAQItABQABgAIAAAAIQBkf15L3QAAAAgBAAAPAAAAAAAAAAAAAAAAAEoEAABkcnMv ZG93bnJldi54bWxQSwUGAAAAAAQABADzAAAAVAUAAAAA " strokecolor="black [3040]"/> Великий радикал.
Таким чином до ПАР належать наступні класи речовин: спирти, альдегіди, карбонові кислоти та їх солі (мила).
Графічна залежність величини поверхневого натягу від концентрації ПАР при сталій температурі називається ізотермою поверхневого натягу.
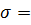 ¦(СПАР) при Т=const.
¦(СПАР) при Т=const.
Вчені Траубе та Дюкло незалежно один від одного дослідили вплив природи гомологічних рядів ПАР сформулювали правило Траубе – Дюкло.
В гомологічному ряді насичених жирних кислот при збільшенні вуглеводневого радикалу на групу СН2 величина поверхневого натягу зменшується у 3 – 3,5 рази, або поверхнева активність зростає у 3 – 3,5 рази.
σn/σn+1=3 – 3,5=γ - коефіцієнт активності Траубе – Дюкло.
ПНР - це речовини при додаванні яких до чистої речовини величина поверхневого натягу не змінюється або навіть зростає на незначну величину.
До них належать речовини:
1. Органічні речовини неполярної будови (полімери, вуглеводи) – не впливають на поверхневий натяг води.
2. Всі неорганічні речовини: мінеральні кислоти, луги, солі.
Відповідно графічна залежність поверхневого натягу від концентрації ПНР при сталій температурі має наступний вигляд.
Основні поняття сорбції. Рівняння Гіббса.
Сорбція – це явище поглинання одних речовин іншими.
Розрізняють два види сорбції: абсорбція, адсорбція.
Абсорбція – явище поглинання газу або рідини об’ємом рідини. Характерні для систем рідина – газ, рідина – рідина.
Наприклад, поглинання О2 об'ємом Н2О.
Адсорбція – явище поглинання газу або рідини поверхнею твердого тіла. Характерне для систем тверде тіло – газ, тверде тіло – рідина. Поглинання кисню поверхнею активованого вугілля.
Прийнято вважати більш щільну фазу (з більшою густиною) сорбентом, менш щільну – сорбатом. Тому розрізняють поняття абсорбент і адсорбент, абсорбат і адсорбат. Слід також розрізняти такі поняття як фізична сорбція – це явище поглинання одних речовин іншими, які утримуються певний проміжок часу, а потім відбувається їх відщеплення (десорбція)
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 6408; Нарушение авторских прав?; Мы поможем в написании вашей работы!