
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Розрахункові задачі. 1. Роздільну здатність класичної полярографії характеризує: а) ∆ ; б) ∆Ігр; в) ∆ ; г) ∆
|
|
|
|
Тестові завдання
1. Роздільну здатність класичної полярографії характеризує: а) ∆ 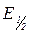 ; б) ∆Ігр; в) ∆
; б) ∆Ігр; в) ∆ 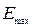 ; г) ∆
; г) ∆ 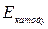 .
.
2. В методі класичної полярографії як робочий електрод використовують: а) золотий дисковий; б) ртутно-плівковий; в) вугільно-пастовий; г) ртутно-крапельний.
3. Головне призначення допоміжного електрода в класичній полярографії: а) стабілізувати потенціал робочого електроду; б) стабілізувати потенціал електроду порівняння; в) зменшити концентраційну поляризацію; г) збільшити перенапругу? – в мене інша відповідь
4. В інверсйній вольтамперометрії розгортка потенціалу на стадії запису вольтамперограми відбувається так, як зображено на рис.: (в мене інша відповідь)

| 
| 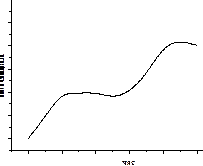
|
| а | б | в |
1. Ртутний краплинний електрод (маса ртуті, що витікає за 50 с, дорівнює 0,1 г, час життя 10 краплин ртуті дорівнює 38 с) застосовували для дослідження відновлення органічної сполуки з коефіцієнтом дифузії 5,4×10–4 см2/с. Для 5,3×10–4 М розчину цієї сполуки дифузійний струм складає 7,3 мкА. Розрахуйте число електронів (n), які беруть участь в реакції.- не для 2 курсу
2. Органічна сполука відновлюється в двоелектронному процесі на краплинному ртутному електроді (m = 1,89 мг/с, t = 2,12 с). Граничний дифузійний струм в 1,17×10‑3 М розчині цієї сполуки дорівнює 9,6 мкА. Розрахуйте коефіцієнт дифузії (D, см2/с) органічної сполуки.- не аналітична задача
3. В процесі відновлення кетону на краплинному ртутному електроді можуть брати участь один або два електрони. Для 1,0.10–3 М розчину кетону граничний дифузійний струм дорівнює 6,80 мкА (D =5,0.10–6 см2/с; m =2 мг/с; t =5 с). Розрахуйте кількість електронів, що беруть участь в електродному процесі.- теж саме
4. Відомо, що потенціали відновлення Zn2+ i Pb2+ на ртутно- графітовому електроді з 0,1 М розчину HNO3 складають відповідно – 1,2 та – 0,9 В. Мінімуми анодного струму на інверсійній вольтамперограмі спостерігаються при потенціалах –1,0 і –0,43 В, відповідно. Чи можна визначити кожний з іонів суміші методом інверсійної вольтамперометрії? Вкажіть які електрохімічні параметри (потенціал катодного накопичення, діапазон анодної розгортки потенціалу) потрібні для цього?
5. Встановили, що для 2,0.10-3 М розчину Zn(II) величина граничного дифузійного струму (Ігр) дорівнює 14,3 мкА. Розрахуйте на скільки відсотків зменшиться концентрація Zn(II) після пропускання цього струму крізь 10 мл розчину впродовж 10 хв? – це більше стосується електролізу аніж ВА
6. Полярограми 50,0 мл 5,0.10–4 М розчину Cd(ІІ) знімали одну за одною впродовж 30 хв. Граничний дифузійний струм дорівнював 4,0 мкА. Розрахуйте частку Cd(ІІ), яка відновилася за цей час до Cd(0). це більше стосується електролізу аніж ВА
7. Розрахуйте концентрацію цинку в аналіті (мг/л) на підставі наступних даних:
| Склад розчину у полярографічній комірці | Ігр, мкА |
| 20,0 мл 0,20 М HCl + 20,0 мл води | 10,2 |
| 20,0 мл 0,20 М HCl + 10,0 мл розчину аналіту + 10,0 мл води | 33,3 |
| 20,0 мл 0,20 М HCl + 10,0 мл 7,00×10–3 М Zn2+ + 10,0 мл води | 35,6 |
8. Розрахуйте концентрацію феруму в аналіті (мг/л) на підставі наступних даних:
| Склад розчину у полярографічній комірці | Ігр, мкА |
| 1. 50,0 мл 1 М НClО4 | 6,4 |
| 2. до розчину п.1 додали 5,0 мл розчину аналіту | 42,1 |
| 3. до розчину п.2 додали 1,0 мл 2,30×10–1 М Fe3+ | 59,3 |
9. Інверсійно-вольтамперометричне визначення вмісту Cu2+ у морській воді проводили за методом добавок. Результати наведено у таблиці:
| Розчин | І, мкА |
| 40 мл 0.1 М HNO3 | 0,112 |
| 20 мл 0.2 М HNO3 + 20 мл досліджуваного розчину | 0,866 |
| 20 мл 0.2 М HNO3 + 20 мл досліджуваного розчину + 5 мкл 10мг/л Cu2+ | 2,521 |
Розрахуйте вміст Cu2+ в зразку морської води в мг/л.
|
|
|
|
|
Дата добавления: 2015-05-29; Просмотров: 828; Нарушение авторских прав?; Мы поможем в написании вашей работы!