
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример решения
|
|
|
|
Газовая смесь 3
Газовая смесь 2
| № | Объемный состав смеси, % | P, | V, | t, | t 1 ¸ t 2, | |||
| п/п | H2 | CО | SO2 | CO2 | бар | м3 | оС | оС |
| 1000 - 2000 | ||||||||
| 900 - 1900 | ||||||||
| 800 - 1800 | ||||||||
| 700 - 1700 | ||||||||
| 600 - 1600 | ||||||||
| 500 - 1500 | ||||||||
| 400 - 1400 | ||||||||
| 300 - 1300 | ||||||||
| 200 - 1200 | ||||||||
| 100 - 1100 | ||||||||
| 1,5 | 9,5 | 100 - 500 | ||||||
| 2,5 | 8,5 | 200 - 600 | ||||||
| 3,5 | 7,5 | 300 - 700 | ||||||
| 4,5 | 6,5 | 400 - 800 | ||||||
| 5,5 | 5,5 | 500 - 900 | ||||||
| 6,5 | 4,5 | 600 - 1000 | ||||||
| 7,5 | 3,5 | 100 - 800 | ||||||
| 8,5 | 2,5 | 200 - 900 | ||||||
| 9,5 | 1,5 | 300 - 1000 | ||||||
| 1,2 | 6,4 | 400 - 1100 | ||||||
| 2,2 | 5,4 | 500 - 1200 | ||||||
| 3,2 | 4,4 | 600 - 1300 | ||||||
| 4,2 | 3,4 | 700 - 1400 | ||||||
| 5,2 | 2,4 | 800 - 1500 | ||||||
| 6,2 | 1,4 | 900 - 1600 |
Т а б л и ц а 3.3
| № | Мольный состав смеси, % | P, | V, | t, | t 1 ¸ t 2, | |||
| п/п | N 2 | О2 | H2O | CO2 | бар | м3 | оС | оС |
| 1,0 | 2,0 | 100 - 700 | ||||||
| 1,2 | 2,2 | 200 - 800 | ||||||
| 1,4 | 2,4 | 300 - 900 | ||||||
| 1,6 | 2,6 | 400 - 1000 | ||||||
| 1,8 | 2,8 | 500 - 1100 | ||||||
| 2,0 | 3,0 | 600 - 1200 | ||||||
| 2,2 | 3,2 | 700 - 1300 | ||||||
| 2,4 | 3,4 | 800 - 1400 | ||||||
| 2,6 | 3,6 | 900 - 1500 | ||||||
| 2,8 | 3,8 | 1000 - 1600 | ||||||
| 3,0 | 4,0 | 1200 - 1800 | ||||||
| 3,2 | 4,2 | 1300 - 1900 | ||||||
| 3,4 | 4,4 | 1300 - 1900 | ||||||
| 3,6 | 4,6 | 1400 - 2000 | ||||||
| 3,8 | 4,8 | 100 - 900 | ||||||
| 4,0 | 5,0 | 200 - 1000 | ||||||
| 4,2 | 5,2 | 300 - 1100 | ||||||
| 4,4 | 5,4 | 400 - 1200 | ||||||
| 4,6 | 5,6 | 500 - 1300 | ||||||
| 4,8 | 5,8 | 600 - 1400 | ||||||
| 5,0 | 6,0 | 700 - 1500 | ||||||
| 5,2 | 6,2 | 800 - 1600 | ||||||
| 5,4 | 6,4 | 900 - 1700 | ||||||
| 5,6 | 6,6 | 1000 - 1800 | ||||||
| 5,8 | 6,8 | 1100 - 1900 |
Дано
1. Смесь имеет следующий объемный состав:
СО2 = 12 %, r CO2 = 0,12,
N2 = 75 %, r N2 = 0,75,
H2O = 8 % r H2O = 0,08,
O2 = 5 % r O2 = 0,05.
____________________________
Всего: 100 % 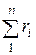 = 1,0.
= 1,0.
2. Объем смеси V = 3 м3;
Давление смеси Р = 10 бар;
Температура смеси t = 100 oC (T = 373 K).
3. Интервал температур для определения средней теплоемкости:
t 1 = 200 oC (T 1 = 473 K),
t 2 = 1000 oC (T 2 = 1273 K).
РЕШЕНИЕ
1. Определение кажущейся молекулярной массы смеси по формуле (1.6), через объемные доли компонентов:
m = 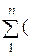 m i ri) = 44 × 0,12 + 28×0,75 + 18 × 0,08 + 32 × 0,05 = 29,32.
m i ri) = 44 × 0,12 + 28×0,75 + 18 × 0,08 + 32 × 0,05 = 29,32.
2. Определение массового состава смеси по формуле (1.4):
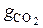 =
= 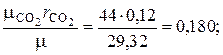
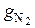 =
= 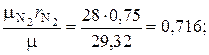
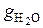 =
= 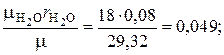
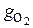 =
= 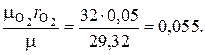
________________________________
Проверка: 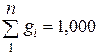
3. Определение кажущейся молекулярной массы смеси по формуле (1.7), через массовые доли компонентов:
m = 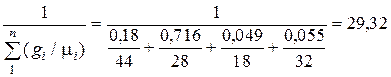 .
.
4. Определение газовых постоянных компонентов смеси:
R CO2= 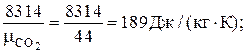
R N2= 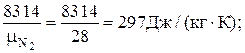
R H2O = 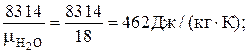
R O2= 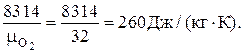
5. Определение газовой постоянной смеси по формуле (1.8), через объемные доли компонентов:
R = 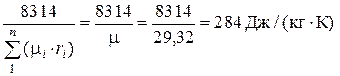
и по формуле (1.9), через массовые доли компонентов:
R = 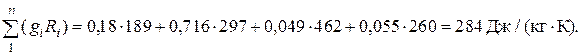
6. Определение парциальных давлений компонентов по формуле (1.10), через объемные доли:
Р со2= Р r co2= 10 × 0,12 = 1,2 бар;
Р N2= Р r N2= 10 × 0,75 = 7,5 бар;
Р H2O = Р r H2O = 10 × 0,08 = 0,8 бар;
Р О2 = Р r O2= 10 × 0,05 = 0,5 бар.
–––––––––––––––––––––––––––––
Проверка по закону Дальтона:
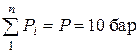 .
.
То же через массовые доли, по формуле (1.11):
Р СО2= Р g CO2 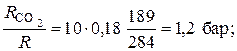
P N2= P g N2 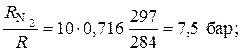
P H2O = P g Н2О 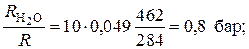
Р О2= Р g O2 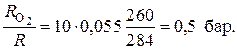
–––––––––––––––––––––––––––––––––––––––
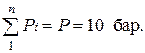
7. Определение массы смеси по уравнению Клапейрона:
m = 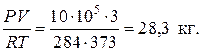
8. Определение масс компонентов смеси:
m СО2= m g CO2= 28,3 × 0,18 = 5,1 кг;
m N2= m g N2= 28,3 × 0,715 = 20,25 кг;
m H2O = m g H2O = 28,3 × 0,049 = 1,39 кг;
m O2= m g O2= 28,3 × 0,055 = 1,56 кг.
––––––––––––––––––––––––––––––––
Проверка: 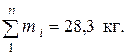
9. Определение истинных теплоемкостей смеси при t = 100 oC:
а) мольные:
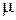 Ср =
Ср = 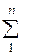 (m СРi × ri) = 40,2 × 0,12 + 29,1 × 0,75 + 34,1 × 0,08 + 29,9 × 0,05 =
(m СРi × ri) = 40,2 × 0,12 + 29,1 × 0,75 + 34,1 × 0,08 + 29,9 × 0,05 =
= 30,9 кДж/ (кмоль×К);
m СV = m CP - 8,314 = 30,9 - 8,314 @ 22,6 кДж/(кмоль×К);
б) массовые:
CP = m CP /m = 30,9/ 29,32 = 1,05 кДж/(кг×К);
СV = m CV / m = 22,6/29,32 = 0,771 кДж/(кг×К);
в) объемные:
С ¢ Р = m СP /22,4 = 30,9/22,4 = 1,38 кДж/(м3×К);
С ¢ V = m CV /22,4 = 22,6/22,4 = 1,01 кДж/(м3×К).
10. Определение средних теплоемкостей смеси:
а) мольные:
m СР ½01000 = 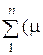 Срi ½01000 ri) = 49,4 × 0,12 + 31,2 × 0,75 + 38,6 × 0,08 +
Срi ½01000 ri) = 49,4 × 0,12 + 31,2 × 0,75 + 38,6 × 0,08 +
+ 33,1 × 0,05 = 34,1 кДж/(кмоль×К);
mСР½0200 = 40,1× 0,12 + 29,1× 0,75 + 34,1 × 0,08 + 29,9 × 0,05 =
= 30,9 кДж/(кмоль×К);
m Ср 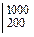 =
= 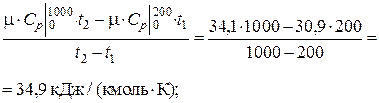
m СV 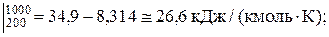
б) массовые:
СР 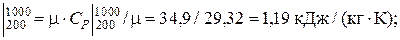
С V 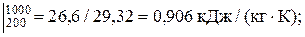
в) объемные:
С¢ Р 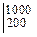 = m СР
= m СР 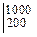 / 22,4 = 34,9/22,4 = 1,56 кДж/(м3×К);
/ 22,4 = 34,9/22,4 = 1,56 кДж/(м3×К);
С¢ V 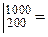 m CV
m CV 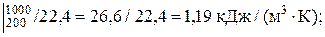
Примечание. Средние мольные теплоемкости берутся из табл. 5.2 для температур t 1 = 200 оС и t 2 = 1000 оС.
11. Определение теплоты на нагревание:
а) двух киломолей смеси:
Q 1 = N × m CP 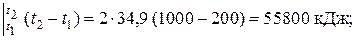
б) 5 м3 смеси:
Q 2 = V 0 × C ¢ P 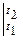 (t 2 - t 1) = 5 × 1,56 (1000 - 200) = 6230 кДж;
(t 2 - t 1) = 5 × 1,56 (1000 - 200) = 6230 кДж;
в) 7 кг смеси:
Q 3 = m × CP 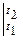 (t 2 - t 1) = 7× 1,19 (1000 - 200) = 6670 кДж.
(t 2 - t 1) = 7× 1,19 (1000 - 200) = 6670 кДж.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 385; Нарушение авторских прав?; Мы поможем в написании вашей работы!