
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Інструкційна карта
|
|
|
|
Внутрикомплексные соединения (хелаты) ЭДТА. Трилон Б. Зависимость состава раствора ЭДТА от рН раствора. Возможность комплексонометрического определения многозарядных ионов в кислой среде.
Комплексоны являются производными аминополикарбоновых кислот. Титрование с использованием компликсонов (полидентатных, т. е. имеющими несколько донорных центров, органических реагентов) называют комплексонометрией. Это основной метод определения металлов. Начало применению комплексонов как аналитических органических реагентов положил Г. Шварценбах (1945 г). Простейшим комплексоном, известным под названием комплексон I, служит трехосновная нитрилотриуксусная кислота (сокращенно H3Y). Наибольшее значение приобрела этилендиаминтетрауксусная кислота ЭДТУ), комплексон II, четырехосновная кислота (сокращенно H4Y) или этилендиаминтетрауксусная кислота:

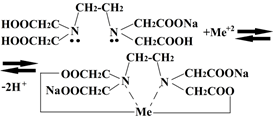 Комплексон III, как и другие комплексоны, образует растворимые внутрикомплексные соли со многими металлами. При этом металл замещает атомы водорода карбоксильных групп – СООН, а также связывается координационной связью с атомами азота:
Комплексон III, как и другие комплексоны, образует растворимые внутрикомплексные соли со многими металлами. При этом металл замещает атомы водорода карбоксильных групп – СООН, а также связывается координационной связью с атомами азота:
Образующиеся комплексные соединения очень прочны, в таблице, представленной ниже, приведены константы образования некоторых этих комплексов.
| Константы образования комплексов при 200С и ионной силе 0,1 | |||||
| Ион металла | lg KMeY | Ион металла | lg KMeY | Ион металла | lg KMeY |
| Fe3+ | 25,1 | Zn2+ | 16,50 | Ca2+ | 10,70 |
| Th4+ | 23,1 | Cd2+ | 16,46 | Mg2+ | 8,69 |
| Cu2+ | 18,62 | Al3+ | 16,13 | Sr2+ | 8,63 |
| Ni2+ | 18,62 | Mn2+ | 13,79 | Ag+ | 7,3 |
Хелаты (лат. chelate — клешня) — клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными лигандами. Хелаты содержат центральный ион (частицу) — комплексообразователь и координированные вокруг него лиганды. Внутренняя сфера хелата состоит из циклических группировок, включающих комплексообразователь.
Иногда разделяют понятия хелатного и внутрикомплексного соединения. Второе определение применяют в случае, когда атом-комплексообразователь замещает протон лиганда в соединении.
Очень важно для анализа то, что почти со всеми ионами металлов в различных условиях образуются комплексные соединения строго определенного состава, а именно такие, в которых соотношение ионов металла к лиганду равно 1:1.
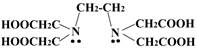 Этилендиаминтетрауксусная кислота (ЭДТА) - э то белое кристаллическое вещество, малорастворимое в воде, так, при 200 растворимость её всего 28,3 мг на 100 мл. растворимость Н4Y минимальна при рН 1,6-1,8. При повышении и понижении концентрации ионов водорода растворимость растет.
Этилендиаминтетрауксусная кислота (ЭДТА) - э то белое кристаллическое вещество, малорастворимое в воде, так, при 200 растворимость её всего 28,3 мг на 100 мл. растворимость Н4Y минимальна при рН 1,6-1,8. При повышении и понижении концентрации ионов водорода растворимость растет.
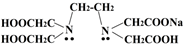 Трилон Б является торговым названием динатриевой соли этилендиаминтетрауксусной кислоты и представляет собой кристаллический порошок белого цвета. Схема действия его основана на извлечении ионов металла из нерастворимых солей металлов и замещения их на ионы натрия, почти все соли которого растворимы в воде, причем независимо от валентности металла 1 молекула трилона реагирует с 1 молекулой металла. Трилон Б не является окислителем, и не взаимодействует с металлами, находящимися в нулевой степени окисления. Стандартными веществами, по которым определяется титр и нормальность трилона CaCO3, ZnSO4·7H2O, MgSO4•7H2O
Трилон Б является торговым названием динатриевой соли этилендиаминтетрауксусной кислоты и представляет собой кристаллический порошок белого цвета. Схема действия его основана на извлечении ионов металла из нерастворимых солей металлов и замещения их на ионы натрия, почти все соли которого растворимы в воде, причем независимо от валентности металла 1 молекула трилона реагирует с 1 молекулой металла. Трилон Б не является окислителем, и не взаимодействует с металлами, находящимися в нулевой степени окисления. Стандартными веществами, по которым определяется титр и нормальность трилона CaCO3, ZnSO4·7H2O, MgSO4•7H2O
Расчеты анализа зависят от рН раствора, поэтому практически всегда используют буферные растворы. Н4Y – многоосновная слабая кислота:
Н4Y = Н+ + Н3Y - ; Н3Y- = H+ + Н2Y2 - ; Н2Y2- = Н+ + НY3-; НY3- = Н+ + Y4- .
Н4Y = 4Н+ + Y4-; kобщ=k1·k2·k3·k4
Металлы образуют комплексные соединения со всеми видами анионов ЭДТА, однако наиболее прочные комплексы образуются с Y4- (у которого нет протонов). В связи с этим, наиболее прочные комплексы образуются в щелочной среде.
| Доля рН ʈ4 процентное содержание Y4- | Наиболее устойчивые комплексы с многозарядными ионами могут образовываться и в кислой среде. К ним относятся комплексы с Bi3+ (lgK = 27,9); Fe3+ (lgK = 25,1); Cr3+ (lgK = 23,0) и т. д. Менее устойчивые комплексы с ЭДТА образуют Ba2+ (lgK = 7,8); Mg2+ (lgK = 8,7); Ca2+ (lgK = 10,7) и т. д. Их определение комплексонометрическим титрованием проводят в щелочной среде. | ||
| pH | ʈ4 = 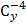 /С0 , % /С0 , %
| рН | ʈ4 |
| 3,0 | 2·10-9 | 8,0 | 5,4·10-1 |
| 4,0 | 3,6·10-7 | 9,0 | 5,2·10-2 |
| 5,0 | 3,5·10-5 | 10,0 | 3,5·10-1 |
| 6,0 | 2,2·10-3 | 11,0 | 8,5·10-1 |
| 7,0 | 4,8·10-2 | 12,0 | 9,8·10-1 |
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 433; Нарушение авторских прав?; Мы поможем в написании вашей работы!