
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Криминалистика 2 страница
|
|
|
|
F)  - сіңірген қабаттың қалыңдығы
- сіңірген қабаттың қалыңдығы
Жоғары жиілікті кондуктометрияда зерттелетін ерітіндінің анықталатын шамаларын есептейтін теңдеулер
A) 
B) 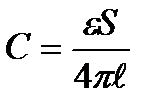
H) 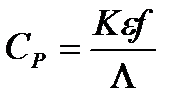
Жарықтың сіңірілуін және түсінің қарқындылығын сандық анықтау үшін қолданылатын приборлар
A) колориметрлік пробиркалар мен цилиндрлер, компараторлар
B) колориметрлер мен фотометрлер
C) фотоэлектрлік колориметрлер, спектрофотометрлер
Жабысқақ материалдардан сынама алуға қойылатын талаптар:
C) материалдарды мұқият араластыру керек
E) сынаманы материал массасының орта бөлігінен алу керек
H) сынаманы материал массасының жоғары және төменгі бөлігнен алу керек
Жұқа қабатты хроматографияда сорбент ретінде қолданылатын заттар қатары:
A) силикагель
B) алюминий оксиді
C) крахмал
Интерферометрия әдісінде зерттелетін ерітіндінің концентрациясын есептеу, талдау және түзету теңдеулері:
D)  ; анализденетін ерітіндінің концентрациясы
; анализденетін ерітіндінің концентрациясы
F) 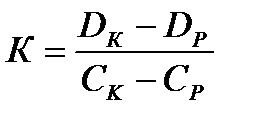 ; қайта есептеу коэффициенті
; қайта есептеу коэффициенті
G)  ; түзету коэффициенті
; түзету коэффициенті
Интерферометрия әдісінде жолақтың ығысуы зерттелетін еріткіштің сыну көрсеткішімен байланысқан теңдеумен бейнеленеді: 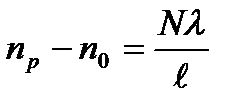 ; мұндағы
; мұндағы
A)  – ерітінді мен еріткіштің сыну көреткіштері
– ерітінді мен еріткіштің сыну көреткіштері
B)  - интерференциялық жолақтың ығысуы
- интерференциялық жолақтың ығысуы
C)  - толқын ұзындығы;
- толқын ұзындығы; 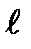 - кюветаның ұзындығы
- кюветаның ұзындығы
Индикаторлық электродқа қойылатын талаптар:
A) потенциал тез қойылу керек
B) қайтымды болу керек
C) химиялық тұрақты болу керек
Иодометриялық титрлеуде біріншілік стандартты заттар қатары:
B) иод ерітіндісі
C) калий дихроматы
D) калий броматы
Иодид ионы хлор суымен күшті тотығады, нәтижесінде хлороформ қабаты күлгін түске боялады. Хлор суын ары қарай қосқанда күлгін түс жоғалады. Сондай-ақ иодид ионы күміс нитратымен сары тұнба түзеді. Осы анықтауларды дәлелдейтін реакция теңдеулері:
D) СІ2 + 2І- →І2+ 2СІ-
E) 5СІ2 +І2 + 6Н2O → 2HIO3 + 10НCI
F) Ag + І- → AgІ(қ)
Концентрациясы 0,5%-ды НСООН құмырсқа қышқылының Н+ ионының концентрациясының, рН және иондану дәрежесінің α мәндері:
A) 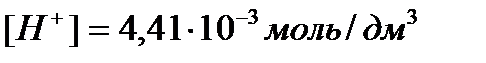
D) 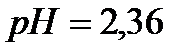
G) 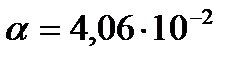
Күкіртсутек қышқылына сәйкес келетін жалпы және сатылы диссоциациялану теңдеулері мен диссоциациялану константалары: Н2S ↔ H+ + HS-;  : НS- ↔ H+ + S2-;
: НS- ↔ H+ + S2-; 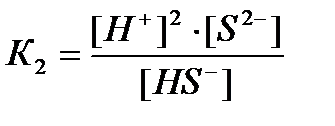 : Н2S ↔ 2H+ + S2-;
: Н2S ↔ 2H+ + S2-; 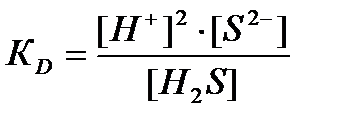
Көп негізді қышқылдың Н2А диссоциациялану константасы:
C) 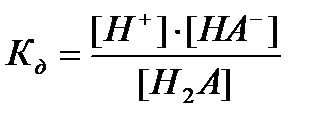
E) 
F) 
Комплексті қосылыстардың комплексті ионның заряды бойынша жіктелуі және сәйкес қосылыстың формуласы:
C) бейтарап – [Pt(NH3)2CI2]
F) катиондық – [Со(NH3)4]2+
G) аниондық – [Ғе(СN6]4-
Комплексті иондардың құрылысы:
B) комплекс түзуші
D) лигандалар
F) координациялық сан
Комплексті қосылыстар түріндегі металл катиондарын экстракциялау үшін қолданылатын хелат түзуші агенттер қатары:
D) 8-оксихинолин
E) диацетилдиоксим
F) дитизон
Күміс тұздарын түзетін топтасқан реактиві азот қышқылының қатысындағы АgNО3 болатын аниондардың қатары:
D) CI-, Br-,,
E) I-, C6H5COO-
F) CN-,SCN-
Күкіртті қышқылдың тұздарына минералды қышқылдармен әсер еткенде қышқыл түзіледі, ол қышқылдық оксид пен суға дейін ыдырайды. Бөлінген оксидті і иісі бойынша немесе йод, КМnO4 ерітінділерін түссіздендіруі бойынша табады. Осы анықтауларды дәлелдейтін реакция теңдеулері:
A) Na2SO3 + 2НСІ → 2NaСІ + Н2SO3; Н2SO3 → SO2(г) + Н2O
E) SO2+ І2 + 2Н2O→ 2НІ + Н2SO4
H) 5SO2+ КМnO4 + 2Н2O→ 2МnSO4 + К2SO4 + 2Н2SO4
Күшті тотықтырғыштардың әсерінен қышқыл ортада хлоридтер бос газға дейін тотығады, бөлінген газды иісі бойынша немесе иодидкрахмал қағазының көгеруі бойынша табады, сонымен қоса хлорид ионы күміс нитратымен ақ тұнба түзеді. Осы анықтауларды дәлелдейтін реакция теңдеулері:
B) MnO2 + 2КСІ + 2Н2SO4 → СІ2↑ + MnSO4 + 2Н2O + К2SO4
D) СІ2 + 2І- →І2+ 2СІ-
F) Ag + СІ- →AgСІ(қ)
Көлемі 5 см3 Н2SO4 ерітіндісінен массасы 0,4582г ВаSO4 тұнбасы алынғанда, Н2SO4 ерітіндісінің пайыздық концентрациясы, тұнбаның молярлық массасы және реакция теңдеуі:
A) М = 200,40 г/моль
D) 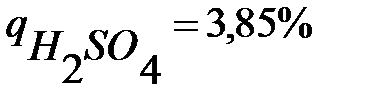
H) SO42- +Ba2+ → BaSO4
Кристалдық тұнбаларды тұндыру ережелері:
C) сұйылтылған ерітіндіні тұндырғыштың сұйылтылған ерітіндісімен тұндыру керек
E) тұндырғышты өте баяу, тамшылатып құю керек
H) ерітіндіні шыны таяқшамен үздіксіз араластырып отыру керек
Кристалдық тұнбаларды тұндыру ережелері:
C) ыстық ерітіндіден тұнбаға түсіру керек
E) ерітінді салқындағаннан кейін тұнбаны фильтрлеу керек
H) тұндыру кезінде тұнбаның ерігіштігін арттыратын зат қосу керек
Комплексонометриялық титрлеу әдісінде реакцияның ерекшелігі
A) металл иондары қатысады
B) арнайы комплекс түзуші органикалық реактивтер қатысады
C) ішкі комплексті қосылыстар түзіледі
Комплексондар – полиаминополикарбон қышқылдарының түрлері:
A) бутанди қышқылының натрий тұзы
C) нитрилтрисірке қышқылы

F) этилендиаминтетрасірке қышқылы

G) трилон Б

Комплексонометриялық титрлеуде жиі қолданылатын комплексон ІІІ ерекшеліктері
B) суда ерігіштігі
C) жоғары тұрақтылығы
D) металл комплекстерін жеңіл түзуі
Комплексонометриялық титрлеу қисығын тұрғызу үшін есептейтін формулалар:
B) 
C) 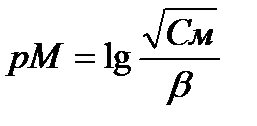
F) 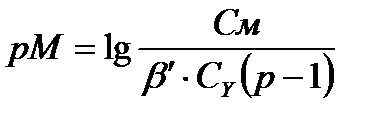
Комплексонометриялық титрлеуде қолданылатын индикаторлардың жіктелуі:
A) азоқосылыстар тобының индикаторы
C) трифенилметан инидкаторлар
H) әртүрлі құрылымды индикаторлар
Комплексонометриялық титрлеуде әртүрлі құрылымды индикаторлардың түрлері:
D) мурексид
G) кальцион
H) метилтимол көк
Көрінетін аймақта ерітінділердің жарықты сіңіруін сипаттайтын параметрлері
D) ерітіндінің түсі
E) ерітіндінің жарықты сіңіретін толқын ұзындығы
H) ерітіндінің жарықты сіңіру мөлшері
Кондуктометрияда ерітіндінің анықталатын параметрлері:
B) электрөткізгіштік
D) меншікті электрөткізгіштік
F) эквивалентті электрөткізгіштік
Кондуктометрияда ерітіндінің анықталатын параметрлердің теңдеулері
A) 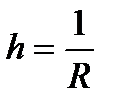
E) 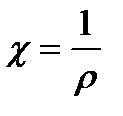
G) 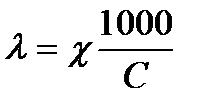
Кондуктометриялық әдісте сұйылтылған ерітінділердің электр өткізгіштігі тәуелді:
F) ерітіндідегі иондардың санына
G) элементарлы зарядтың санына
H) бірдей зарядталған иондардың қозғалу жылдамдығына
Кондуктометриялық титрлеу әдісінің артықшылықтары
C) лайлы және боялған ерітінділерді индикаторлық анықтауға болады
G)сезімталдығы жоғары, сұйытылған ерітінді анализдеуге болады
H) қоспа заттарда анализдеуге болады
Кулонометриялық әдіс сипатталады:
F) жоғары селективтілігімен
G) алдын ала градуйровканы қажет етпейтіндігімен
H) төмен селективтілігімен
Кондуктометриялық титрлеуде қолданылатын титрометриялық анализ түрлері:
A) қышқылдық негіздік титрлеу
D) тұнбалық титрлеу
G)комплексонометриялық титрлеу
Кулонометриялық титрлеуде электролиз заңына сәйкес электр мөлшерін есептейтін  ; мұндағы
; мұндағы
A) І – тоқ күші, А
B) t – уақыт, С
C) n – электрон саны
Кулонометриялық титрлеу қисықтарының түрлері
D, Е, G
Классикалық полярографияда диффузиялық токтың (I) концентрацияға тәуелділігі Ильякович теңдеуімен өрнектеледі: I=KC; K=607nDmt, мұндағы
A) n – реакцияға қатысатын электрон саны
D) D – заттың диффузия коэффициенті
F) m – капиллярдан аққан сынаптың мөлшері
Кулонометриялық титрлеу жүргізетін қарапайым құрылғыдағы нөмірленген бөліктер
B) 1 – электролиттік ұяшық
D) 2 – тұрақты ток көзі
E) 3 – реостат
Кулонометриялық титрлеудің ерекшелігі
C) титрлеу электролиттік ұяшықта өтеді
F) ұяшыққа қосымша зат қосылады
G)титрант ұяшықта генерацияланады
Классикалық полярогфиялық анализ жүргізілетін арнайы құрылғы – поляграфтың негізгі бөліктері:
| V |
| A |
B) батарея мен реостат
C) вольтметр мен микроамперметр
ҚҚҚҚ
Қабат қалыңдығы 1 см ерітінді арқылы өткенде жарықтың қарқындылығы 10% әлсірейді, егер қабат қалыңдығы 10 см ерітіндіден жарық өтсе, онда оның сіңірілу коэффициентінің (k), оптикалық тығыздығының (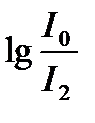 ) және жарық қарқындылығының (I2) мәндері
) және жарық қарқындылығының (I2) мәндері
D) 
E) 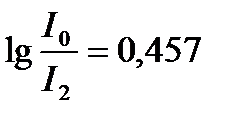
F) 
Қабат қалыңдығы 5 см түсті ерітіндіден өткен жарық ағының бастапқы қарқындылығы 5 есеге азайды. Түсті ерітіндінің оптикалық тығыздығының, сіңіру коэффициентінің формулары, сіңіру коэффициентінің мәні.
A) 
B) 
C) 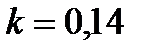
Қайтымды редокс – индикатордың қатары:
B) дифениламин
C) метилен көк
D) ферроин
Қатты және сусымалы материалдардан сынама алуға қойылатын талаптар:
B) сынаманы қаптаманың әр жерінен алу керек
D) материалдың сыртқы тұздары қамтылу керек
G) материалдың ішкі тұздары қамтылу керек
Қатты дене – сұйықтық жүйесінде экстракция жүргізгенде қатты фазаның сипаты мен күйі есепке алынып, экстракциялауға дайындалатын материалдардың түрлері:
D) тегіс (кен, балқыма) немесе кеуекті (кепкен өсімдік пен жануар шикізаты)
F) монолитті (балқыма кесектері) немесе сусымалы (ұнтақталған материалдар)
H) ылғалданған немесе кепкен
Қатты материалдарды экстракцияға алдын ала дайындау жолдары:
A) кептіру
D) минимальді дәрежеде ұнтақтау
G) орташа сынаманы жинау
Қатты денеге немесе сұйықтыққа газ тәрізді немесе еріген заттардың сіңуіне, сондай-ақ химиялық қосылыстың түзілуіне байланысты сорбцияның жіктелуі:
D) адсорбция
E) абсорбция
F) хемосорбция
Қоспа заттарының фазаларға бөліну механизмі бойынша хроматографиялық анализ әдісінің жіктелуі:
C) таралмалы хроматография
D) адсорбциялық хроматография
G) ион алмасу хроматография
Қышқылдармен (НСІ, Н2SO4) және негіздермен (NН3 ерітіндісі) өзара әрекеттескен кезде тұнбаға түсетін катиондардың аналитикалық топтарының түрлері:
C) сульфатты топтар
D) хлоридті топтар
G) гидроксилді топтар
Қышқылдық-негіздік титрлеу әдісінде қолданылатын титранттар:
A) 0,05-0,1М НСІ және Н2SO4
B) 0,05-0,1М КОН және NaOH
E) 0,05-0,1М Ba(ОН)2
Қышқылдық-негіздік индикаторлар ретінде кеңінен қолданылатын трифенилметан индикаторларының қатары:
C) фенолфталеин
F) кристалл күлгін
G) тимолфталеин
Қышқылдық-негіздік титрлеу әдісінде индикатордың түс өзгертуіне байланысты сипатталатын терминдер:
A) индикатордың түс өзгерту интервалы
B) титрлеу көрсеткіші
C) титрлеу секірісі
Қышқылдық-негіздік титрлеу әдісінде эквиваленттік нүктені химиялық көрсеткіштер арқылы анықтайтын физико-химиялық әдістер:
A) ортаның рН өзгерісі бойынша потенциометриялық әдіс
E) ерітіндінің электр өткізгіштігі бойынша кондуктометриялық әдіс
G) ерітіндінің оптикалық қасиеттері бойынша фотометриялық әдіс
Қышқылдық-негіздік титрлеу әдісінде рН-тың бірден өзгеру аймағына әсер ететін факторлар:
B) титрлеу кезінде өтетін реакцияның тепе-теңдік константасы
E) әрекеттесетін реагенттердің концентрациялары
F) температура
Қышқылдық-негіздік титрлеу әдісінде индикаторлық қателікті туғызатын факторлар:
A) электролит концентрациясының өзгерісі
F) ауадағы СО2 әсер етуі
H) температураның индикатордың рКHІnd әсер етуі
Қышқылдық-негіздік титрлеу әдісінде күшті қышқылды күшті негізбен титрлегенде титрлеу қисығындағы HCl ерітіндісі мен NaOH ерітіндісінің қысқаша анализі:
C) Бейтарап сызығында жатқан эквивалент нүктесі, рH= 7 болады
D) Қышқылды сілтімен титрлегенде титрлеу секірмесі рT= 4 басталады
G) рН секірмесінде үлкен интервал (4-10) болады
Қышқылдық-негіздік титрлеуде біріншілік стандартты заттар қатары:
A) натрий карбонаты
B) натрий тетрабораты
E) натрий оксалаты
Қышқылдық-негіздік титрлеуде біріншілік стандартты заттар қатары:
E) калий бифталаты
G) бензой қышқылы
H) қымыздық қышқылы
Қышқылдық-негіздік титрлеуде біріншілік стандартты заттар Na2CO3, Na2B4O7ּ10H2O, Na2C2O4 қосылыстарының эквиваленті:
C) fэ(Na2CO3) = 1/2 моль
F) fэ(Na2B4O7ּ10H2O) = 1/2 моль
G) fэ(Na2C2O4) = 1/2 моль
Қышқылдық-негіздік титрлеуде біріншілік стандартты заттар С6H5COOH, H2C2O4ּ2H2O қосылыстарының эквиваленті:
A) fэ(H2C2O4ּ2H2O) = 1/3 моль
D) fэ(С6H5COOH) = 1 моль
E) fэ(KHC8H4O4) = 1 моль
F) fэ(H2C2O4ּ2H2O) = 1/2 моль
Люминесценцияның энергетикалық және кванттық шығымдарын есептейтін формулалар:
A) 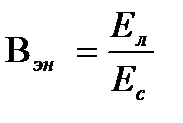
B) 
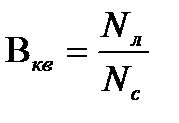
C) 
Лиганданың табиғатына байланысты комплексті қосылыстардың жіктелуі:
A) амиакатты комплекстер
B) аква комплекстер
C) ацидокомплекстер
Люминесценция әдісінде толқындық сипаттамаларға жататын параметрлер:
A) тербеліс жиілігі
C) толқын ұзындығы
E) толқындық сан
Массасы 0,5236г тең ВаCl2.2H2O өлшемесінен ВаSO4 тұнбаға түсіру үшін қажетті Н2SO4 10% ерітіндісінің – тұнбаға түсірушінің көлемінің, тұнбаның молярлық массасының мәндері және тұнбаға түсу реакция теңдеуі:
A) 
C) Н2SO4 + BaSO4 → BaSO4 + 2HCl
F) M(BaSO4)=233,4 г/моль
Массасы 0,3289г Са(NO3)2 . 6Н2О өлшемеден калдьцийді тұнбаға түсіру үшін қалыпты және 50% артық мөлшерде 0,5 н. Н2С2О4 . 2Н2О ерітіндісінің қажетті көлемі және тұнбаға түсу реакция теңдеуі:
B) Са(NO3)2 . 6Н2О + Н2С2О4 . 2Н2О → СаС2О4 + 2НNO3 + 8Н2О
C) қалыпты жағдайда 
E) 50% артық 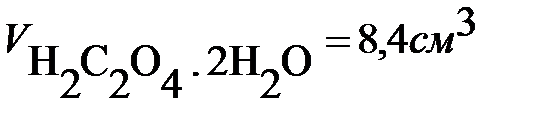
Массасы 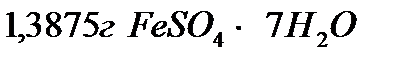 суда ерітіп, көлемін 100 см3 дейін супен жеткізіп, оның 25,00 см3 ерітіндісін K2Cr2O7 ерітіндісімен титрлейді. Титрлеуге 17,25 см3 0,05н K2Cr2O7 жұмсалды. Тотықтырғыш пен тотықсыздандырғыштың жартылай тотығу – тотықсыздану реакция теңдеулері және
суда ерітіп, көлемін 100 см3 дейін супен жеткізіп, оның 25,00 см3 ерітіндісін K2Cr2O7 ерітіндісімен титрлейді. Титрлеуге 17,25 см3 0,05н K2Cr2O7 жұмсалды. Тотықтырғыш пен тотықсыздандырғыштың жартылай тотығу – тотықсыздану реакция теңдеулері және  өлшемдегі (%) мөлшері:
өлшемдегі (%) мөлшері:
D) 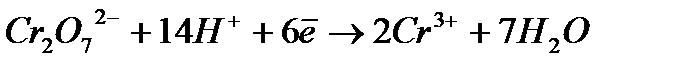
E) 
F) 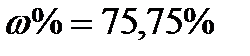
Массасы 0,1120г х.т. K2Cr2O7 қышқыл ортада KI ерітіндісімен өңделіп натрий тиосульфатымен титрленеді титрлеуге 20,12 см3 натрий тиосульфаты жұмсалды. Натрий тиосульфаты ерітіндісінің нормальдігі, титрі және түзету коэффициенті
F) 
G) 
H) 
Мартин мен Синджаның теоретикалық табақшалар теориясы бойынша хроматографиялық колонкада ойша бөлінген әрбір табақшада болжанады
D) сорбент пен жылжымалы фаза арасында өте тез тепе-теңдік орнайды
E) жаңа порциясы тепе-теңдікті ығыстырып, хроматографияланатын заттың жартысы келесі табақшаға ауысады
F) хроматографияланатын зат бірнеше табақшаларға таралып, ортадағы табақшаларда көрші табақшаға қарағанда оның концентрациясы максимальді мәнге ие болады
Мартин мен Синджаның теоретикалық табақшалар теориясы бойынша хроматографиялық колонкадағы сорбент қабатының бойына заттың таралуын, теоретикалық табақшалардың санын, теоретикалық табақшалардың биіктігін есептейтін теңдеулер қатары:
F) 
G) 
H) 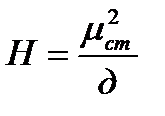
Марганец (ІІ) – ионына қышқыл ортада аммоний пероксидсульфатымен және сутегінің асқын тотығымен әсер етсе, сондай-ақ азот қышқылының қатысымен қорғасын диоксидімен әсер етсе, таңқурай түске ие болады. Марганец (ІІ) – ионына сілтілік металдардың гидроксидімен әсер еткен кезде түзілген ақ тұнба ауадағы оттектің әсерінен қоңыр түске айналады. Осы анықтауларды дәлелдейтін реакция теңдеулері:
A) 2MnSO4 + 5(NH4)2S2O8 + 7H2O → 2НMnO4 + 5(NH4)2SO4+ 7Н2SO4
B) 2MnSO4 + 5PbO2 + 6HNO3 → 2НMnO4 + 2PbSO4+ 3Pb(NO3)2 + 2H2O
H) 2Mn(OH)2+ O2+ 2H2O → 2Mn(OH)4(қ)→ 5MnO(OH)2+ H2O
Магний тұзының ерітіндісі NH4CI мен аммиактың қатысында натрий гидрофосфатымен ақ кристалды тұнба түзеді, тұнба күшті қышқылдарда және сірке қышқылында ериді. Осы анықтауларды дәлелдейтін реакция теңдеулері:
B) Mg2++ НPO42- + NH3 → MgNH4PO4(қ)
C) MgNH4PO4(қ)+ 3Н+→ Mg2++ NH4+ + Н3PO4
D) 2MgNH4PO4 + 4CH3COOH → Mg(H2PO4)2 + 2CH3COONH4+ Mg(CH3COO)2
Мессбауэр эффектісімен атомдардың ядросында байқалатын құбылыстар:
C) γ-квант сәулесінің шығарылуы
E) γ-квант сәулесінің жұтылуы
G) γ-квант сәулесінің шашырауы
Молекулалық адсорбциялық әдісінің оптикалық спектр аймағына, жарық сәулесі жолағының енін өлшеуге байланысты жіктелуі
B) колориметрия
C) фотоколориметрия
F) спетрофотометрия
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 603; Нарушение авторских прав?; Мы поможем в написании вашей работы!