
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Восстановительные процессы в воспаленной ткани
|
|
|
|
Выход лейкоцитов в воспаленную ткань (эмиграция лейкоцитов)
Эмиграция (emigratio, от лат. emigrare - выселяться, переселяться) - выход лейкоцитов из сосудов в ткань. Осуществляется путем диапедеза главным образом через стенку венул. Эмиграция лейкоцитов в очаг является ключевым событием патогенеза воспаления. Лейкоциты служат основными эффекторами воспаления. Внеклеточные бактерицидный и литический эффекты лейкоцитарных продуктов и фагоцитоз играют решающую роль в борьбе с флогогеном. Одновременно, оказывая влияние на клетки, сосуды и кровь, компоненты лейкоцитов выступают как важные медиаторы и модуляторы воспаления, в том числе повреждения собственных тканей. Осуществляя раневое очищение, фагоциты создают предпосылки для репаративных явлений, где они стимулируют пролиферацию, дифференцировку и функциональную активность фибробластов и других клеток. Механизм эмиграции (по И.И. Мечникову) состоит в явлении хемотаксиса.
Пусковым моментом активации лейкоцитов является воздействие на рецепторы (часто специфические) клеточных мембран разнообразных хемотаксических агентов (хематтрактантов), высвобождаемых микроорганизмами или фагоцитами, а также образующихся в ткани в результате действия воспалительного агента или под влиянием самих фагоцитов. Наиболее важными хематтрактантами являются: фрагменты комплемента, фибринопептиды и продукты деградации фибрина, калликреин, проактиватор плазминогена, фрагменты коллагена, фибронектин, метаболиты арахидоновой кислоты, цитокины, лимфокины, бактериальные пептиды, продукты распада гранулоцитов.
В результате связывания хематтрактантов с рецепторами и активации ферментов плазматической мембраны в фагоците развивается респираторный взрыв - резкое повышение потребле-
ния кислорода и образование активных его метаболитов. Этот процесс не имеет отношения к обеспечению фагоцита энергией. Он направлен на дополнительное вооружение фагоцита высокореактивными токсическими веществами для более эффективного уничтожения микроорганизмов. Наряду с дыхательным взрывом в фагоците происходят другие изменения: повышенная выработка особых мембранных гликопротеинов, определяющих адгезивность фагоцита; понижение поверхностного натяжения мембраны и изменение коллоидного состояния участков цитоплазмы (обратимый переход из геля в золь), что необходимо для образования псевдоподий; активация актиновых и миозиновых микрофиламентов, являющаяся основой миграции; усиленная секреция и выделение веществ, облегчающих прикрепление лейкоцита к эндотелию (лактоферрин, катионные белки, фибронектин, интерлейкины).
Лейкоциты выходят из осевого тока крови в плазматический. Этому способствуют нарушение реологических свойств крови, замедление кровотока, изменение его характера, в частности уменьшение краевой плазматической зоны (рис. 10-12).
Вследствие возрастания адгезивных свойств лейкоцитов и эндотелиальных клеток происходит приклеивание лейкоцитов к
 Рис. 10-12. Схема кровотока в норме и при воспалении: 1 - нормальная циркуляция: осевой ток, краевая плазматическая зона с отдельными лейкоцитами; 2 - замедление кровотока: видны эритроциты, краевое стояние лейкоцитов и тромбоцитов; 3 - сильный застой крови: краевое стояние лейкоцитов и тромбоцитов, уменьшение краевой плазматической зоны (по Д.Е. Альперну)
Рис. 10-12. Схема кровотока в норме и при воспалении: 1 - нормальная циркуляция: осевой ток, краевая плазматическая зона с отдельными лейкоцитами; 2 - замедление кровотока: видны эритроциты, краевое стояние лейкоцитов и тромбоцитов; 3 - сильный застой крови: краевое стояние лейкоцитов и тромбоцитов, уменьшение краевой плазматической зоны (по Д.Е. Альперну)
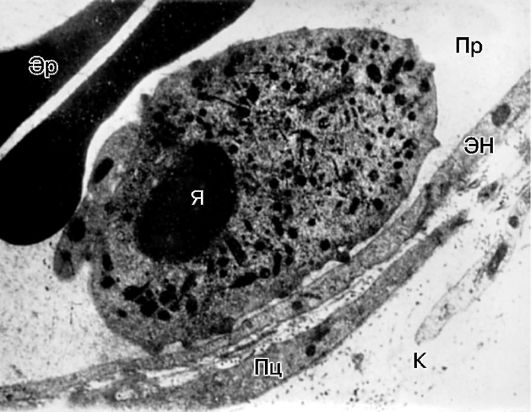 Рис. 10-13. Краевое стояние лейкоцита в венуле брыжейки крысы при воспалении: Пр - просвет сосуда; ЭН - эндотелиальная клетка; Пц - перицит; К - коллагеновые волокна; Я - ядро; Эр - эритроциты. Электронная микроскопия, х10 000 (по А.М. Чернуху)
Рис. 10-13. Краевое стояние лейкоцита в венуле брыжейки крысы при воспалении: Пр - просвет сосуда; ЭН - эндотелиальная клетка; Пц - перицит; К - коллагеновые волокна; Я - ядро; Эр - эритроциты. Электронная микроскопия, х10 000 (по А.М. Чернуху)
эндотелию - развивается феномен краевого стояния лейкоцитов
(рис. 10-13).
Повышение адгезивности эндотелия может быть обусловлено: усиленной продукцией им адгезивных гликопротеинов (лектинов) и других веществ, которые включаются в состав фибриновой пленки, в норме покрывающей эндотелий со стороны просвета сосуда, фиксацией на эндотелиальных клетках хематтрактантов, впоследствии взаимодействующих со специфическими рецепторами на лейкоцитах, усилением экспрессии на эндотелиоцитах рецепторов к иммуноглобулину G и фрагменту комплемента С3Ь, что способствует фиксации иммунных комплексов, а через них - лейкоцитов, несущих рецепторы к иммуноглобулину (Ig) G и С3Ь.
Прилипание лейкоцитов к эндотелию опосредовано следующими факторами:
• лейкоциты в фазе инициации воспаления активируются и образуют агрегаты; в результате активации лейкоцита его отрицательный заряд снижается, что уменьшает силы взаимного отталкивания между ним и отрицательно заряженным эндотелием;
• между лейкоцитами и эндотелием образуются кальциевые мостики (Са2+ и другие двухвалентные ионы играют ключевую роль в прилипании лейкоцитов);
• в ходе активации в лейкоцитах усиливается синтез специфических гранул, некоторые компоненты которых, например лактоферрин, усиливают адгезивные свойства клеток;
• на мембране лейкоцитов возрастает экспрессия адгезивных гликопротеинов классов Мас-1 и LAF-1.
Первоначальный контакт лейкоцитов с эндотелием является весьма непрочным, и под влиянием кровотока они могут перекатываться по поверхности фибриновой пленки, однако контакт быстро стабилизируется, поскольку лейкоциты выделяют в зону слипания протеазы, обнажающие лектиноподобные участки мембраны эндотелиоцитов и придающие им повышенную адгезивность. Прямое отношение к прилипанию фагоцитов к эндотелию имеет выделяемый ими фибронектин. Занявшие краевое положение лейкоциты выпускают псевдоподии, которые проникают в межэндотелиальные щели и таким образом «переливаются» через эндотелиальный слой (рис. 10-14). Эмиграции способствуют повышение сосудистой проницаемости и усиление тока жидкости из сосуда в ткань, существенно облегчающие прохождение сосудистой стенки для лейкоцита.
Оказавшись между эндотелиальным слоем и базальной мембраной, лейкоцит выделяет лизосомальные протеиназы, растворяющие ее, а также катионные белки, изменяющие коллоидное состояние базальной мембраны (обратимый переход из геля в золь), что обеспечивает повышенную проходимость ее для лейкоцита. Иммигрировавшие лейкоциты отделяются от наружной поверхности сосудистой стенки и амебоидными движениями направляются к центру очага воспаления (рис. 10-15), что определяется градиентом концентрации хемотаксических веществ в очаге. Некоторую роль могут играть электрокинетические явления, обусловленные разностью потенциалов между отрицательно заряженным лейкоцитом и положительным зарядом ткани, характеризующейся Н+- гиперионией.
Первоначально среди лейкоцитов экссудата в очаге острого воспаления преобладают гранулоциты, в основном нейтрофилы, а затем - моноциты/макрофаги. Позже в очаге накапливаются лимфоциты.
Поскольку замедление кровотока в отдельных разветвлениях микроциркуляторного русла и краевое стояние лейкоцитов могут
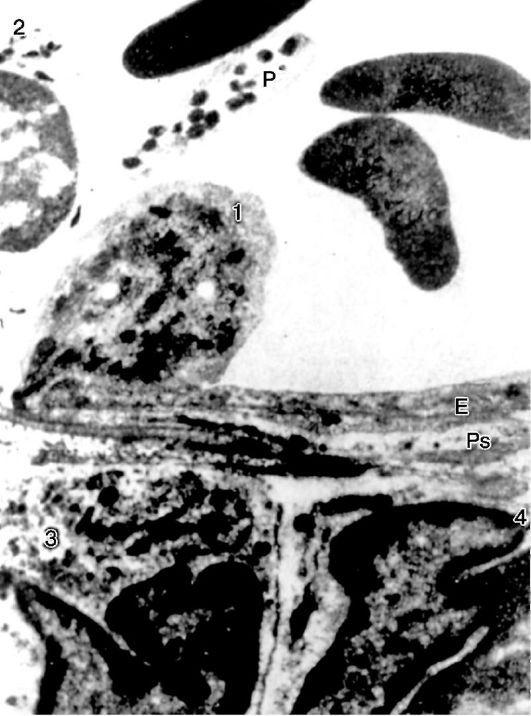 Рис. 10-14. Эмиграция нейтрофила: 1 - эмигрирующий нейтрофил; Е - эндотелиальная клетка; Ps - длинный псевдоподий, расположенный параллельно эндотелию; 2 - нейтрофил в просвете сосуда; 3, 4 - эмигрировавшие нейтрофилы; Р - тромбоцит. х15 500 (по Марчези)
Рис. 10-14. Эмиграция нейтрофила: 1 - эмигрирующий нейтрофил; Е - эндотелиальная клетка; Ps - длинный псевдоподий, расположенный параллельно эндотелию; 2 - нейтрофил в просвете сосуда; 3, 4 - эмигрировавшие нейтрофилы; Р - тромбоцит. х15 500 (по Марчези)
 Рис. 10-15. Схема эмиграции лейкоцитов (по Марчези)
Рис. 10-15. Схема эмиграции лейкоцитов (по Марчези)
развиваться весьма быстро, а мигрирующему нейтрофилу достаточно 3-12 мин, чтобы пройти эндотелий, появление гранулоцитов в очаге может наблюдаться уже к 10-й мин от начала воспаления. Скорость аккумуляции нейтрофилов в очаге является наивысшей в первые 2 ч, постепенно снижаясь в последующие. Количество их достигает максимума через 4-6 ч. В этот период лейкоциты очага представлены нейтрофилами более чем на 90%. Гранулоциты фагоцитируют бактерии или иные инородные тела и частицы отмирающих клеточных элементов, параллельно осуществляя внеклеточную поставку ферментов, катионных белков, активных метаболитов кислорода. Одновременно происходит массивное разрушение нейтрофилов, останки которых являются важным стимулом расширения инфильтрации - как нейтрофильной, так и моноцитарной. Как и в норме, большинство гранулоцитов, вышедших в ткань, никогда не возвращается в кровоток.
Моноциты обычно преобладают в очаге острого воспаления спустя 16-24 ч и достигают пика, как правило, на третьи сутки. Однако миграция моноцитов из крови в ткань начинается одновременно с миграцией нейтрофилов. Предполагается, что вначале меньшая, чем у нейтрофилов, скорость аккумуляции моноцитов связана с торможением хемотаксиса этих клеток под влиянием продуктов жизнедеятельности нейтрофилов в течение определенного времени, необходимого для полной выраженности нейтрофильной реакции и предупреждения ее моноцитарного контроля. В очаге воспаления наблюдаются постепенное превращение иммигрировавших моноцитов в макрофаги и созревание последних, в процессе которого объем цитоплазмы и органелл в ней увеличивается. В частности, повышается количество митохондрий и лизосом, что имеет существенное значение для полноценного выполнения макрофагами их функций в очаге. Возрастает активность пиноцитоза, в цитоплазме увеличивается количество фаголизосом, повышается число филоподий. Моноциты/макрофаги также являются источником медиаторов воспаления (ферментов, метаболитов кислорода, цитокинов), фагоцитируют бактерии, но имеют преимущественное значение в фагоцитозе останков погибших клеток, в частности нейтрофилов. Поэтому понятна зависимость аккумуляции моноцитов от предыдущего выхода нейтрофилов. Так, у кроликов с нейтропенией моноциты не появляются в очаге воспаления в течение 16 ч, в то время как в естественных условиях воспаления они обнаруживаются уже через 4 ч, а введение в очаг
воспаления лейкопеническим животным нейтрофилов восстанавливает обычную аккумуляцию мононуклеаров. Известно хемотаксическое действие лизатов нейтрофилов на моноциты, обусловленное отчасти катионными белками их лизосомальных гранул.
С другой стороны, аккумуляция нейтрофилов во многом зависит от моноцитов. Особенно это касается той части нейтрофильной инфильтрации, которая связана с усиленным кроветворением, поскольку последнее инициируется моноцитарно-макрофагальными гемопоэтическими факторами, в частности IL-1, различными типами так называемых колониестимулирующих факторов - веществ преимущественно белковой природы, ответственных за пролиферацию и дифференцировку в костном мозгу кроветворных клеток. В настоящее время выделен ряд хемотаксических пептидов из моноцитов человека для нейтрофилов, которым может принадлежать роль в механизме саморегуляции лейкоцитарной реакции очага воспаления. Однако вопрос о механизмах смены клеточных фаз в очаге воспаления, перехода от развертывания воспалительной реакции к ее разрешению относится к наименее изученным в проблеме воспаления.
Клеточный состав экссудата в большой мере зависит от характера и течения воспалительного процесса, в свою очередь определяемых воспалительным агентом и состоянием реактивности организма. Так, экссудат особенно богат нейтрофилами, если воспаление вызвано гноеродными микробами; при аллергическом воспалении в очаге содержится много эозинофилов. Хронические воспалительные процессы характеризуются незначительным содержанием нейтрофилов, преобладанием моноцитов и лимфоцитов.
Иммигрировавшие лейкоциты совместно с пролиферирующими клетками местного происхождения образуют воспалительный инфильтрат. При этом экссудат с содержащимися в нем клетками пропитывает ткань, распределяясь между элементами воспалительного участка и делая его напряженным и плотным. Инфильтрат наряду с экссудатом обусловливает припухлость и имеет значение в возникновении воспалительной боли.
Под воспалительной пролиферацией (proliferat e, от лат. proles - потомство, ferre - создавать) понимают размножение местных кле-
точных элементов в очаге воспаления. Пролиферация развивается с самого начала воспаления наряду с явлениями альтерации и экссудации, но становится преобладающей в более поздний период процесса, по мере стихания экссудативно-инфильтративных явлений. Первоначально она в большей мере выражена на периферии очага. Важнейшим условием прогрессирования пролиферации является эффективность очищения очага воспаления от микроорганизмов или другого вредного агента, продуктов альтерации тканей, погибших лейкоцитов (раневое очищение). Ведущая роль в этом отводится макрофагам - гематогенного (моноциты) и тканевого (гистиоциты) происхождения.
Раневое очищение происходит главным образом путем внеклеточной деградации поврежденной ткани и фагоцитоза. Оно осуществляется под регуляторным влиянием цитокинов с помощью таких ферментов, как протеогликаназа, коллагеназа, желатиназа. Активация этих ферментов может происходить под воздействием активатора плазминогена, высвобождаемого при участии цитокинов из мезенхимальных клеток. Простагландины, высвобождаясь вместе с ферментами, могут, со своей стороны, индуцировать протеиназы и вносить свой вклад в процессы деградации.
Фагоцитоз был открыт и понят как важнейший элемент воспаления и естественного иммунитета И.И. Мечниковым в 1882 г.
И.И. Мечников выделил 4 фазы фагоцитоза:
1) фаза приближения: выход лейкоцита из сосуда и приближение к объекту фагоцитоза под действием хематтрактантов;
2) фаза прилипания (контактная);
3) фаза погружения: обволакивание и погружение объекта внутрь фагоцита; образуется особая вакуоль, где скапливаются лизосомы;
4) фаза переваривания, результатом которой могут быть 2 варианта исхода: а) адекватное дозированное освобождение лизосомальных ферментов, разрушающее только флогоген (сам фагоцит остается интактным); б) чрезмерное выделение лизосомальных ферментов, что ведет к разрушению объекта фагоцитоза и самого фагоцита.
Фагоциты, взаимодействуя с бактериями, активируются, их мембрана становится «липкой», так как количество различных рецепторов на ней резко увеличивается, как увеличивается и «ощупывающая» подвижность цитоплазмы этих клеток. Одновременно в цитоплазме накапливаются пероксисомы и гранулы, наполнен-
ные мощными протеазами. Когда такая клетка встречается с микроорганизмом, бактерия «прилипает» к поверхности фагоцита, обволакивается его псевдоподиями и оказывается внутри клетки, где и разрушается. Макрофаги начинают выделять в среду фактор некроза опухолей (TNF), интерферон γ (IFN-γ) и IL-8, который играет в воспалении особую роль - он вызывает появление в эндотелиоцитах рецепторов, реагирующих с моноцитами и нейтрофилами с высоким сродством, так что эти клетки останавливаются в капиллярах, расположенных в районе воспаления. IL-8 наиболее эффективен в создании градиента для хемотаксиса фагоцитирующих клеток. Фагоциты имеют рецепторы к IL-8, которые «чувствуют» разницу в его концентрации со стороны, обращенной к его источнику, и с противоположной стороны, и направляют свое движение по оси максимального отличия. Таким образом, фагоцитирующие клетки накапливаются в очаге воспаления, активно поглощают и разрушают (внутриклеточно) бактерии и обломки клеток и выделяют ферменты, разрушающие межклеточное вещество соединительной ткани. При нагноении кожный покров, окружающий очаг воспаления (нарыв), истончается и прорывается: флогогены, обломки клеток и накопившиеся фагоциты выбрасываются из организма. Пораженный участок ткани постепенно восстанавливается. Удаляя останки лейкоцитов и разрушенных тканей, макрофаги устраняют важнейший источник собственной хемотаксической стимуляции и подавляют дальнейшее развитие местной лейкоцитарной реакции. По мере очищения очага воспаления количество макрофагов убывает из-за снижения их поступления из крови. Из очага они уносятся восстанавливающимся током лимфы в регионарные лимфоузлы, где погибают. Лимфоциты частью погибают, частью превращаются в плазматические клетки, продуцирующие антитела, и затем постепенно элиминируются.
Пролиферация осуществляется главным образом за счет мезенхимальных элементов стромы, а также элементов паренхимы органов. В ней участвуют камбиальные, адвентициальные, эндотелиальные клетки. В результате дифференцировки стволовых клеток соединительной ткани - полибластов - в очаге появляются эпителиоидные клетки, фибробласты и фиброциты. Основными клеточными элементами, ответственными за репаративные процессы в очаге воспаления, являются фибробласты. Они продуцируют основное межклеточное вещество - гликозаминогликаны, а также синтезируют и секретируют волокнистые структуры - коллаген,
эластин, ретикулин. В свою очередь, коллаген является главным компонентом рубцовой ткани.
Регуляция пролиферации. Процесс пролиферации находится под сложным гуморальным контролем. Решающее значение здесь имеют опять-таки макрофаги. Они являются основным источником фактора роста фибробластов - термолабильного белка, стимулирующего пролиферацию фибробластов и синтез коллагена. Макрофаги также усиливают привлечение фибробластов в очаг воспаления, секретируя IL-1 и фибронектин. Макрофаги стимулируют пролиферацию эндотелиальных и гладкомышечных клеток сосудистой стенки, базальной мембраны и, таким образом, образование микрососудов. Угнетение или стимуляция системы мононуклеарных фагоцитов соответственно ослабляет или усиливает развитие грануляционной ткани в очаге гнойного воспаления.
В свою очередь, макрофаги опосредуют регуляторное влияние на фибробласты и пролиферацию Т-лимфоцитов. Последние же активируются протеиназами, образующимися в очаге воспаления в результате распада ткани. Протеиназы могут оказывать непосредственное влияние как на макрофаги, так и на фибробласты. Макрофаги и лимфоциты могут высвобождать моно- и лимфокины, не только стимулирующие, но и угнетающие фибробласты, выступая в качестве истинных регуляторов их функций.
Фибробласты зависят также от тромбоцитарного фактора роста, являющегося термостабильным белком с высоким содержанием цистеина и молекулярной массой 30 000Д. В качестве других факторов роста для фибробластов называют соматотропин, соматомедины, инсулиноподобные пептиды, инсулин, глюкагон.
Важную роль в пролиферативных явлениях играют кейлоны - термолабильные гликопротеины с молекулярной массой 40 000Д, способные ингибировать клеточное деление путем инактивации ферментов, участвующих в редупликации ДНК. Одним из основных источников кейлонов являются сегментоядерные нейтрофилы. По мере снижения количества нейтрофилов в очаге воспаления уменьшается содержание кейлонов, что приводит к ускорению деления клеток. По другим предположениям, при воспалении сегментоядерные нейтрофилы практически не вырабатывают кейлоны и усиленно продуцируют антикейлоны (стимуляторы деления); соответственно деление клеток ускоряется, пролиферация усиливается.
Другие клетки и медиаторы могут модулировать репаративный процесс, воздействуя на функции фибробластов, макрофа-
гов и лимфоцитов. Существенное значение в регуляции репаративных явлений, по Д.Н. Маянскому, имеют также реципрокные взаимоотношения в системе коллаген - коллагеназа, стромальнопаренхиматозные взаимодействия.
Пролиферация сменяется регенерацией. Последняя не входит в комплекс собственно воспалительных явлений, однако непременно следует им и трудно от них отделима. Она состоит в разрастании соединительной ткани, новообразовании кровеносных сосудов, в меньшей степени - в размножении специфических элементов ткани. При незначительном повреждении ткани происходит относительно полная ее регенерация. При образовании дефекта он заполняется вначале грануляционной тканью - молодой, богатой сосудами, которая впоследствии замещается соединительной тканью с образованием рубца.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 722; Нарушение авторских прав?; Мы поможем в написании вашей работы!