
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лейкозы
|
|
|
|
Одной из наиболее опасных для жизни человека патологий системы крови являются лейкозы, относящиеся к группе гемобластозов - злокачественных новообразований кроветворной (миелоидной и лимфоидной) ткани. В отличие от лейкоцитозов, лейкемоидных реакций и лейкопений лейкоз является не реактивным состоянием, а болезнью системы крови.
Лейкоз - это опухоль, исходящая из кроветворных клеток костного мозга, в основе развития которой лежит неконтролируемый рост клеток с преобладанием процессов их пролиферации над дифференцировкой и образованием очагов патологического кроветворения в органах и тканях, в норме не участвующих в гемопоэзе. При этом утратившие способность к созреванию лейкозные клетки могут проходить значительно большее, чем нормальные клетки крови, число циклов деления, что и создает огромную клеточную продукцию, характеризующую лейкоз.
Этиология лейкозов до настоящего времени точно не установлена. Об опухолевой природе лейкозов свидетельствует наличие общих закономерностей, объединяющих лейкозы и опухоли: нарушение способности клеток к дифференцировке; морфологическая и метаболическая анаплазия клеток; способность к метастазированию; общие этиологические факторы, способствующие развитию лейкозов и опухолей, и др.
К возможным этиологическим факторам, вызывающим развитие лейкозов, относят ионизирующую радиацию, ряд химических веществ, вирусы. Определенное значение в развитии лейкозов придается генетическим факторам, наследственной и приобретенной иммунной недостаточности, действию бластомогенных метаболитов триптофана и тирозина.
Соответственно существует несколько теорий происхождения лейкозов.
Радиационная теория. Роль ионизирующих излучений в возникновении лейкозов доказана в эксперименте. Как однократное (в дозе 2 Гр и выше), так и хроническое (в течение 2-3 месяцев) облучение лучами Рентгена в малых дозах может индуцировать лейкоз у лабораторных животных (крысы, мыши). Прослежено повышение заболеваемости острым и хроническим миелолейкозом у жителей Хиросимы и Нагасаки, у рентгенологов и радиологов. Приводятся данные об увеличении частоты лейкозов у больных, леченных
большими дозами лучей Рентгена, иттрия, радия по поводу злокачественных новообразований и анкилозирующего спондилоартрита, а также у детей, получавших облучение вилочковой железы в раннем возрасте, и др. Описано учащение случаев острых лейкозов среди больных эритремией после лечения их радиоактивным фосфором.
Теория химического лейкозогенеза. Экспериментально доказана возможность индуцирования лейкозов у животных введением канцерогенных веществ (диметилбензантрацен, метилхолантрен и др.). Также в эксперименте показана возможность стимуляции лейкозогенеза метаболитами триптофана и тирозина (М.Л. Раушенбах). Однако роль этих веществ в лейкозогенезе человека не доказана. В то же время накоплены данные, указывающие на увеличение риска заболевания лейкозами (как правило, острыми) у людей, имеющих длительный профессиональный контакт с бензолом и летучими органическими растворителями (шоферы, работники кожевенной и обувной промышленности и т.д.). В последние годы отмечено заметное учащение случаев острого лейкоза у больных злокачественными новообразованиями, леченных такими цитостатическими препаратами, как циклосфосфан, хлорбутин, метотрексат, миелосан, адриамицин и др. К лекарственным препаратам, способным индуцировать лейкозы, относятся также бутадион, левомицетин и некоторые другие.
Вирусная теория связывает возникновение лейкозов с активацией (под действием радиации и химических факторов) латентных лейкозогенных вирусов. Несомненно доказанным является вирусное происхождение лейкозов у многих видов животных - птиц, мышей, крыс, хомячков, кошек, крупного рогатого скота. К настоящему времени выделено и детально охарактеризовано несколько типов вирусов, вызывающих различные виды лейкозов у животных. Как правило, это РНК-содержащие вирусы, а также ДНК-содержащие вирусы, которые относятся к герпесвирусам (подробнее см. раздел 13.3).
Вопрос о роли вирусов в происхождении лейкозов у человека остается во многом спорным. Против вирусной этиологии лейкозов у человека свидетельствует, прежде всего, факт невозможности прямой перевивки лейкозов при случайном переливании крови лиц, больных лейкозом, и отсутствие убедительных доказательств контагиозности лейкозов. Не описаны также случаи передачи лейкоза от больной матери плоду и новорожденному в период вскармливания грудью.
Таблица 14-10. Дифференциальные критерии лекарственных агранулоцитозов
| Критерии | Вид агранулоцитоза | ||
| миелотоксический | иммунный | ||
| Патогенез | Вследствие прямого повреждения клетокпредшественниц гемопоэза | Вследствие иммунного разрушения циркулирующих нейтрофилов | Вследствие иммунного разрушения клетокпредшественниц гранулоцитопоэза |
| Начало | Постепенное | Острое | Постепенное |
| Клинические проявления | Лихорадка, язвеннонекротическое поражение слизистых оболочек ротоглотки и желудочнокишечного тракта, некротическая энтеропатия | Лихорадка, озноб, крапивница, отек Квинке, изъязвление слизистых оболочек ротоглотки, верхних дыхательных путей, желудочно-кишечного тракта, увеличение размеров лимфоузлов, печени и селезенки, грибковые инфекции | |
| Связь с дозой медикамента | Присутствует | Отсутствует | |
| Количество лейкоцитов | Снижение общего количества лейкоцитов, нейтропения до (0,2-0,1)-109/л, моноцитоз, лимфоцитоз, увеличение числа плазматических клеток (только при иммунном агранулоцитозе) | ||
| Количество тромбоцитов | Снижено | В норме | |
| Анемия | Определяется | Не определяется | |
| Картина костного мозга | Тотальное угнетение гемопоэза | Гиперплазия гранулоцитарного ростка | Гипоплазия гранулоцитарного ростка |
| Антилейкоцитарные антитела | Отсутствуют | Присутствуют |
Генетическая теория располагает достаточно убедительными аргументами, указывающими на возможность наследственной предрасположенности к лейкозам. Известны случаи семейных лейкозов, доказана роль этнических особенностей в развитии лимфолейкоза. К возникновению лейкозов предрасполагают болезни, характеризующиеся спонтанными разрывами хромосом и нерасхождением соматических или половых хромосом (болезнь Дауна, анемия Фанкони, синдромы Кляйнфелтера, Тернера и др.). Получены линии мышей, у которых частота спонтанных лейкозов близка к 100%.
Патогенез лейкозов. Согласно мутационно-клоновой теории, в основе происхождения лейкозов лежат мутация и опухолевая трансформация ранних клеток-предшественниц гемопоэза (клеток II и III классов) под влиянием лейкозогенного фактора (ионизирующей радиации, химических веществ, вирусов и др.). В результате происходит выход кроветворных клеток из-под контроля регулирующих систем макроорганизма с активацией их деления на фоне подавления дифференцировки. Формируется клон опухолевых (лейкозных) клеток - потомков одной первоначально мутировавшей клетки (моноклоновая опухоль), которые заселяют (инфильтрируют) костный мозг. В моноклоновой стадии опухолевые клетки чувствительны к химиотерапии. В процессе развития лейкоза (опухолевая прогрессия) происходят качественные изменения составляющих субстрат опухоли клеток, обусловленные нестабильностью их генетического аппарата, что проявляется нарушениями структуры хромосом, анэуплоидией, переходом части ранее неактивных в клетке генов в активное состояние (феномен дерепрессирования генов). Эти изменения ведут к появлению новых клонов опухолевых клеток, среди которых в процессе жизнедеятельности организма, а также под воздействием лечебных средств, применяемых в химиотерапии заболевания, «отбираются» наиболее автономные клоны. В результате моноклоновая опухоль превращается в поликлоновую злокачественную опухоль. На этой стадии развития лейкоза лейкозные клетки становятся устойчивыми к цитостатической терапии, метастазируют в органы и ткани, в норме не участвующие в гемопоэзе, образуя очаги экстрамедуллярного кроветворения (табл. 14-11).
Таблица 14-11. Основные стадии патогенеза лейкозов
| Стадия Характеристика | |
| Инициация | Лейкозогенный фактор (радиация, вирусы и др.) действует на стволовые кроветворные клетки II-III классов, вызывая их опухолевую трансформацию в результате мутационного превращения протоонкогенов в онкогены и инактивации антионкогенов |
| Промоция | Активация и гиперпролиферация лейкозных клеток при действии промотора с формированием клона лейкозных клеток, идентичных по фенотипу и генотипу (моноклоновая стадия) |
| Инфильтрация | «Расселение» лейкозных клеток в костном мозгу с угнетением нормального гемопоэза |
| Прогрессия | Формирование множества клонов лейкозных клеток, различающихся по фенотипу и генотипу (поликлоновая стадия), и естественный отбор наиболее автономных из них, что ведет к «озлокачествлению» заболевания |
| Метастазирование | Образование очагов патологического кроветворения вне костного мозга за счет способности лейкозных клеток к инвазии, интра- и экстравазации, миграции по сосудистой системе, имплантации и пролиферации в различных тканях и органах |
О клоновой природе лейкозов свидетельствуют возможность перевивки лейкоза мышам путем введения одной лейкозной клетки; продукция гомогенного иммуноглобулина при парапротеинемических гемобластозах (миеломная болезнь, макроглобулинемия Вальденстрема и др.); однотипность лейкозных клеток (несущих на поверхности иммуноглобулины одного класса и подкласса) при хроническом лимфолейкозе; наличие специфических хромосомных изменений в опухолевых клетках (транслокации, делеции). Частным подтверждением клонового происхождения лейкозов является обнаружение в 80-90% случаев хронического миелолейкоза аномальной филадельфийской (Ph') хромосомы (рис. 14-12) в миелоидных клетках, включая гранулоцитарный, эритроидный и мегакариоцитарный ростки. Этот факт служит неоспоримым доказательством происхождения хронического миелолейкоза из одного патологического клона, родоначальницей которого является
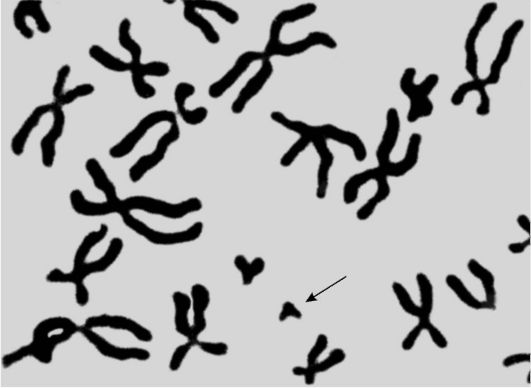 Рис. 14-12. Аномальная Ph'-хромосома в клетке больного хроническим миелолейкозом
Рис. 14-12. Аномальная Ph'-хромосома в клетке больного хроническим миелолейкозом
плюрипотентная стволовая клетка-предшественница миелопоэза (КОЕ-ГЭММ).
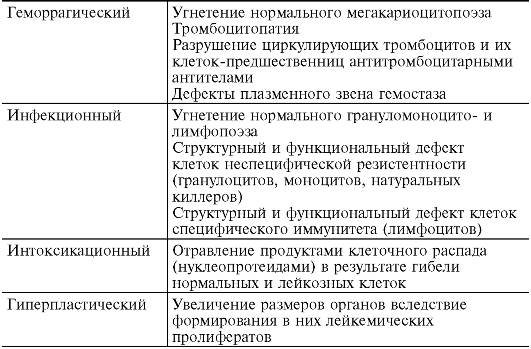
Общие нарушения в организме при лейкозах проявляются следующими клиническими синдромами: анемическим (головокружение, слабость, повышенная утомляемость, одышка и т.д.), геморрагическим (кровотечения из десен, носа, кишечника, кровоизлияния в жизненно важные органы), инфекционным (рецидивирующие инфекции вследствие угнетения фагоцитоза, микробицидной функции лейкоцитов, синтеза антител и т.д.), интоксикационным (тошнота, рвота, снижение аппетита, уменьшение массы тела и т.д.) и гиперпластическим (увеличение размеров и нарушение функции различных органов) (табл. 14-12).
Таблица 14-12. Патогенез основных клинических синдромов лейкозов

 Причинами смерти при лейкозах являются резкое малокровие и тяжелая общая интоксикация, поражение жизненно важных органов (лейкозная инфильтрация, обширные кровоизлияния). Непосредственной причиной смерти больных могут стать инфекционные осложнения (пневмонии, сепсис, перитонит).
Причинами смерти при лейкозах являются резкое малокровие и тяжелая общая интоксикация, поражение жизненно важных органов (лейкозная инфильтрация, обширные кровоизлияния). Непосредственной причиной смерти больных могут стать инфекционные осложнения (пневмонии, сепсис, перитонит).
Классификация лейкозов, особенности кроветворения и клеточного состава периферической крови при различных видах лейкозов
По патогенетическому принципу лейкозы подразделяют на острые и хронические.
Острый лейкоз - это опухоль, исходящая из костного мозга, с полной утратой способности кроветворных клеток к дифференцировке на
уровне клеток IV класса - бластов, составляющих морфологический субстрат опухоли. Гематологическая картина острого лейкоза характеризуется появлением большого числа бластных клеток в крови (до нескольких десятков процентов) и так называемым лейкемическим зиянием (hiatus leukaemicus), проявляющимся наличием бластных и (в небольшом количестве) зрелых клеток в крови при практически полном отсутствии их промежуточных форм.
Хронический лейкоз - опухоль, исходящая из костного мозга, с частичной задержкой способности кроветворных клеток к дифференцировке. При хронических лейкозах клетки сохраняют способность к дифференцировке до стадии созревающих или зрелых клеток, т.е. морфологическим субстратом опухоли являются клетки V и VI классов.
Диагностика лейкозов требует комплексного подхода. Она основывается прежде всего на анализе мазков периферической крови и костного мозга. Для дифференциальной диагностики отдельных форм и цитологических вариантов острых и хронических лейкозов применяют цитохимические, цитологические, иммунологические, цитогенетические и молекулярно-генетические методы.
Острые лейкозы. Острые лейкозы характеризуются высокой скоростью развития опухолевого процесса, что при отсутствии необходимого лечения быстро приводит к гибели больного. Выделяют следующие стадии клинического течения острых лейкозов: первая атака, развернутая стадия, терминальная стадия или выздоровление.
Стадия первой атаки охватывает период времени от проявления первых клинико-гематологических симптомов заболевания, установления диагноза и начала лечения до получения эффекта от проводимой терапии. Критерием лабораторной диагностики острых лейкозов служит наличие в костном мозгу свыше 30% бластных клеток.
В зависимости от содержания бластных клеток в периферической крови острые лейкозы подразделяются на:
• алейкемические - бластные клетки в крови отсутствуют;
• сублейкемические - бластные клетки в крови обнаруживаются в небольшом количестве (3-5%);
• лейкемические - бласты составляют основную массу клеток крови.
Общее количество лейкоцитов (ОКЛ) в периферической крови при острых лейкозах может быть различным:
• при алейкемическом варианте - менее 6-109/л;
• при сублейкемическом варианте - (6-60)-109/л;
• при лейкемическом варианте - более 60-109/л.
Уже на ранних стадиях болезни отмечаются нормохромная анемия и тромбоцитопения, развитие которых обусловлено угнетением нормального гемопоэза вследствие лейкемической трансформации кроветворения.
Развернутая стадия острого лейкоза (стадия развернутых клинических проявлений) характеризуется чередованием ремиссий и рецидивов.
Ремиссия - исчезновение проявлений патологического процесса под влиянием цитостатической терапии. Различают полную и неполную ремиссию.
Полная ремиссия характеризуется нормализацией клинических показателей, картины периферической крови и костного мозга в течение не менее 1 месяца.
Клинико-лабораторные критерии полной ремиссии:
• костно-мозговой - содержание в костном мозгу не более 5% бластных клеток и не более 30% лимфоцитов при нормальной его общей клеточности;
• кровяной - отсутствие бластов в периферической крови, количество гранулоцитов более 1,5-109/л, количество тромбоцитов более 100-109/л, содержание гемоглобина более 100 г/л;
• клинический - исчезновение патологических симптомов;
• субъективный - отсутствие жалоб.
Неполная ремиссия - состояние, при котором нормализуются клинические показатели и гемограмма, но в пунктате костного мозга сохраняются бластные клетки в количестве не более 20%.
Рецидив проявляется возвратом активной стадии заболевания после ремиссии. Рецидив может быть:
костно-мозговым, который подразделяется на:
а) алейкемический - характеризуется обнаружением бластов в костном мозгу (свыше 20%) при отсутствии их в периферической крови;
б) лейкемический - характеризуется обнаружением бластов не только в костном мозгу (свыше 20%), но и в периферической крови;
внекостно-мозговым (местным) - присутствие лейкемических инфильтратов вне костного мозга (в лимфоузлах, селезенке, лейкемидах кожи и др.).
Терминальная стадия острого лейкоза представляет собой завершающий этап опухолевой прогрессии при полном истощении нормального кроветворения и резистентности к цитостатической терапии. Причиной гибели пациентов чаще всего являются инфекционно-воспалительные осложнения (перитонит, пневмония, сепсис и др.), кровотечения, кровоизлияния во внутренние органы.
Под выздоровлением подразумевают полную ремиссию, сохраняющуюся в течение 5 лет и более.
Составляющие субстрат опухоли бластные клетки при различных вариантах острого лейкоза морфологически трудноразличимы. Для определения линейной принадлежности и степени зрелости бластных клеток с целью дифференциальной диагностики отдельных форм и цитологических вариантов острых лейкозов применяются цитохимическое исследование и метод идентификации поверхностных, цитоплазматических и ядерных антигенов (т.е. иммунофенотипа) бластных клеток костного мозга и крови. В качестве базисных цитохимических методов диагностики острых лейкозов проводят определение в бластах содержания и характера распределения липидов, гликогена, кислых сульфатированных мукополисахаридов, активности миелопероксидазы, кислой фосфатазы, неспецифической эстеразы (α-нафтилацетатэстеразы), хлорацетатэстеразы (табл. 14-13).
В 1975 г. гематологами Франции, США и Великобритании была создана Франко-американо-британская классификация острых лейкозов, базирующаяся на цитоморфологических признаках бластных клеток - ФАБ-классификация, получившая наиболее широкое применение в практике. Согласно цитоморфологической ФАБклассификации, острые лейкозы подразделяют на две группы - миелоидные и лимфобластные лейкозы, в структуре которых выделены следующие цитологические варианты:
1. Острые миелоидные лейкозы (ОМЛ)
М0 - острый миелобластный лейкоз с минимальными признаками дифференцировки
М1 - острый миелобластный лейкоз без признаков вызревания М2 - острый миелобластный лейкоз с признаками вызревания М3 - гипергранулярный острый промиелоцитарный лейкоз М3v - микрогранулярный острый промиелоцитарный лейкоз М4 - острый миеломонобластный лейкоз М5а - острый монобластный лейкоз без признаков вызревания М5b - острый монобластный лейкоз с признаками вызревания М6 - острый эритробластный лейкоз (эритролейкоз) М7 - острый мегакариобластный лейкоз
2. Острые лимфобластные лейкозы (ОЛЛ) L1 - микролимфобластный ОЛЛ
L2 - ОЛЛ с типичными бластами L3 - макролимфобластный ОЛЛ
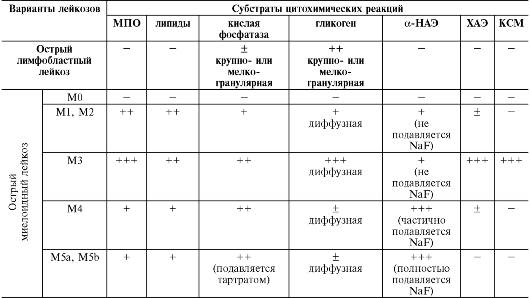
Таблица 14-13. Цитохимические особенности бластных клеток при острых лейкозах различного происхождения
 Окончание табл. 14-13
Окончание табл. 14-13
 Примечание. МПО - миелопероксидаза; -НАЭ--нафтилацетатэстераза; ХАЭ - хлорацетатэстераза; КСМ - кислые
Примечание. МПО - миелопероксидаза; -НАЭ--нафтилацетатэстераза; ХАЭ - хлорацетатэстераза; КСМ - кислые
сульфатированные мукополисахариды; «-» - отрицательная реакция; «+» - положительная реакция в единичных клетках; «+» - слабая реакция; «++» - умеренная реакция; «+++» - интенсивная реакция.
Выделенные нозологические формы острых лейкозов различаются по клиническим признакам и, что особенно важно, по ответу на цитостатическую медикаментозную терапию. У взрослых больных чаще встречаются миелобластный и лимфобластный, у детей - лимфобластный и (реже) недифференцированный варианты острого лейкоза.
Острый недифференцированный лейкоз, вариант М0. Морфологический субстрат опухоли представлен клетками II-III классов по современной схеме кроветворения, которые морфологически напоминают лимфобласты, но отличаются цитохимической интактностью (см. табл. 14-13). Из хромосомных аномалий для МО типичны моносомия 7, трисомия 4, 8, 13.
Острый миелобластный лейкоз. Представляет собой опухоль, исходящую из клетки-предшественницы миелопоэза и состоящую преимущественно из родоначальных клеток гранулоцитарного ряда - миелобластов. Выделяют 2 варианта ОМЛ - М1 и М2, для которых свойственны транслокации хромосом соответственно t(9;22) и t(8;21). В костном мозгу и крови у больных ОМЛ обнаруживаются многочисленные миелобласты средних размеров с узким ободком незернистой цитоплазмы и крупные миелобласты с обширной (иногда вакуолизированной) цитоплазмой с азурофильными гранулами и 1-2 палочками Ауэра (они могут определяться в более зрелых клетках гранулоцитарного ряда). Для зрелых нейтрофилов характерна гиперили гипосегментация ядер, «истощение» цитоплазматической зернистости.
Острый промиелоцитарный лейкоз. Для лейкозных клеток при этой форме острого лейкоза характерны транслокации хромосом: t(15;17), t(5;17), t(11;17). Атипичные промиелоциты содержат большое количество крупных (при гипергранулярном варианте - М3) или мелких (при микрогранулярном варианте - M3v) гранул и палочки Ауэра (нередко их 1О-2О и более). При слиянии палочек Ауэра образуются «faggot cells» - клетки с «пучком прутьев». Ядра атипичных промиелоцитов имеют рыхлую структуру хроматина, неправильную форму со смазанными контурами (иногда их форма неразличима из-за обилия гранул в цитоплазме).
Острый монобластный лейкоз. Существует два его варианта - без признаков вызревания клеток (М5а) и с признаками вызревания клеток (М5Ь), при которых обнаруживаются транслокационные перестройки хромосом t(9;11) и t(4;11). При М5а субстрат опухоли составляют монобласты крупных размеров с обширной
серо-голубой цитоплазмой, скудной азурофильной зернистостью и вакуолизацией. При М5b преобладающим типом клеток в костном мозгу и крови являются промоноциты (количество монобластов не превышает 10-15%).
Острый миеломонобластный лейкоз или вариант М4 острого лейкоза. В его основе лежат перестройки хромосомы 16: inv (16), t(16;16), t (8;16). Для М4 характерно присутствие в костном мозгу одновременно двух типов атипичных бластов - миелобластов и монобластов. В крови могут обнаруживаться также промоноциты.
Острый эритробластный лейкоз или М6. Наиболее частой цитогенетической аномалией при М6 является делеция длинного плеча хромосомы 5 или 7. Субстрат опухоли составляют клетки эритроидного ряда: эритронормобласты, гигантские, многоядерные эритрокариоциты с мегалобластическим оттенком, мегалобласты, аномальные эритроидные клетки с вакуолизированной и отростчатой цитоплазмой, с кариорексисом. В крови отмечаются выраженный анизо- и пойкилоцитоз, гиперхромия эритроцитов, появление в кровотоке эритроцитов с базофильной зернистостью, кольцами Кабо, эритробластов, полихроматофильных и оксифильных эритронормобластов.
Острый мегакариобластный лейкоз, вариант М7. Характерными цитогенетическими признаками М7 являются inv (3), t(3;3), t(1;22). В костном мозгу и крови выявляются мегакариобласты и их осколки. В крови обнаруживается тромбоцитоз (более 1000-109/л). Тромбоциты имеют гигантские размеры, могут склеиваться в «кучки», имеется качественный дефект клеток - «серые» тромбоциты (в результате дефекта α-гранул).
Острый лимфобластный лейкоз. Это опухоль, возникающая из клетки-предшественницы лимфопоэза. В костном мозгу при ОЛЛ выявляется тотальная лимфобластная метаплазия. Картина периферической крови при ОЛЛ характеризуется присутствием бластных клеток. Согласно ФАБ-классификации, в зависимости от цитоморфологических признаков лимфоидных клеток выделяют три цитологических варианта ОЛЛ: L1 (микролимфобластный), представленный однородной популяцией клеток малых размеров; L2 (с типичными бластами), характеризующийся неоднородностью клеток, среди которых преобладают крупные клетки, реже выявляются клетки средних и малых размеров; L3 (макролимфобластный), при котором обнаруживаются клетки только крупных размеров.
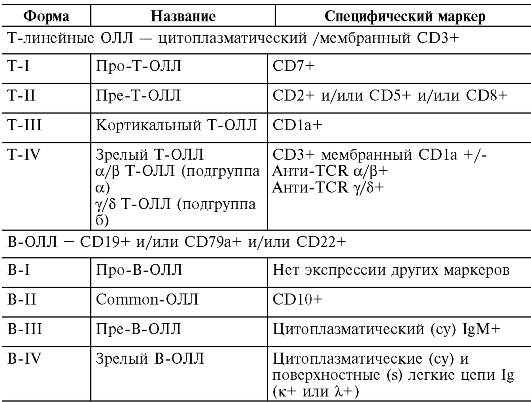
В 1995 г. Европейской группой по иммунологической характеристике лейкозов (European Group for the immunological characterization of leukemias, EGIL) была предложена классификация острых лимфобластных лейкозов по иммунологическому принципу. В соответствии с EGIL-классификацией их подразделяют на Т- и В-линейные лейкозы (табл. 14-14).
Таблица 14-14. EGIL-классификация острых лимфобластных лейкозов
(ОЛЛ)
 Хронические лейкозы. Несколько упрощенно классификацию хронических лейкозов можно представить в следующем виде. 1. Хронические миелопролиферативные лейкозы: Хронический миелолейкоз
Хронические лейкозы. Несколько упрощенно классификацию хронических лейкозов можно представить в следующем виде. 1. Хронические миелопролиферативные лейкозы: Хронический миелолейкоз
• Ph-позитивный (типичный, взрослый тип)
• Ph-негативный (атипичный, ювенильный тип) Хронический миеломоноцитарный лейкоз Хронический нейтрофильный лейкоз Хронический эозинофильный лейкоз Хронический базофильный лейкоз
Хронический тучноклеточный лейкоз Истинная полицитемия (эритремия) Тромбоцитемия
Хронический идиопатический миелофиброз (сублейкемический миелоз)
2. Хронические лимфопролиферативные лейкозы:
В-клеточные хронические лимфолейкозы Хронический лимфолейкоз Волосатоклеточный лейкоз Парапротеинемические гемобластозы
• Множественная миелома (миеломная болезнь)
• Макроглобулинемия Вальденстрема
• Болезни тяжелых цепей
Т- и ЕК-клеточные (из ЕК-клеток - естественных киллеров) хронические лимфолейкозы
Болезнь Сезари (лимфоматоз кожи)
Лейкоз из больших гранулосодержащих лимфоцитов (ЕКклеток)
В отличие от острых лейкозов моноклоновая («доброкачественная») стадия хронических лейкозов является более продолжительной (годы, десятилетия). В развитии хронических лейкозов выделяют хроническую фазу, которая характеризуется длительным компенсированным течением, и фазу бластной трансформации, проявляющуюся бластным кризом с резким увеличением количества бластных клеток в костном мозгу и периферической крови (более 30%), прогрессированием анемии, тромбоцитопении и формированием внекостно-мозговых лейкемических инфильтратов.
Клинико-лабораторная картина хронических лейкозов характеризуются разнообразием признаков, строго специфичных для определенной формы заболевания. Наиболее распространенными вариантами хронических лейкозов являются хронический миелолейкоз, хронический миеломоноцитарный лейкоз, эритремия, сублейкемический миелоз, хронический лимфолейкоз, парапротеинемические гемобластозы и лимфоматоз кожи.
Хронический миелолейкоз. Одно из самых частых заболеваний в группе лейкозов. Морфологическим субстратом хронического миелолейкоза (ХМЛ) являются зрелые и созревающие клетки гранулоцитарного ростка кроветворения (лейкоэритробластическое отношение в костном мозгу увеличивается до 20:1 при 2:1-4:1 в норме). По современным представлениям ХМЛ возникает в резуль-
тате соматической мутации в стволовой клетке-предшественнице миелопоэза, что в 85-95% случаев приводит к образованию хромосомного маркера - Ph'-хромосомы (см. рис. 14-12), являющейся продуктом делеции хромосомы 22 или транслокации дистальной части длинного плеча хромосомы 22 на хромосому 9. У детей ХМЛ встречается в двух вариантах - с филадельфийской хромосомой в кариотипе лейкозных клеток (взрослый тип заболевания) и без нее (ювенильный тип).
Течение хронического миелолейкоза как у взрослых, так и у детей разделяют на стадии или фазы заболевания в зависимости от степени зрелости клеточного состава крови. В хронической фазе типичного ХМЛ общее количество лейкоцитов в периферической крови колеблется от 50-109/л и более (у 25% больных - более 350-109/л). Отмечается нейтрофильный лейкоцитоз с выраженным ядерным сдвигом влево: обнаруживаются единичные миелобласты (2-3%), промиелоциты, миелоциты, метамиелоциты, палочко- и сегментно-ядерные формы гранулоцитов. Количество промиелоцитов и миелоцитов увеличивается по мере прогрессирования болезни при одновременном уменьшении числа палочкоядерных и сегментно-ядерных форм гранулоцитов. Отмечаются выраженная эозинофилия и базофилия (эозинофильно-базофильная ассоциация). В гранулоцитах обнаруживаются признаки дегенерации - псевдопельгеризация, низкая активность щелочной фосфатазы. У детей ювенильная (Ph-негативная) форма ХМЛ характеризуется высоким моноцитозом и тромбоцитопенией. В период бластной трансформации происходит резкое «омоложение» лейкоцитарной формулы за счет увеличения числа промиелоцитов и миелобластов (не менее 30%), прогрессирует цитопения (анемия, лейко-и тромбоцитопения), возникают лейкемические инфильтраты в коже, лимфоузлах, миокарде и других органах. При кариологическом исследовании выявляется поликлоновость патологических клеток (анэуплоидия), которая является основным признаком терминальной стадии - новым этапом опухолевой прогрессии.
Хронический миеломоноцитарный лейкоз характеризуется гиперклеточностью костного мозга за счет увеличения количества незрелых и зрелых клеток гранулоцитарного и моноцитарного ряда (промоноцитов, моноцитов). Миелобласты и монобласты составляют не более 5% от общего числа миелокариоцитов. В периферической крови обнаруживаются незрелые клетки нейтрофильного ряда (не более 10% от общего количества лейкоцитов), промоно-
циты, реже - бласты. В гранулоцитах - псевдопельгеризация, «истощение» зернистости в цитоплазме, отрицательная реакция на миелопероксидазу, низкая активность лейкоцитарной щелочной фосфатазы. В сыворотке крови и моче устанавливается высокое содержание лизоцима.
Эритремия (истинная полицитемия, болезнь Вакеза). Заболевание опухолевой природы, характеризующееся относительно доброкачественным течением. Источником роста опухоли является клетка-предшественница миелопоэза, основной субстрат опухоли - эритроциты. Наиболее характерны изменения со стороны периферической крови: количество эритроцитов достигает (6-12)-1012/л, уровень гемоглобина - 180-220 г/л, показатель гематокрита увеличивается до 60-80%. Уровень эритропоэтина в крови и моче в отличие от симптоматических эритроцитозов остается нормальным. Имеются лейко- и тромбоцитоз, уменьшается СОЭ, возрастает вязкость крови. Важным диагностическим признаком является увеличение массы циркулирующих эритроцитов, опосредующее гиперемию кожи и слизистых, окклюзию микрососудов и связанные с ней головные боли, боли в суставах, позвоночнике, эпигастрии и др.
Сублейкемический миелоз характеризуется гиперклеточностью костного мозга за счет гиперплазии гранулоцитарного, эритроидного и мегакариоцитарного ростков, а также миелофиброзом и миелосклерозом, при прогрессировании которых клеточность костного мозга постепенно снижается. В крови обнаруживаются незрелые клетки гранулоцитарного ряда, гипо- и гиперсегментированные нейтрофилы, миелобласты (1-5%). Количество тромбоцитов варьирует. Нередко выявляются крупные гипогранулярные тромбоциты:, аномальные мегакариоциты и их фрагменты. Гематологическими признаками сублейкемического миелоза, позволяющими дифференцировать его с ХМЛ, наряду с выраженным фиброзом и склерозом костного мозга, являются: увеличение общего количества лейкоцитов в крови не более 50-109/л (при ХМЛ более 50-109/л), умеренная базофилия при нормальном содержании эозинофилов (при ХМЛ сочетанное увеличение количества базофилов и эозинофилов - эозинофильно-базофильная ассоциация) и высокая активность щелочной фосфатазы в нейтрофилах (при ХМЛ активность лейкоцитарной щелочной фосфатазы низкая).
Хронический лимфолейкоз. Это опухоль иммунокомпетентной ткани, состоящая преимущественно из зрелых лимфоцитов, пред-
ставленных в большинстве случаев В-клетками. Характерен лейкоцитоз; в мазках крови преобладают зрелые узкоцитоплазменные лимфоциты, содержание которых может доходить до 80% и более. Важным признаком служит появление дегенеративных форм лимфоцитов - теней Гумпрехта (результат раздавливания качественно неполноценных лимфоцитов при приготовлении гематологических мазков), голых ядер лимфоцитов и форм Ридера. Количество лимфоцитов в костном мозгу составляет не менее 30% всех миелокариоцитов. Разрастание лимфоидной ткани имеет место в лимфатических узлах, селезенке и печени, что сопровождается увеличением указанных органов.
Функциональная неполноценность образующих опухоль лимфоцитов приводит к нарушению иммунологического гомеостаза у больных, что, в свою очередь, становится причиной аутоиммунных конфликтов (аутоиммунные гемолитические анемии и тромбоцитопении); инфекционных осложнений (вследствие нарушения антителообразования) и т.д.
В отличие от хронического миелолейкоза бластные кризы наблюдаются крайне редко, не развивается также вторичной резистентности к цитостатическим препаратам.
Парапротеинемичские гемобластозы. К парапротеинемическим гемобластозам относятся миеломная болезнь (множественная миелома, плазмоцитома), макроглобулинемия Вальденстрема и болезни тяжелых цепей - опухоли В-клеточного происхождения. Главной особенностью данных лейкозов является сохранение способности В-клеток к дифференцировке до стадии иммуноглобулинсекретирующих клеток. При этом секретируемые ими иммуноглобулины отличаются однообразием структуры (моноклональные парапротеины), что объясняется их происхождением из одного клона опухолевых клеток. Парапротеины соответствуют разным вариантам нормальных иммуноглобулинов (чаще IgG или IgM), отличаясь от них строгой однотипностью тяжелых и легких цепей, либо представляют собой структурно аномальные молекулы иммуноглобулинов (изолированные фрагменты тяжелых цепей, свободные легкие цепи).
При множественной миеломе имеет место диссеминированная злокачественная пролиферация клона В-лимфоцитов на уровне плазматических клеток. Множественная миелома составляет около 1% всех злокачественных новообразований, частота встречаемости миеломной болезни колеблется в разных этнических группах
от 1 до 10 на 100 000 населения. Плазматические клетки наиболее часто пролиферируют диффузно по костному мозгу, но иногда формируют солитарную опухоль, называемую плазмоцитомой. Из-за остеолитических повреждений, обусловленных продукцией опухолевыми клетками остеокластактивирующих факторов (IL-1, TNF-α, TNF-β), развивается гиперкальциемия и связанные с ней поражения нервной, сердечно-сосудистой системы, почек, желудочно-кишечного тракта, формируются тромбоцитопения, анемия, лейкопения. Одновременно подавляется формирование нормальных плазматических клеток, что приводит к нарушению образования других иммуноглобулинов, развивается синдром возвратных инфекций.
В случае выявления парапротеинов при электрофорезе сыворотки крови обязательным является электрофоретическое исследование мочи. В 20% случаев миеломной болезни опухоль продуцирует только легкие цепи иммуноглобулинов, которые из-за низкой молекулярной массы быстро фильтруются в почках и могут не обнаруживаться в сыворотке, но выявляются в моче (протеинурия Бенс-Джонса). В связи с этим для подтверждения диагноза методом электрофореза определяют белок Бенс-Джонса в моче, который располагается недалеко от старта соответственно М-градиенту в сыворотке, между γ- и β-глобулинами.
Макроглобулинемия Вальденстрема характеризуется тем, что опухолевые В-лимфоциты продуцируют макромолекулярные моноклональные парапротеины класса IgМ. Из-за накопления высокомолекулярных белков характерны повышение вязкости крови, нарушение микроциркуляции, сладж-синдром, предрасположенность к тромбозам, геморрагический синдром. Болеют преимущественно мужчины после 60 лет. Картина крови характеризуется анемией, в патогенезе которой играют роль опухолевое подавление эритропоэза, кровопотери, нередко развивается лейкопения с нейтропенией, моноцитоз, тромбоцитопения присоединяется по мере прогрессирования заболевания. СОЭ всегда резко увеличена, в сыворотке гиперпротеинемия, а на электрофореграмме - М-градиент за счет IgМ. В моче белок Бенс-Джонса встречается примерно в 80% случаев, но количество его значительно меньше, чем при множественной миеломе. В отличие от миеломной болезни при макроглобулинемии Вальденстрема обычно обнаруживаются увеличение лимфоузлов и гепатоспленомегалия, но лимфоидная инфильтрация прогрессирует, как правило, относительно медленно.
При этом поражение костей и гиперкальциемия отмечаются редко. Проявления болезни исчезают при замещающей гемотрансфузии.
Болезни тяжелых цепей представляют собой В-клеточные лимфатические опухоли с разнообразной клинической и морфологической картиной и секрецией фрагментов тяжелых цепей различных классов иммуноглобулинов. Это обычно α-цепи, но могут быть также γ- или μ-цепи. Выделяют две формы течения болезни: абдоминальную и легочную. Абдоминальная форма характеризуется диффузной инфильтрацией слизистой тонкой кишки и мезентериальных лимфатических узлов лимфоидными и плазматическими клетками, макрофагами, тучными клетками. Поражение желудочно-кишечного тракта приводит к атрофии ворсинчатого эпителия и развитию синдрома мальабсорбции. Легочная форма протекает с бронхопульмональными поражениями и медиастинальной лимфаденопатией. Протеинурия отсутствует. Диагностика основана на иммунохимическом анализе сывороточных белков, позволяющем выявить тяжелые цепи иммуноглобулинов.
Болезнь Сезари (лимфоматоз кожи) проявляется генерализованной эритродермией, алопецией, поражением век, дистрофией ногтей, интенсивным зудом кожи. У 30% больных отмечается спленомегалия, у 60% - лимфаденопатия смешанной природы (одни лимфатические узлы увеличиваются реактивно вследствие присоединения кожных инфекций, другие - в связи с их лейкемической инфильтрацией). При исследовании трепанобиоптатов костного мозга обнаруживаются очаги лимфоидной инфильтрации из малых лимфоцитов и клеток Сезари - атипичных Т-лимфоцитов со светлой цитоплазмой и складчатыми (конволютными) ядрами. Содержание гемоглобина, количество эритроцитов и тромбоцитов в крови обычно сохраняется в пределах нормы. Характерен лимфоцитоз (до 70-109/л), наличие клеток Сезари в мазках крови.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 4072; Нарушение авторских прав?; Мы поможем в написании вашей работы!