
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Плотность 750
|
|
|
|
Расчет реактора
Рассчитать реактор технологической установки при следующих данных:
Таблица - Материальный баланс ТУ производительностью
| Приход | Расход | ||||||
| Компонент | % масс | кг/ч | т/г | Компонент | % масс | кг/ч | т/г |
| Сырье | УВГ Головка стабилизации Катализат ВСГ | 7,4 4,5 82,3 5,8 | |||||
| Итого |
Часовая загрузка по сырью
G=120000 т/г
G= 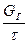 (1)
(1)
G= 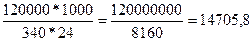 кг/ч
кг/ч
Объемный часовой расход сырья на установку
VБ= 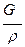 (2)
(2)
Объемный расход ВСГ в тройнике смешения
Vвсг=K*Vδ (3)
где К – кратность циркуляции
Vвсг=
Масса ВСГ
m=Vвсг*ρвсг (4)
m= кг
Материальный поток ВСГ
Nвсг= 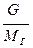 (5)
(5)
Nвсг= 
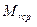 =
= 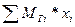 (6)
(6)
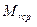 = =33,726
= =33,726
Таблица 5 - Состав ВСГ
| Компоненты | Молекулярная масса | Объемные % | Моль ные доли | Молекуля рная масса ВСГ | ВСГ массовые доли | кг/ч | кмоль/ч |
| H2 C C2 C3 C4 nC4 iC5 nC5 C6 Итого | 84,37 5,02 3,32 5,07 0,77 1,1 0,19 0,1 0,06 | 1,6874 0,8032 0,9960 2,2308 0,4466 0,6380 0,1368 0,0720 0,0516 7,062 | 0,2389 0,1137 0,1410 0,3159 0,0632 0,0903 0,0194 0,0102 0,0073 1,0000 |
Материальный поток сырья на установку
XI= 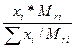 (7)
(7)
XI= 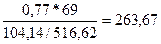
Таблица 6 - Материальный поток сырья на установку
| Температура | Массовые доли | Mr | Массовые доли/Mr | Мольные доли | Мольные доли*Mr | кг/ч | кмоль/ч |
| 15-60 60-100 100-120 120-150 150-169,5 Итого | 0,11 0,17 0,27 0,2 0,25 1,00 | 90,4 105,1 118,72 133,4 516,62 |
Таблица 7 - Материальный баланс
| Компонент | ВСГ, кг/ч | Сырье, кг/ч | ∑ | Xi, масс |
| H2 C C2 C3 C4 nC4 iC5 nC5 C6 15-60 60-100 100-120 120-150 150-169,5 Итого | - - - - - 4277100,9 | - - - - - - - - - | 23,81 11,33 14,05 31,48 6,29 8,99 1,93 1,01 0,72 0,03 0,05 0,09 0,06 0,08 100,64 |
Над платиновым катализатором при изомеризации протекают следующие реакции:
превращение нафтеновых углеводородов в ароматические:
СnH2n ↔ СnH2n-6 + 3H2
превращение нафтеновых углеводородов в парафиновые:
СnH2n + H2 ↔ СnH2n+2
гидрокрекинг нафтеновых углеводородов:
СnH2n +n/2H2 ↔ n/15 (CH4+C2H6+ C3H8+С4H10 + C5H12)
гидрокрекинг парафиновых углеводородов:
СnH2n+2 + 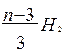 ↔ n/15 (CH4+C2H6+ C3H8+С4H10 + C5H12)
↔ n/15 (CH4+C2H6+ C3H8+С4H10 + C5H12)
превращение нормальных парафиновых углеводородов в изомерные:
н-СnH2n+2  ↔ иСnH2n+2
↔ иСnH2n+2
где n- углеродное число (число углеродных атомов в молекуле углеводорода).
Для указанных реакций можно записать четыре дифференциальных уравнения, описывающих уменьшение количества углеводородов в результате химических превращений:
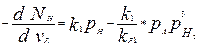 (8)
(8)
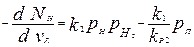 (9)
(9)
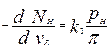 (10)
(10)
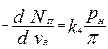 (11)
(11)
где NП – доля н парафиновых углеводородов в питании, подвергнутых химическому превращению, кмоль/кмоль; vR – величина, обратная объемной скорости питания, кг катализатора/(кмоль/ч) сырья; k1- константа скорости реакции, определяемая из графика, кмоль/(ч*Па*кг катализатора); pH, pА, pП, pH2 – парциальные давления парафиновых углеводородов и водорода, Па; kP1- константа химического равновесия, Па3; k2 – константа скорости реакции определяемая из графика, кмоль/(ч*Па2*кг катализатора); kP2- константа химического равновесия, Па-1; k3, k4 – константы скорости реакций,определяемые из графика, кмоль/(ч*кг катализатора).
Константы химического равновесия рассчитываются по уравнениям:
kP1=9.813*1012 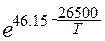 (12)
(12)
kP2=9.81-1*10-3 
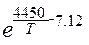 (13)
(13)
где Т- температура в реакторе, К.
Уравнения не учитывают состояния катализатора. Однако ввиду отсутствия в литературе сведений о зависимости степени химических превращений при риформинге от состояния катализатора, из-за малого (всего 0.5-0.7%) содержания платины и возможности компенсации снижения активности катализатора некоторым повышением температуры процесса, указанные уравнения обеспечивают достаточную точность при проектировании.
Для уменьшения коксовых отложений осуществляют при избытке водорода. С этой целью в блоке циркулирует водородосодержащий газ.
Основные реакции сопровождаются значительным увеличением объема, поэтому процесс протекает под повышенным давлением в интервале (2÷4)* 106Па.
Примем давление в начале процесса 22кгс/м2 = 22*0,980665*105 Па = 2,15*106 Па (22атм).
Изомеризацию проводят в интервале температур 740-810 К. По мере отработки катализатора температуру повышают до 790-810 К. Примем в расчете температуру подачи сырья и циркулирующего газа в реактор ТВХ1=793К.
В промышленных реакторах объемная скорость подачи сырья равна 1-3 ч-1 В расчете используем числовое значение объемной скорости подачи сырья v0 = 1.5ч-1. Циркуляцию водородосодержащего газа поддерживают в интервале 900-1850 м3 (при нормальных условиях) на 1 м3 сырья. Принимаем кратность циркуляции газа по данным производства nГ= 1500м3/м3. Содержание водорода в водородосодержащем газе достигает 83-93 объем.%. Состав циркулирующего газа приведен в таблице.
Таблица8
| Компоненты | H2 | CH4 | C2H6 | C3H8 | C4H10 | C5H12 | C6H14 |
| Содержание, объемн.% | 84,37 | 5,02 | 3,32 | 5,07 | 1,87 | 0,29 | 0,06 |
В уравнениях уменьшение количества углеводородов в питании в результате химических превращений выражено в мольных долях, а состав питания задан в массовых долях. Для пересчета состава питания воспользуемся формулой:
МС yI= MIyI’ (14)
где МС – средняя молекулярная масса сырья;
МI – средняя молекулярная масса I-ого компонента (фракции) сырья;
YI – cодержание I-го компонента в питании в массовых долях;
YI’ –тоже в мольных долях.
Среднюю молекулярную массу сырья рассчитаем по формуле:
MC = 0.4 T50 – 45 (15)
где Т50 – температура выкипания 50% бензина, К.
При температуре Т50 = 110+273 = 383К средняя молекулярная масса сырья равна:
МС = 0,4*391 – 45 = 111,4
Необходимый реакционный объем, м3:
Vр=  м3
м3
Задавшись кратностью циркуляции, находят его количество в объемных единицах, нм3/ч:
Vц.г =Wк.р К (16)
где К – кратность циркуляции ВСГ, нм3/ч3
Vц.г =160,13*1366=218737,58
Массовое количество циркулирующего газа, кг/ч:
Gц.г= 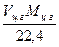 (17)
(17)
где, Мц.г – молекулярная масса циркулирующего газа
Gц.г=
Парциальные давления компонентов в сырье ввиду не очень высокого давления и значительного разбавления водородом рассчитываем по формуле:
PI = π yI’ (18)
где π – общее давление в аппарате, Па;
yI’ – содержание i-го компонента в смеси газов, мол. доли.
PIа=2,26*0,127=0,287
PIн=2,26*0,382=0,863
PIп=2,26*0,491=1,109
Количество сырья (в кмоль) равно:
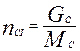 (19)
(19)
где GC – количество сырья, кг/час.
Величина GC=
Подставив числовое значение величины GС в предыдущую формулу, получим:
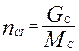 =
=
 кмоль/ч
кмоль/ч
Количество водородосодержащего газа:
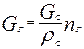
(20)
где nГ – кратность циркуляции газа, м3/м3;
ρС – плотность сырья в жидком виде (при нормальных условиях), кг/м3.
Плотность сырья равна:
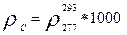 кг/м3
кг/м3
Подставив в формулу числовые значения величин, находим:
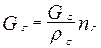 =
=
м3/ч
Количество циркулирующего газа в кмолях равно:
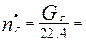 кмоль/ч (21)
кмоль/ч (21)
Таблица – Определение состава циркулирующего газа
| Компоненты | Молекулярная масса Mi | Cодержание Y’гi (таблица 7.2.) мол.доли | МiyГ i’ | Количество NГ i=nГ i’ *yГ i’ кмоль/ч |
| H2 | 0,84 | |||
| CH4 | 0,05 | |||
| C2H6 | 0,03 |
Продолжение таблицы
| C3H8 | 0,05 | |||
| C4H10 | 0,01 | |||
| C5H12 | 0,002 | |||
| C6H14 | 0,001 | |||
| Cумма | - | 1,00 | МГ = 6,48=6,5 | 605544,78 |
Общее количество парафиновых углеводородов в циркулирующем газе равно:
605544,78 – 510899,7 = 94645,08 кмоль/ч
Таблица – Данные расчета по определению состава смеси сырья и водорода и парциальных давлений ее компонентов
| Компоненты | Количество n3 i кмоль/ч | Содержание y3i= 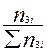 мол. доли мол. доли
| Парциальное давление Pi = π*y3i’=2.15*106 y3i’ Па |
| Cумма | 1145,03 | ||
| H2 | 891,82 | ||
| СnH2n+2* | 145,18 | ||
| СnH2n+2 | 47,75 | ||
| СnH2n | 48,83 | ||
| СnH2n-6 | 11,45 |
Количество катализатора, необходимого для проведения реакции:
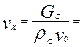
(22)
Насыпная масса алюмоплатинового катализатора равна ρК = 560-700 кг/м3. Приняв насыпную массу катализатора ρК = 650 кг/м3, находим количество катализатора:
GK = VK * ρК =
(23)
Расчет реактора
Константа скорости реакции изомеризации. Зная температуру подачи сырья в первый реактор ТВХ1 = 793К, из графика при данной температуре находим k1 = 314,5*10-9 кмоль/(ч*Па кг катализатора).
Константа химического равновесия реакции изомеризации. При температуре ТВХ1 = 793К по уравнению найдем:
KP1=9.813*1012 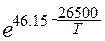 = 14.96*1020Па3
= 14.96*1020Па3
Материальный баланс реакций в реакторе. На основе рассчитанного количества прореагировавшего сырья и стехиометрических уравнений (1)-(4) в таблице 15 сделан расчет материального баланса реакций.
Из таблицы 7.9 следует, что в результате гидрокрекинга получается углеводородный газ, который обогатит циркулирующий газ.
Количество углеводородного газа, образовавшегося в реакторе, при n=7.7 равно:
(4,11+3,95)*7,7/15 (CH4+C2H6+ C4H10 C3H8+C5H12+C6H14) = 52,6*(CH4+C2H6+ C4H10 C3H8+C5H12+C6H14)
Cостав газа, покидающего реактор.
Cостав газа, покидающего реактор рассчитаем на основе данных таблиц.
Этот расчет необходим для составления материального баланса реактора.
Таблица16 – Cостав газа, покидающего реактор
| Компоненты | Приход, кмоль/ч | Расход, кмоль/ч |
| СnH2n-6 | 174,8 | 174,8+446=3620,8 |
| СnH2n | 526-446+6-39,8=17,89 | |
| СnH2n+2 | 676,2 | 676,2-6-62,7=607,5 |
| Сумма | 1274,5 | |
| Циркулирующий газ | ||
| H2 | 510899,7 | 510899+4,46*3+6-39,8*7,7/3-62,7*(7,7-3)/3 = 512043,35 |
| CH4 | 30394,14 | 30394,14+47,9=30442,04 |
| C2H6 | 20102,37 | 20102,37+47,3=20149,67 |
| C3H8 | 30707,64 | 30707,64+47,3=30754,94 |
| 4H10 | 11319,56 | 11319,56+47,3=11366,86 |
| C5H12 | 1758,32 | 1758,32+47,3=1805,62 |
| C6H14 | 363,05 | 363,05+47,3=410,35 |
| Сумма | 605544,78 | 606972,83 |
| ВСЕГО | 606921,78 | 608247,33 |
Материальный баланс реактора. Материальный баланс реактора составляется для определения выхода продуктов
Таблица17 – Материальный баланс реактора
| Компоненты | Молекулярная масса Мi | Количество ni, кмоль/ч | Содержание yГ1i’= 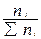 мол. доли мол. доли
| МiyГ 1i’ |
| H2 | 512043,35 | |||
| CH4 | 30442,04 | |||
| C2H6 | 20149,67 | |||
| C3H8 | 30754,94 | |||
| C4H10 | 11366,86 | |||
| C5H12 | 1805,62 | |||
| C6H14 | 410,35 | |||
| Сумма | - | 1123,08 |
Средняя молекулярная масса водородсодержащего газа на выходе из реактора рассчитана в таблице 17
Средние молекулярные массы углеводородов СnH2n-6, СnH2n и СnH2n+2, покидающих реактор, не будут равны соответствующим числовым значениям величин на входе в реактор. Рассчитаем новые числовые значения средних молекулярных масс указанных углеводородов.
Количество обогащенного циркулирующего газа на выходе из реактора
1123,08*6,9=7749,25кг/час=7750кг/ч
Таблица – Материальный баланс реактора
| Компоненты | Количество ni, кмоль/ч | Содержание yi’= 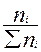 мол. доли мол. доли
| Средняя молекулярная масса Мi | Количество Gi = ni *Mi кг/час |
| Приход | ||||
| СnH2n-6 | 174,8 | 101,8 | ||
| СnH2n | 107,8 | |||
| СnH2n+2 | 676,2 | 109,8 | ||
| H2 | 510899,7 | 6,5 | ||
| СnH2n+2* | ||||
| Cумма | 514206,7 | - | ||
| Расход | ||||
| СnH2n-6 | 602,8 | 102,08 | ||
| СnH2n | 64,1 | 108,08 | ||
| СnH2n+2 | 616,8 | 110,08 | ||
| H2 | 512043,35 | 6,7 | ||
| СnH2n+2* | 2169,5 | |||
| Cумма | 515496,55 | - |
Из материального баланса реактора следует, что количество углеводородов, покидающих реактор, равно разности между количеством всего газового потока и количеством обогащенного водородосодержащего газа:
3583170 - 3445250=137920 кг/ч
Напишем уравнение материального баланса для углеводородов, покидающих реактор:
137920 = 602,8СnH2n-6 + 64,1СnH2n + 618,8СnH2n+2
C учетом данных таблицы 9, это уравнение принимает вид:
137920 = 602,8*(14n-6) + 64,1*(14n) + 618,8*(14n+2)
После вычисления найдем, что углеродное число равно n = 7,8. Принятое ранее при расчете количество образовавшегося газа n = 7,7 не могло привести к существенной погрешности при расчетах.
Тепловой баланс реактора
Рассчитаем энтальпию газового потока на входе в аппарат. Предварительный расчет показывает, что ввиду не очень высокого давления и значительного разбавления водородом поправка на давление величины энтальпии не требуется. Состав потока в мольных долях пересчитаем в массовые. Данные по энтальпии при температуре ТВХ1=793К для водорода, метана, этана, пропана, бутана и пентана можно найти в справочной литературе.
Таблица 0 – Расчет энтальпии питающей смеси
| Компоненты | Молекулярная масса Мi | Количество ni, кмоль/ч | Содер-жание yi’= 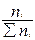 мол.доли мол.доли
| Мiyi’ | Содер-жание yi= 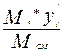 мол.доли мол.доли
| Энтальпия кДж/кг | |
| qTiГ | qTiГyi | ||||||
| H2 | |||||||
| CH4 | |||||||
| C2H6 | |||||||
| C3H8 | |||||||
| C4H10 | |||||||
| C5H12 | |||||||
| C6H14 | |||||||
| СnH2n-6 | 101,8 | ||||||
| СnH2n | 107,8 | ||||||
| СnH2n+2 | 109,8 | ||||||
| Сумма | - | - |
Тепловой эффект реакции рассчитать, пользуясь законом Гесса, нельзя из-за незнания детального химического состава сырья и продуктов реакции. Поэтому воспользуемся формулой:
qP = -335b (24)
где b- выход водорода в расчете на исходное сырье, масс %.
Из материального баланса реактора следует, что в результате изомеризации получен водород в количестве:
GH2 = 512043,35 -510899,7 = 1143,65 кмоль/ч
или
GH2 = 1143,65*МH2 = 1143,65 *2 = 2287,3 кг/ч
Тогда
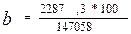 =1,5553 масс%
=1,5553 масс%
а тепловой эффект реакции:
qP = -335*1,5552=-519,25 кДж/кг
Тепловой эффект реакции лежит в пределах 356-838 кДж на 1 кг исходного сырья.
Тепловой баланс реактора с учетом принятой величины теплопотерь в окружающую среду в количестве Q4 = 0.01Q1 =0,113*103 кВт приведён в таблице
Из теплового баланса реактора имеем:
Q3 = Q1 –Q2 –Q4 = 148,3*103-20,5*103-1,48*103 =126,3*103 кВт (25)
Тогда
qГТвых1 = 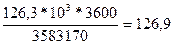 кДж
кДж
Таблица 21 – Тепловой баланс
| Потоки | Температура,К | Количество, кг/ч | Энтальпия, кДж/кг | Количество тепла, кВт |
| Приход | ||||
| Q1 | ТВХ1=801К | 2908,36 | 148,3*103 | |
| Сумма | - | - | 148,3*103 | |
| Расход | ||||
| Q2 | - | - | 519,25 | 20,5* 103 * |
| Q3 | ТВЫХ1 | qГТвых1 | Q3 | |
| Q4 | принимается | - | 1,48*103 | |
| Сумма | - | 148,3*103 |
Для определения числового значения температуры ТВЫХ1 потока, покидающего реактор, необходимо рассчитать состав смеси на выходе из реактора и построить вспомогательный график зависимости qГТвых1 =f (ТВЫХ1).
Состав газа, покидающего реактор, рассчитан на основе данных таблицы 16 и представлен в таблице
Таблица – Состав газа, покидающего реактор
| Компоненты | Молекулярная масса Мi | Количество ni, кмоль/ч | Содержание yi’= 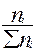 мол.доли мол.доли
| Мiyi’ | Содержание yi= 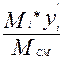 мол.доли мол.доли
|
| H2 | |||||
| CH4 | |||||
| C2H6 | |||||
| C3H8 | |||||
| C4H10 | |||||
| C5H12 | |||||
| C6H14 | |||||
| СnH2n-6 | 103,3 | ||||
| СnH2n | 109,3 | ||||
| СnH2n+2 | 111,3 | ||||
| Сумма | - |
Для построения вспомогательного графика зависимости qГТвых1 =f (ТВЫХ1) зададимся двумя ориентировочными числовыми значениями температуры: 713 К и 743 К. Значение энтальпии при этих температурах рассчитаны в таблице 23
Таблица23 – Значение энтальпии при температурах: 713 К и 743 К
| Компоненты | Содержание yi, масс.доля | Энтальпия, кДж/кг | |||
| 713 К | 743 К | ||||
| qГТi | qГТi*yi | qГТi | |||
| H2 | 0,2246 | ||||
| CH4 | 0,1017 | ||||
| C2H6 | 0,1158 | ||||
| C3H8 | 0,28 | ||||
| C4H10 | 0,2691 | ||||
| C5H12 | 0,0279 | ||||
| C6H14 | 0,0069 | ||||
| СnH2n-6 | 0,0125 | ||||
| СnH2n | 0,0013 | ||||
| СnH2n+2 | 0,0153 | ||||
| Сумма | 1,0000 | - | - |
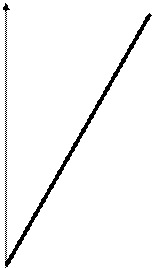
Вспомогательный график qГТвых1 =f (ТВЫХ1), построенный по данным таблице 23, представлен на рис. 1. Из него найдем, что энтальпии qГТвых1 =1958 кДж/кг соответствует температура ТВЫХ1 = 740 К.
Перепад температуры в первом реакторе равен ΔТ = ТВХ1 - ТВЫХ1 = 801 – 767 = 34 К.
qГТвых1
 | |||
 |
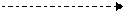
 2000
2000
 1900
1900




 1800
1800
Рисунок - График зависимости qГТвых1 =f (ТВЫХ1)
Основные размеры реактора
Диаметр реактора рассчитаем так, чтобы перепад давления ΔπСЛ1 в слое катализатора не превышал допустимого значения [ΔπСЛ1 ].
Величину [ΔπСЛ1 ] для реактора примем по данным таблицы:
[ΔπСЛ1 ] = 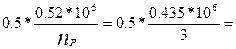 86666,7 Па = 0,086*106 Па
86666,7 Па = 0,086*106 Па
где 0,5 – доля гидравлического сопротивления слоя в общем гидравлическом сопротивлении реактора.
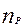 - число реакторов.
- число реакторов.
Последующим расчетом принятое значение должно быть подтверждено.
Для расчета воспользуемся формулой
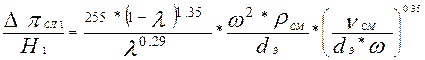 (26)
(26)
где 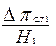 - потери напора на 1м высоты (толщины слоя катализатора в реакторе, Па/м);
- потери напора на 1м высоты (толщины слоя катализатора в реакторе, Па/м);
λ – порозность слоя;
ω – скорость фильтрования, м/с;
ρCМ – плотность газов кг/м3;
νСМ - кинематическая вязкость, м2/с;
dЭ – эквивалентный диаметр частиц катализатора, м.
По разности слоя катализатора при допущении упорядоченного расположения частиц катализатора равна:
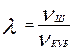 (27)
(27)
где vШ – объем шара, эквивалентный объему частицы катализатора цилиндрической формы, м3;
vКУБ – объем куба, описанного вокруг шара, м3.
Цилиндрические частицы алюмоплатинового катализатора имеют диаметр 2-3мм и высоту 4-5мм. Если принять диаметр цилиндрика равным d = 0,003м и высоту принять равной H = 0,005м, то
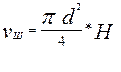 м3
м3
(28)
Сторона куба, описанного вокруг шара, равна эквивалентному dЭ диаметру этого шара:
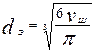 м (29)
м (29)
Числовое значение порозности при vКУБ = dЭ2:
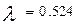
VCЕК – объем газов, проходящих через свободное сечение реактора найдем по формуле:
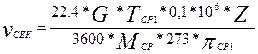 (30)
(30)
где G – количество газовой смеси в реакторе, кг/ч;
ТСР1 – средняя температура в реакторе, К;
Z = 1 – коэффициент сжимаемости газа, значительно разбавленного водородом;
МСР – средняя молекулярная масса газовой смеси; πСР1 – среднее давление в реакторе, Па.
Средняя температура в реакторе равна:
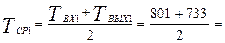 767 К (31)
767 К (31)
Среднее давление в реакторе примем равным:
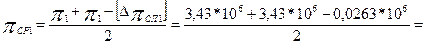 3,42*106 Па (32)
3,42*106 Па (32)
Тогда
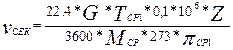 =
= 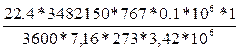 =248,59м3/с
=248,59м3/с
Приняв диаметр реактора DP1 = 1.6м, вычислим площадь поперечного сечения реактора, через которую проходит газ:
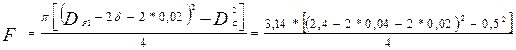
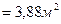
Высота слоя катализатора в стакане:
 (33)
(33)
Подставив числовые значения величин в формулу для расчета скорости фильтрации, получим:
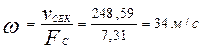 (34)
(34)
Допустимая скорость потока в аксиальных реакторах составляет 0,4 –0,6м/с., как видно скорость движения газового потока в реакторе находиться в допустимых пределах.
Плотность газовой смеси на выходе из реактора:
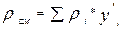 (35)
(35)
где ρI – плотность компонентов газовой смеси, кг/м3;
yI’ – содержание компонентов в газовой смеси, мол.доли (объемн. доли).
Плотность компонентов газовой смеси при средней температуре ТСР.1 = 771К в реакторе:
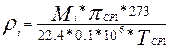 (36)
(36)
га де Мi –средние молекулярные массы компонентов
Результаты расчета плотности даны в таблице
Таблица – Расчет плотности
| Компоненты | Содержание Yi’, мол.доли. | Плотность ρI, кг/м3 | ρI * Yi’, |
| СnH2n-6 | 0,0011 | 56,13 | 0,0617 |
| СnH2n | 0,0001 | 59,39 | 0,0059 |
| СnH2n+2 | 0,0011 | 60,48 | 0,0665 |
| H2 | 0,9975 | 3,64 | 3,6309 |
| СnH2n+2* | |||
| Cумма | 1.0000 | - | 3,765 |
Определяется высота реактора
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 920; Нарушение авторских прав?; Мы поможем в написании вашей работы!