
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретические положения. Энтропии при плавлении олова
|
|
|
|
Энтропии при плавлении олова
Определение изменения
Методические указания
к лабораторной работе № 11
Пенза 2007
УДК 531.23
ББК 22я7
А 13
| Составители: | Г. И. Грейсух, доктор технических наук, профессор; Л.И.Абрамова, кандидат физико-математических наук, доцент; С.В.Голобоков, кандидат технических наук, доцент; Н.А. Очкина, кандидат технических наук, доцент |
| Рецензент – | В.Г.Недорезов, доктор технических наук, профессор |
Рассмотрены процессы нагревания и плавления олова, приведены расчетные формулы для определения изменения энтропии.
Методические указания подготовлены на кафедре физики и предназначены для использования студентами специальностей 290100, 290300, 290600 и др. в лабораторном практикуме по курсу общей физики.
© Пензенский государственный
Университет архитектуры и строительства, 2007
Цель работы – изучение процессов плавления и кристаллизации олова и определение изменения энтропии.
1. Теплоемкость твердых тел
Теплоемкостью твердого тела называется величина, равная отношению количества теплоты d Q, поглощаемого телом при бесконечно малом изменении его температуры dT, к этому изменению:
 . (1)
. (1)
Удельной теплоемкостью вещества называется физическая величина, равная количеству теплоты d Q, необходимому для нагревания единицы массы вещества на один Кельвин:
 . (2)
. (2)
Отсюда количество теплоты, необходимое для нагревания вещества, определяется выражением
 . (3)
. (3)
Молярная теплоемкость С m – физическая величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества
на 1 К:
 , (4)
, (4)
где n = 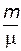 – количество вещества, выражающее число молей.
– количество вещества, выражающее число молей.
Удельная теплоемкость с связана с молярной Сm соотношением
 , (5)
, (5)
где m – молярная масса вещества.
Твердое тело – агрегатное состояние вещества, отличающееся стабильностью формы. Тепловое движение атомов твердого тела характеризуется малыми колебаниями около положения равновесия. Все вещества (за исключением гелия) при достаточно низких температурах переходят в твердое состояние. При подводе теплоты к твердому телу она расходуется на увеличение энергии колебаний атомов.
Согласно молекулярно-кинетической теории средняя кинетическая энергия, приходящаяся на одну степень свободы атома твердого тела

Полная энергия колебательного движения атомов в одном направлении складывается из кинетической и потенциальной энергии, которые равны друг другу, и может быть определена по формуле

Так как каждый атом обладает тремя степенями свободы, то полная энергия одного атома твердого тела равна:
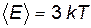 . (6)
. (6)
Внутренняя энергия одного моля равна:
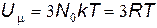 , (7)
, (7)
| где N 0 – | число Авогадро; |
| R – | универсальная газовая постоянная. |
При подводе теплоты в условиях постоянного объема все тепло уходит на увеличение внутренней энергии. Поэтому молярная (атомная) теплоемкость твердого тела определяется равенством:
 . (8)
. (8)
Из формулы (8) следует, что молярная теплоемкость твердых тел есть величина постоянная, одинаковая для всех веществ. Это утверждение называется законом Дюлонга и Пти.
Как показал опыт, при обычных температурах молярная (атомная) теплоемкость большинства твердых тел близка к значению 25,12 Дж/(К×моль) и почти не зависит от температуры.
|
|
|
|
|
Дата добавления: 2015-07-02; Просмотров: 319; Нарушение авторских прав?; Мы поможем в написании вашей работы!