
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Распространенные окислители и их продукты
|
|
|
|
| Окислитель | Полуреакции | Продукт | Стандартный потенциал, В |
| O2 кислород | 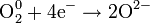
| Разные, включая оксиды, H2O и CO2 | +1,229 (в кислой среде) +0,401 (в щелочной среде) |
| O3 озон | Разные, включая кетоны и альдегиды | ||
| Пероксиды | 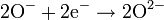
| Разные, включая оксиды, окисляет сульфиды металлов до сульфатов H2O | |
| Hal2 галогены | 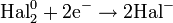
| Hal−; окисляет металлы, P, C, S, Si до галогенидов | F2: +2,87 Cl2: +1,36 Br2: +1,04 I2: +0,536 |
| ClO− гипохлориты | Cl− | ||
| ClO3− хлораты | Cl− | ||
| HNO3 азотная кислота | с активными металлами, разбавленная
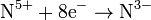 с активными металлами, концентрированная
с активными металлами, концентрированная
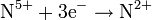 с тяжёлыми металлами, разбавленная
с тяжёлыми металлами, разбавленная
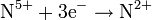 c тяжёлыми металлами, концентрированная
c тяжёлыми металлами, концентрированная
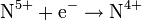
| NH3, NH4+ NO NO NO2 | |
| H2SO4, конц. серная кислота | c неметаллами и тяжёлыми металлами
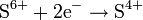 с активными металлами
с активными металлами
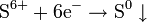
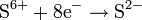
| SO2; окисляет металлы до сульфатов с выделением сернистого газа или серы S H2S | |
| Шестивалентный хром | 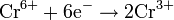
| Cr3+ | +1,33 |
| MnO2 оксид марганца(IV) | 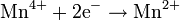
| Mn2+ | +1,23 |
| MnO4− перманганаты | кислая среда
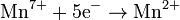 нейтральная среда
нейтральная среда
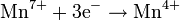 сильнощелочная среда
сильнощелочная среда
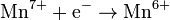
| Mn2+ MnO2 MnO42− | +1,51 +1,695 +0,564 |
| Катионы металлов и H+ | 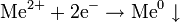
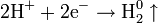
| Me0 H2 | см. Электрохимический ряд активности металлов |
- частицы (атом, молекула или ион), отдающие электроны, называются восстановителями.
Восстановителями могут быть:
1. Нейтральные атомы металлов и некоторые неметаллы (Znо, Mgо, Cо и др.)
2. Отрицательно заряженные ионы неметаллов (S-2, J-,…);
3. Положительно заряженные ионы металлов с низшей степенью окисления (Sn+2, Pb+2);
4. Сложные кислородосодержащие ионы с низшей степенью окисления (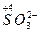 ,
, 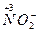 );
);
5. Катод.
Наиболее употребляемыми восстановителями на практике являются: C, CO, H2 , Zn, Ca, Mg, Al, Fe, H2S, Na, Na2S, Na2S2O3, HI, KI, HBr, HCl, SnCl2, NH3, альдегиды, спирты, муравьиная и щавелевая кислоты, глюкоза.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 294; Нарушение авторских прав?; Мы поможем в написании вашей работы!