
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 7. Физико-химические основы зарождения и роста новой фазы
Физико-химические основы зарождения и роста новой фазы
Анализ гомогенного и гетерогенного зарождения новой фазы
Пленки металлов, диэлектриков и полупроводников, осажденныена различные поверхности широко используютя в ЭС для изготовления резисторов, конденсаторов, транзисторов, ИМС, ПП, приборов на ПАВ и др.
Механизм процессов зарождения и роста пленок во многом определяет их кристаллическую структуру, а следовательно, и электрофизические, физико-химические, механические свойства. Т.к. пленки создаются на поверхности подложек при взаимодействии этих поверхностей с потоком частиц осаждаемых веществ то результатом такого взаимодействия является появление на поверхности подложки новой фазы.
Потоки частиц могут быть: молекулярнымиили ионными, в виде направленных пучков, потоков газовой и жидкой сред,движущиеся по законам газо- и гидродинамики, атакже в виде диффузионных потоков частиц. Процессы зарождения новой фазы могут протекать на границах различных фаз: жидкость — твердое тело, газ (пар) —твердое тело, твердое тело — твердое тело, композиционные пасты— твердое тело, жидкость — пар (газ).
Например, молекулярный пучок формируется испарением вещества и достигая поверхности конденсации (подложки), имеющей температуру значительно ниже температуры испарения, конденсируется на ней, образуя пленку. Если температура конденсации (подложки) ниже температуры плавления вещества, то сначала образуются зародыши твердой фазы, а затем и сама твердая пленка. Если температура конденсации близка к температуре плавления вещества или выше ее, то формируется жидкая пленка. Однако в любом случае исходным материалом для создания пленки является поток частиц (молекул или атомов) от испарителя к подложке. Причем испаритель является источником, а пленка стоком. Энергия этих частиц практически равна энергии испарения вещества.
В настоящее время существуют две теории гетерогенного образования зародышей конденсированной фазы: термодинамическая (макроскопическая) Гиббса — Фольмера и кинетическая (микроскопическая) Френкеля — Родина. Первая исходит из условий термодинамического равновесия в системе пар (газ) — зародыш — подложка. В ней используются такие термодинамические понятия, каксвободная и поверхностная энергии, степень перенасыщения и др. Такой подход оправдан при небольших перенасыщениях пара, когда критический зародыш состоит из большого числа атомов, а следовательно, к нему применимы термодинамические законы. Однако во многих реальных процессах, когда степень перенасыщения велика (108—1040), критический зародыш оказывается состоящим из одного атома. Описывать термодинамическими уравнениями столь малые агрегаты нельзя. В таком случае возможен лишь кинетический подход. Поэтому необходимо рассмотреть обе теории гетерогенного образования зародышей.
Если поток частиц формируется за счет образования ионной плазмы при катодном или другом каком-либо способе распыления, то этот поток имеет сложный состав (включая нейтральные атомы, ионы и электроны в различных пропорциях). Так как энергии этих частиц могут отличаться друг от друга, то и характер их взаимодействия с поверхностью подложки будет различным, что скажется на механизме зарождения и роста пленок.
При химическом осаждении пленок (например, из газовой фазы) характер взаимодействия частиц с поверхностью еще более усложняется. Процесс протекает в несколько стадий: 1)адсорбция взаимодействующих молекул на этой поверхности; 2) диффузия молекул; 3) химическая реакция исходных компонентов с появлением молекул осаждаемого вещества; 4)адсорбция этих молекул и выделение их в отдельную фазу на поверхности; 5) десорбция летучих продуктов реакции. Аналогичная картина наблюдается и при электрохимическом осаждении пленок из электролитов.
Рассмотрим механизм зарождения и роста пленок сделав две предпосылки: имеется наличие потока вещества, направленного к поверхности осаждения, и поверхность является теоретически чистой.
Процесс образования зародышей заключается в возникновении
и росте агрегатов молекул в результате последовательных бимолекулярных реакций по схеме

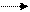

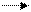

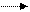

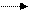 А1 + А 1 А 2, А 2 + А 1 А3, А 3 + А 1 А4, …, Аi + А 1 Аi+1,…, (195)
А1 + А 1 А 2, А 2 + А 1 А3, А 3 + А 1 А4, …, Аi + А 1 Аi+1,…, (195)
где A1…Ai - агрегаты, состоящие из i молекул (атомов).
i= 1,2,3, ….
Агрегат, содержащий i = i кp молекул, рассматривается как зародыш критического размера, который в общем случае растет или уменьшается. Другие механизмы образования зародышей (например, одновременного столкновения i кp молекул или нескольких агрегатов размерами меньше критического) считаются вероятными только для потока, имеющего высокую плотность (например, для импульсных процессов испарения).
Зародыш – это минимальное количество новой фазы, способное к самостоятельному существованию и находящийся в равновесии с окружающей исходной (маточной) фазой.
Разность химических потенциалов 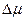 является движущей силой процессов фазовых переходов:
является движущей силой процессов фазовых переходов:
пар-кристалл 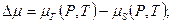
расплав-крисстал 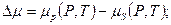
пар-жидкость 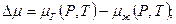
Появление и рост зародыша возможны, только когда химический потенциал новой фазы меньше химического потенциала исходной фазы.
Обычно для определения условий образования зародышей исползуют величины не 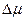 , а непосредственно измеряемые -
, а непосредственно измеряемые - 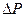 (пересыщение) и
(пересыщение) и 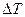 (переохлаждение) от их равновесных значений, отвечающих какой либо точке на кривых равновесия.
(переохлаждение) от их равновесных значений, отвечающих какой либо точке на кривых равновесия.
Абсолютное пересыщение – это разность парциального давления пара в газовой фазе и его равновесного давления при заданной температуре:
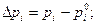
Относительное пересыщение – это отношение абсолютного пересыщения к равновесному давлению:
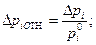
Коэффициент пересыщения 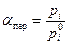 .
.
Условия образования зародышей для пересыщенного раствора в системе кристалл-раствор удобнее выражать через концентрации:
абсолютное пересыщение
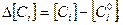
Относительное пересыщение – 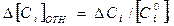
Коеффициент пересыщения - 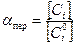 .
.
Системы расплав-кристалл характеризуются абсолютным переохлаждением:
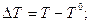
где 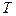 - фактическая температура расплава;
- фактическая температура расплава; 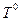 - равновесная температура (температура фазового перехода).
- равновесная температура (температура фазового перехода).
Для характеристики пересыщения применяется также безразмерный параметр 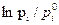 , который при умножении на кТ определяет разность химических потенциалов в газовой фазе в начальном и конечном состояниях:
, который при умножении на кТ определяет разность химических потенциалов в газовой фазе в начальном и конечном состояниях:
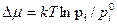
Образование сферического зародыша новой фазы, содержащего i кp молекул, сопровождается некоторым изменением свободной энергии ΔGi связанным с появлением определенной поверхности Sn и объема новой фазы V. В отсутствие полей и зарядов этот процесс можно описать уравнениями:
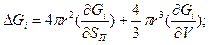
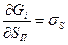 (196)
(196)
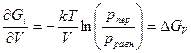 (197)
(197)
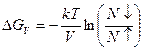 (198)
(198)
где r — радиус сферического зародыша, σs —поверхностная энергия, ΔGV — изменение свободной энергии при конденсации, практически равное энергии испарения, р пер — давление перенасыщенного пара, р равн—равновесное давление пара, соответствующее температуре конденсации Т; N↓- и N ↑ — число молекул, движущихся к поверхности конденсации и испаряющихся с нее.
Следовательно, уравнение (196) можно представить в виде
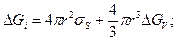
(199)
Зависимость ΔGi = f(r) для различных температур поверхности конденсации показана на рис. 12. Как видно из рисунка, свободная энергия ΔG i,- растет с увеличением r до значения ΔG кр [r= r кр (i = iкp)], а затем быстро убывает. Агрегаты радиусом r<. r кр считаются нестабильными, а радиусом r>rкр— стабильными зародышами новой фазы.
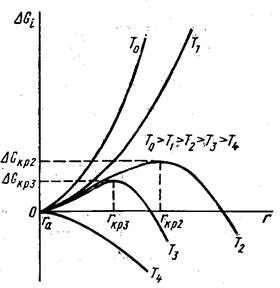 |
Рис. 12. Зависимость свободной энергии ΔGi от радиуса сферического зародыша r при различных температурах Т поверхности конденсации: rа – радиус одного атома
Последним соответствует уменьшение свободной энергии.
Определив максимум функции (199) из условия 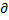 ΔGi/
ΔGi/ 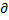 r=0, найдем радиус rкр:
r=0, найдем радиус rкр:
rкp= - 2σ s/ (ΔGV). (200)
Подставив значение rкр в (199), определим
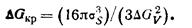 (201)
(201)
Соотношения (200) и (201) были впервые получены Дж. У. Гиббсом.
Для различных веществ rкр=1-50 нм.
Разделив объем критического зародыша на молекулярный Vm , получим число молекул
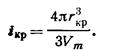 |
(202)
Из рис. 12 видно, что уравнение (169) справедливо в диапазоне температур от T1 до Т4. Вне этого диапазона теорию Гиббса — Фольмера использовать нельзя.
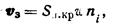 Скорость образования зародыша
Скорость образования зародыша
(203)
где S п.кp—площадь поверхности критического зародыша; w — частота столкновений молекул с этой поверхностью; ni-—число молекул на единице этой поверхности, т. е. равновесная поверхностная.концентрация молекул.
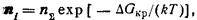 По изотерме Вант-Гоффа
По изотерме Вант-Гоффа
(204)
где n å -число молекул в паре
Согласно уравнению Герца — Кнудсена частота столкновений
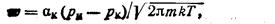 |
(205)
где α к — коэффициент конденсации; р и рк — давления насыщенных паров при температурах испарения и конденсации (т. е. испарителя и подложки). Следовательно, скорость образования зародышей,
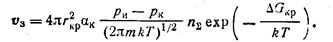 |
(206)
Уравнение (206) не учитывает ряда факторов. Например, не всякое столкновение молекулы с агрегатом ведет к ее конденсации и внедрению в агрегат. Поэтому выражение (206) следует умножить на равновесный фактор Z, учитывающий, какая доля из ударяющихся о поверхность молекул конденсируется.
Обычно
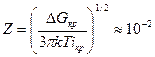 (207)
(207)
Таким образом,
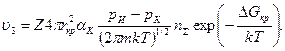 (208)_
(208)_
Все выкладки относятся к гомогенному образованию зародышей, которое редко реализуется на практике.
Модель гетерогенного образования зародышей отличается от гомогенной тем, что вводится геометрический фактор, определяемый межфазовыми взаимодействиями в системе подложка — зародыш— пар или подложка — зародыш — жидкость. Если свойства зародыша изотропны, то образуется куполообразный зародыш, если анизотропны — другие конфигурации зародышей (рис. 13). Геометрический фактор вводится в уравнение (199) в виде функций поверхности соприкосновения зародыша с соответствующими фазами и объема зародыша fs(φ) и fv(φ), зависящих от контактного угла φ (для жидкостей — угла смачивания):
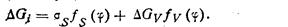 |
(209)
Эти функции описывают геометрическую конфигурацию зарот дыша. Значение φ определяется при равновесии поверхностных энергий:
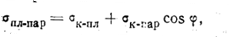 |
(210)
где 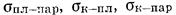 — удельные межфазовые поверхностные энергии поверхностей раздела пластина — пар, конденсат — пластина и конденсат— пар.
— удельные межфазовые поверхностные энергии поверхностей раздела пластина — пар, конденсат — пластина и конденсат— пар.
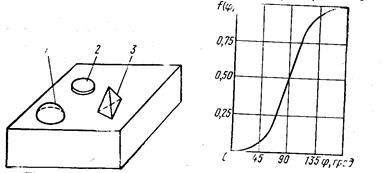
Рис.13. Конфигнурация зародышей Рис.14. Функция контактного
новой фазы: 1- куполообразный; угла f (φ) для куполообразного
2- дискообразный; 3- пирамидальный зародыша
Для куполообразного зародыша
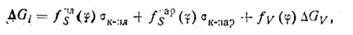
(212)
где fsпл (φ) —функция поверхности соприкосновения зародыша с пластиной fsпар (φ) —функция поверхности соприкосновения зародыша с паровой фазой.
Свободную энергию образования критического зародыша найдем из условия максимума уравнения (209):
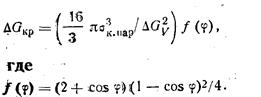 |
(213)
(214)
Функция контактного угла f(φ) для куполообразного зародыша (рис. 14) характеризует взаимодействие конденсата с пластиной. При φ→0 f(φ) →0, ΔGкр→0 и образование зародышей облегчается. При φ→180°, f(φ)→ -1, ΔGкpрастет до максимума и образование зародышей затрудняется (случай гомогенного зарождения новой фазы). Следовательно, уравнение (196) является предельным случаем образования зародышей, когда оно протекает с максимальной трудностью. Таким образом, свободная энергия гетерогенного меньше свободной энергии гомогенного образования зародышей. Кроме того, механизм гомогенного и гетерогенного образования зародышей (рис. 15) различен. При гомогенном образовании рост происходит только за счет реакции поверхности зародыша с паровой фазой (механизм v 3), при гетерогенном — за счет поверхностной диффузии (механизм v 2), т. е. v 2>> v 3. При очень низких температурах пластины v 3> v 2.
Скорость гомогенного образования зародышей в случае прямого осаждения из пара
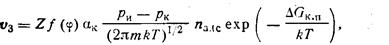 |
(215)
где n адc — концентрация молекул, адсорбированных на поверхности; ΔGк.п. — свободная энергия конденсации из пара.
Скорость образования зародышей при преобладании поверхностной диффузии
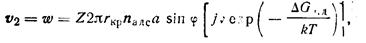 |
(216)
где а — длина скачка диффундирующей молекулы к поверхности зародыша; j — величина, обратная числу возможных направлений скачков; v — частота поверхностных колебаний; ΔGп.д—свободная энергия активации поверхностной диффузии;
jv exp(- ΔGп.д/kT) – частота скачков диффундирующей молекулы.
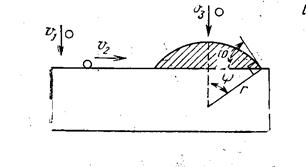 |
Рис.15. Образование куполообразного зародыша на поверхности пластины: v 1 – скорость молекул, движущихся к пластине; v 2 - скорость молекул, диффундирующих по поверхности пластины; v 3 - скорость молекул, движущихся к поверхности зародыша
При температурах пластины, позволяющих реализовать оба механизма образования зародышей, скорость образования зародышей равна сумме скоростей v2 и v 3:
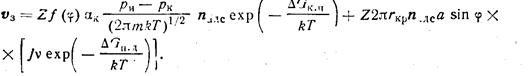 |
((217)
Для обычных условий осаждения пленок уравнение (217) удобно представить в виде
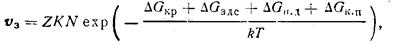 |
(218)
где К — константа, учитывающая размер критического зародыша и другие геометрические параметры; N — общее число частиц, участвующих в процессе образования зародышей.
Как видно из выражения (218), скорость образования зародышей существенно зависит от энергетических характеристик процесса, а следовательно, от условий осаждения. На рис. 16 показана логарифмическая зависимость скорости образования зародышей от скорости конденсации, характеризуемой степенью перенасыщения N↑ /N↓.
Рост критических (докритических) зародышей за счет поверхностной диффузии возможен только в случае, когда температура пластины достаточно высока (kT>>ΔG n.д .). При низких температурах диффузия атомов по поверхности мала и адсорбированные атомы можно считать локализованными. В этом случае рост зародыша происходит за счет прямого добавления атомов из пара (механизм v 3). Скорость образования зародышей определяют по (215).
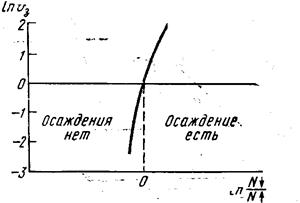 |
Рис.16. Логарифмическая зависимостьскорости образования зародышей v 3 от степени перенасыщения N↑/N↓
|
|
Дата добавления: 2014-01-03; Просмотров: 2832; Нарушение авторских прав?; Мы поможем в написании вашей работы!