
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Новые препараты
|
|
|
|
Г. Р. Парк (Кембридж, Великобритания)
Перед тем, как обсуждать новые препараты необходимо понять, в чем слабости старых. Хоть мы и используем их в течение многих лет, некоторые из их эффектов все еще плохо поняты. Надеемся, что строгие законы лицензирования новых препаратов и пытливый ум врачей отделений интенсивной терапии будут стимулировать более глубокое исследование новых лекарств и ответить на некоторые из стоящих вопросов по старым препаратам.
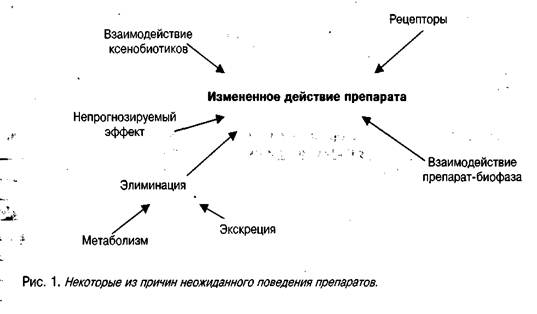
Изменение эффекта препарата может происходить по многим причинам, некоторые из них представлены на рисунке 1. Данный обзор не может охватить все аспекты, внимание будет сконцентрировано на элиминации новых и старых препаратов.
Метаболизм превращает жирорастворимые препараты в водорастворимые метаболиты. Активные препараты способны проходить через мембраны, они жирорастворимы. Их метаболиты выводятся с мочой и желчью, они водорастворимы.
Препараты обычно метаболизируются двумя путями, называемыми фаза 1 и фаза 2. Вмешательство в фазу 1 метаболизма изменяет выведение препарата. Промежуточные метаболиты могут быть высоко активными, например, продукт метаболизма парацетамола в фазу 1 NAPQI является почечным и печеночным ядом. Некоторые препараты (морфин, лоразепам) проходят метаболизм сразу через фазу 2 (рис. 2).
Метаболизм в фазу 1 зависит от работы ферментов. В этом процессе участвуют несколько групп ферментов, но наиболее важным среди них является цитохром Р450. У человека описано только около двадцати из них. Они являются критически важными для понимания действия седативных и анальгетических препаратов. Цитохром Р450 (CYP) 2Е1 является ферментом, отвечающим за метаболизм ингаляционных анестетиков. CYP ЗА4 метаболизирует многие препараты, используемые для седации и обезболивания критических больных. CYP 2D6 метаболизирует кодеин до морфина. Этот путь имеет различные фармакогенетические отклонения, а у 10% населения нормально не функционирует. В таблице 1 представлены некоторые препараты и цитохромы, участвующие в их метаболизме.
Рис. 2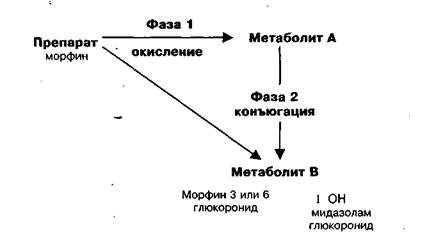
Таблица 1. Некоторые из препаратов, используемых в интенсивной терапии, цитохромы, участвующие в их метаболизме
| CYP1A | CYP2C | CYP2D6 | CYP3A | |
| Альфентанил | + | |||
| Карбамазепин | + | |||
| Циметидин | + | + | ||
| Кодеин | + | |||
| Диазепам | + | + | ||
| Дигоксин | + | |||
| Эритромицин | + | |||
| Мидазолам | + | |||
| Метранидазол | + | |||
| Парацетамол | + | + | ||
| Теофиллин | + | + | ||
| Варфарин | + | + | ||
Ферменты также могут находиться под влиянием различных состояний критических больных. Гипоксия, медиаторы воспаления, нарушения питания, характерные для таких пациентов, изменяют эффект ферментов. Применение других лекарств дополнительно изменяет их работу. Обычно они действуют как ингибиторы (флуконазол, эритромицин и даже пропофол), но в некоторых случаях действуют как стимуляторы (рифампицин, барбитураты). При всех этих условиях элиминация препаратов становится непредсказуемой.
Метаболиты сами по себе могут быть активными. Действие их может быть похоже на действие исходного препарата или совершенно отличаться от него. Например, продукт петидина норпетидин при почечной недостаточности может накапливаться и вызывать судорожные приступы. У морфина образуются два основных метаболита - морфин-3-глюкуронид (МЗГ) и морфин-6-глюкуронид (М6Г). Первый из них является вероятно антианальгетиком, в то время как второй - определенно анальгетик.
Когда впервые была описано действие метаболитов, это привело в замешательство, т.к. они считались веществами водорастворимыми, не способными проникать через мембраны, а значит не обладающими активностью. Carrupt et al. показали, что у основных метаболитов морфина МЗГ и М6Г может меняться конфигурация молекулы. Это позволяет ей в водной среде быть водорастворимой, а в присутствии липидов - жирорастворимой. Это явление было названо морфиновым молекулярным хамелеонизмом.
Опиоиды обладают широким спектром действия вне центральной нервной системы (рис. 3). Важность этих эффектов на исход неизвестна. Интересно, что естественные опиоиды (морфин, кодеин) были обнаружены в нормальном мозге млекопитающих. Они также оказывали влияние на почки, не характерное для синтетических аналогов. Морфин обладает выраженным влиянием на метаболизм препаратов, вероятно, через гормональный рост, но без участия опиоидных рецепторов. Синтетические опиоиды подобным эффектом не обладают.
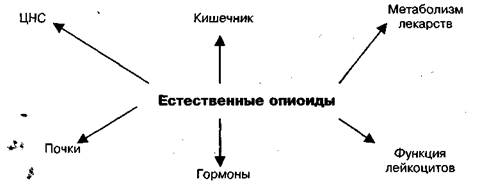
Рис.3 Периферические эффекты апиоидов
Новые препараты имеют менее активные метаболиты, чем те, что были у старых. Когда сравниваются метаболиты старого морфина, относительно нового мидазолама и новейшего опиоида ремифентанила, на каждом этапе получаем 100-кратное уменьшение метаболитной активности. Для новейших препаратов мало характерно появление продуктов метаболизма, способных накапливаться у критических больных с полиорганной недостаточностью.
Между этими тремя препаратами меняется важность различных путей элиминации. Морфин метаболизируется в фазу 2 и при заболеваниях печени может накапливаться. Его высоко активные метаболиты накапливаются при почечной недостаточности. Мидазолам у критических больных вследствие ферментной недостаточности может не мета-болизироваться. В обе фазы он продуцирует малоактивные соединения, которые при почечной недостаточности могут накапливаться. Метаболизм ремифентанила (нового ультра короткодействующего опиоида) происходит независимо от цитохрома Р450, а при участии эртераз крови и тканей. Благодаря их большому количеству ферментная эсте-разная недостаточность маловероятна. Даже в беспеченочный период трансплантации печени фармакокинетика ремифентанила не меняется. При почечной недостаточности образующиеся метаболиты могут накапливаться, однако, учитывая их слабость, на сегодняшний день считается, что они не могут оказать значительного влияния. Эти свойства делают ремифентанил очень предсказуемым.
Одним из основных негативных эффектов седативных и обезболивающих препаратов является депрессия дыхания. Новый препарат дексмедетомидин не обладает подобным действием. Он является сс2-агонистом, обладающим высокой специфичностью, благодаря чему сильнее клонидина в 8 раз. Этот препарат вызывает сон, из которого больного можно легко разбудить, обеспечивает обезболивание, анксиолизис, отсутствие депрессии дыхания. Препарат лицензирован в США, однако в Европе все еще не применяется.
Новые препараты не только обладают преимуществами для больного, но и могут принести экономическую выгоду. При использовании ремифентанила и дексмедетомидина уменьшается применение других седативных и обезболивающих препаратов.
Литература
1. Park, G. R. Molecular mechanisms of drug metabolism in the critically ill. British Journal of Anaesthesia 1996 77, 32-49..
2. Janicki PK, James MF, Erskine WA. Propofo/ inhibits enzymatic degradation of alfentanil and sufentanil by isolated liver m/crosomesin vitro. BrJ Anaesth 1992;68:311-2.
3. Chen, T. L, Ueng, T. H., Chen, S. H., Lee, P. H., Fan, S. Z., and Liu, C. C. Human cytochrome P450 mono-oxygenase system is suppressed by propofol. British Journal of Anaesthesia 74, 558-562.1995. Ref Type: Journal (Full)
4. Leung BP, Miller E, Park GR. The effect of propofol on midazolam metabolism in human liver microsome suspension. Anaesthesia 1997. AN 1997;52:945-8.
5. Gong QL, Hedner J, Bjorkman R, Hedner T. Morphine-3-glucuronide may functionally antagonize morphine-6-glucuronide induced antinociception and ventilatory depression in the rat. Pain 1992;48:249-55.
6. Smith MT, Watt J A, Cramond T. Morphine-3-glucuronide a potent antagonist of morphine analgesia. Life Sd. 1990;47:579-85.
7. Shelly MP, Cory EP, Park GR. Pharmacokinetics of morphine in two children before and after liver transplantation. Br J Anaesth 1986;58:1218-23.
8. Osborne RJ, Joel SP, Slevin ML Morphine intoxication in renal failure: the role of morphine-6- glucuronide. BMJ 1986;292:1548-9.
9. Carrupt PA, Testa B, Bechalany A, El Tayar N, Descas P, Perrissoud D. Morphine 6-glucuronide and morphine 3-glucuronide as molecular chameleons with unexpected lipophilicity. J Med Chem 1991;34:1272-5.
10. Wilkins M, Park GR. The peripheral effects of opioids. In Schulte am Esch J, Scholz J, Tonner PH, eds. Molecular Pharmacology of Anaesthesia, pp 172-90. Lengerich: PABST Science Publishers, 2000.
11. Waltz CJ, Lowney U, Faull KF, Feistner G. Morphine and codeine from mammalian brain. Proc Natl Acad Sci USA 1986;83:9784-8.
12. Dhasmana KM, Dixit KS, Dhawam Щ Gupta GP. Blockade of the depressor response of dopamine. Jpn J Pharmacol 1969; 19:168-9.
13. Rane, A., Liu, Z., Henderson, C. J., and Wolf, C. R. Divergent regulation of cvtochrome P450 enzymes by morphine and pethidine; a neuroendocrine mechanism? Molecular Pharmacology 47, 57-64.1995. Ref Type: Journal (Full)
14. Navapurkar VU, Archer S., Gupta SK, Muir KT, Frazer N, Park GR. Metabolism of remifentanil during liver transplantation. BrJ Anaesth 1998;81:881-6.
15. Bhana N, Goa KL, McOellan KJ, Dexmedetomidine. Drugs 2000;59:263-8.
16. Quintan, P., Fletcher, N., Royston, D., Farrimond, J., and Reidel, B. Propofol sparing effect of remifentanil when added to propofol for sedation in the intensive care unit. Intensive Care Medicine 26 (S3), 304. 2000.
17. Motsch, J., Bauer, M., Bottinger, B. W., Martin, E., and Bach, A. Cost effectiveness of dexmedetomidine for sedation in postoperative patients. Intensive Care Medicine 26 (S3), 306. 2000.
18. Soliman HM, Melot M, Vincent J-L. Sedative and analgesic practice in the intensive care unit: the results of a European survey. Intensive Care medicine 26 (S3) 303 2000
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 450; Нарушение авторских прав?; Мы поможем в написании вашей работы!