
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влажный пар и его параметры
|
|
|
|
Рассматривая влажный пар как механическую смесь сухого насыщенного пара и жидкости той же температуры, т. е. температуры насыщения, его объем можно представить как сумму объемов указанных компонентов. Непосредственно отсюда вытекает формула для определения удельного объема влажного пара
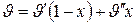 , (7.2)
, (7.2)
где х – степень сухости пара.
Здесь первое слагаемое представляет собой объем жидкости, содержащейся в 1 кг влажного пара, а второе – объем содержащегося в нем сухого насыщенного пара.
Для превращения 1 кг кипящей воды в сухой насыщенный пар при
p = const ему необходимо сообщить определенное и различное для разных давлений количество тепла, называемое теплотой парообразования. Эта величина обозначается буквой r и, как легко видеть, может быть определена по формуле
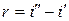 .
.
Часть теплоты парообразования расходуется на увеличение внутренней энергии, связанное с совершением работы против сил взаимного притяжения молекул. Она называется внутренней теплотой парообразования и обозначается буквой ρ.
Остальная часть теплоты парообразования расходуется на работу расширения, не связанную с наличием сил молекулярного взаимодействия и равную 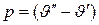 . Она называется внешней теплотой парообр азования. Таким образом, получаем
. Она называется внешней теплотой парообр азования. Таким образом, получаем
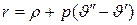 . (7.3)
. (7.3)
Внутренняя теплота парообразования всегда значительно больше внешней. Например, для воды при нормальном давлении по табличным данным из полной теплоты парообразования на долю внутренней приходится около 93%, а на долю внешней – только около 7 %.
Связь между теплотой парообразования и давлением может быть установлена следующим образом.
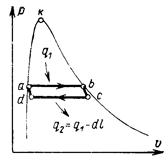
Рассмотрим элементарный цикл Карно a-b-c-d (рис. 7.6), в котором на участке a-b давление рн и температура Тн постоянны, а на участках b-c и d-a они изменяются соответственно на dpн dTн. Точка а лежит на нижней пограничной кривой, а точка b – на верхней, поэтому тепло, подводимое на участке a-b, равно теплоте парообразования при давлении рн, т.е. q1= r, работа же данного цикла 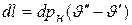 .
.
 Таким образом, для термического к.п.д. рассматриваемого цикла можно написать выражения
Таким образом, для термического к.п.д. рассматриваемого цикла можно написать выражения
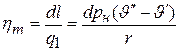
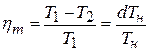
Приравнивая правые части этих выражений, находим

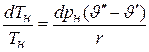
и окончательно
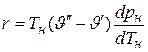 . (7.4)
. (7.4)

 Полученное выражение называется уравнение Клапейрона–Клаузиуса. Оно позволяет вычислить величину r, если зависимость
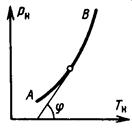
Полученное выражение называется уравнение Клапейрона–Клаузиуса. Оно позволяет вычислить величину r, если зависимость 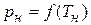 известна из опыта. Нетрудно видеть, что если эта зависимость графически выражается линией АВ (рис. 7.7), то производная определяётся как угловой коэффициент касательной к этой кривой в заданной точке, т. е.
известна из опыта. Нетрудно видеть, что если эта зависимость графически выражается линией АВ (рис. 7.7), то производная определяётся как угловой коэффициент касательной к этой кривой в заданной точке, т. е.
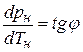 .
.
С помощью теплоты парообразования r энтальпия влажного пара легко определяется следующим образом. В процессе парообразования при p= const
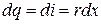
где х– степень сухости влажного пара.
Интегрируя это выражение, получаем:
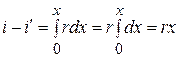 ,
,
откуда
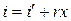 . (7.5)
. (7.5)
Энтропия влажного пара может быть определена по формуле (5.10), из которой получаем
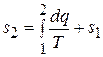 ,
,
а для данного случая
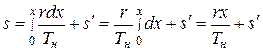 , (7.5/)
, (7.5/)
где Тн– температура кипения при заданном постоянном давлении.
Для сухого насыщенного пара х=1, поэтому
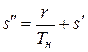 ,
,
откуда получаем
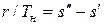 .
.
Формула (7.5/) может быть записана так
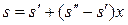 . (7.6)
. (7.6)
Пользуясь приведенными формулами и зная степень сухости пара, можно определить все основные параметры и для влажного пара.
7.5 Ts– диаграмма водяного пара
Рассмотрим характер и расположение изобар воды и водяного пара в Ts-диаграмме.
Изменение энтропии воды в обратимом изобарном процессе находится по общей формуле (5.9)
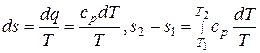 .
.
Полагая, что изобары при любом давлении начинаются от температуры тройной точки ТА=Т0, при которой энтропия равна s0, получаем зависимость
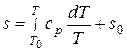 , (7.7)
, (7.7)
которая является уравнением изобары воды в Ts-диаграмме в самом общем виде.
Принимая приближенно, что для всех давлений sо=0, получаем
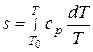 (7.8)
(7.8)
В области жидкого состояния при невысоких давлениях можно считать cp=const, тогда
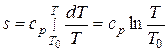 . (7.9)
. (7.9)
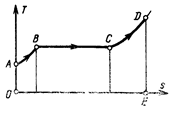 Таким образом, изобара воды представляет собой экспоненциальную кривую, начинающуюся на оси ординат в точке А при температуре То и кончающуюся в точке В при температуре кипения Тн и энтропии s/(рис. 7.8).
Таким образом, изобара воды представляет собой экспоненциальную кривую, начинающуюся на оси ординат в точке А при температуре То и кончающуюся в точке В при температуре кипения Тн и энтропии s/(рис. 7.8).
 В области влажного пара T=Тн=const, поэтому изобара имеет вид горизонтальной прямой ВС, конечная точка которой С соответствует состоянию сухого насыщенного пара, когда энтропия равна s".
В области влажного пара T=Тн=const, поэтому изобара имеет вид горизонтальной прямой ВС, конечная точка которой С соответствует состоянию сухого насыщенного пара, когда энтропия равна s".
В области перегретого пара уравнение изобары принимает вид
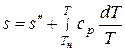 , (7.10)
, (7.10)
где ср – истинная теплоемкость перегретого пара.
В точке С изобара имеет излом (поскольку ср, будучи бесконечно большой для влажного пара, при переходе в область перегретого пара принимает конечное значение) и превращается в кривую СD.
Крутизна этой кривой изменяется в зависимости от ср. Действительно, из дифференциального соотношения
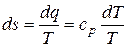
следует, что угловой коэффициент касательной к изобаре перегретого пара
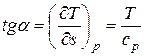 .
.
На начальном участке вблизи состояния насыщения ср для перегретого пара велика, поэтому изобара идет полого. По мере удаления от точки С величина ср уменьшается и крутизна изобары возрастает, а на достаточно большом расстоянии от нее, когда зависимость ср от температуры становится незначительной, изобара по характеру приближается к экспоненциальной кривой.
Изображение изобары воды и водяного пара в Ts-диаграмме позволяет представить графически их энтальпию. Так, например, площадь, заключенная между отрезком изобары АВ и осью абсцисс, представляет собой теплоту кипящей воды. Если с небольшой погрешностью пренебречь энтальпией воды при температуре тройной точки, то на основании формулы (4.6) эту площадь можно считать равной и энтальпии i /. Равным образом площадь, заключенная между отрезком изобары АВС и осью абсцисс, равна энтальпии i", причем площадь прямоугольника, расположенного между отрезком ВС и осью абсцисс, равна теплоте парообразования r.
Аналогично этому в виде площади можно представить себе энтальпию некипящей воды, влажного пара и перегретого пара. Во всех случаях она изображается площадью, заключенной между отрезком изобары от оси ординат до заданной точки и осью абсцисс. Например, если состояние перегретого пара характеризуется точкой D, то его энтальпия равна площади фигуры ОАВСDЕО.
Отправляясь от упрощающих предпосылок, что при всех давлениях sо=0 и для воды cр не зависит от давления, а является функцией лишь температуры, в Тs – диаграмме можно изобразить целую систему изобар, начиная от изобары
 ра =0,006112 бар и кончая изобарой ркр = 221,15 бар (рис. 7.9).Изобара воды ркр, изображаемая линией АК, на нижнем участке, где теплоемкость можно считать постоянной, имеет экспоненциальный характер. При более
ра =0,006112 бар и кончая изобарой ркр = 221,15 бар (рис. 7.9).Изобара воды ркр, изображаемая линией АК, на нижнем участке, где теплоемкость можно считать постоянной, имеет экспоненциальный характер. При более 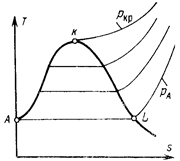 высоких температурах, когда ср начинает возрастать, она становится менее крутой и, наконец, в критической точке, когда ср= ∞, приобретает горизонтальное направление, имеет перегиб и плавно переходит к изобару перегретого пара.
высоких температурах, когда ср начинает возрастать, она становится менее крутой и, наконец, в критической точке, когда ср= ∞, приобретает горизонтальное направление, имеет перегиб и плавно переходит к изобару перегретого пара.
Как видно из графика, изобары воды для других, более низких давлений на всем своем протяжении сливаются с изобарой ркр, заканчиваясь при соответствующей температуре кипения и переходя в изобару влажного, а затем перегретого пара. По мере снижения давления теплота парообразования возрастает. Поэтому длина горизонтального участка, соответствующего области влажного пара, увеличивается.
Изобара рА начинается непосредственно с горизонтального участка АL, соответствующего парообразованию при температуре тройной точки, а затем продолжается в области перегретого пара в виде кривой, близкой по характеру к экспоненте уже в самом начале.
Все точки, соответствующие состоянию кипящей воды, в такой диаграмме размещаются на линии АК, т. е. на изобаре ркр, которая, следовательно, является и нижней пограничной кривой. Более того, на этой же изобаре лежат и все без исключения точки, соответствующие состоянию некипящей воды при разных давлениях, поэтому вся область жидкого состояния в такой диаграмме представляет собой не площадь, а линию, совпадающую с нижней пограничной кривой.
Все точки, соответствующие состоянию сухого насыщенного пара, образуют плавную кривую КL, которая, таким образом, является верхней пограничной кривой. По форме она почти симметрична линии АК., но в точке L не заканчивается, а продолжается вниз, отделяя область двухфазного состояния лед – насыщенный пар от области перегретого пара. С точки зрения паротехники этот участок ее интереса не представляет, ибо он располагается в области весьма низких давлений и температур.
Из-за упрощающих предпосылок график на рис. 7.9 имеет приближенный характер. Особенно существенно в нем искажаются изобары воды, что тем более заметно, чем выше давление. В связи с этим рассмотрим расположение изобар воды в Ts– диаграмме подробнее.
Для этого удобно использовать уравнение Максвелла (6.14), которое показывает, что изменение энтропии с давлением при постоянной температуре противоположно по знаку изменению удельного объема с температурой при постоянном давлении.
Вода при нагревании расширяется, следовательно, энтропия ее с повышением давления при постоянной температуре уменьшается. Это означает, что изобары воды в Ts –диаграмме в действительности не сливаются с нижней пограничной кривой, а располагаются левее ее, тем дальше, чем выше давление.
Вопрос о взаимном расположении этих изобар на начальном участке осложняется известной аномалией воды, температура наибольшей плотности которой в широком диапазоне давлений (примерно до 300 бар) несколько выше 0°С. Например, при нормальном давлении она равна 3,98 °С. В связи с этим изобары воды начинаются ниже начала нижней пограничной кривой (тем дальше от него, чем выше давление), пересекают ее на участке от 0 до 4°С, а затем отходят от нее, тем дальше, чем выше давление.
Естественно, что в докритической области давлений изобары в верхней своей части вновь приближаются к нижней пограничной кривой и заканчиваются на ней тем выше, чем выше давление.
В диапазоне давлений примерно от 300 до 500 бар начало изобар с повышением давления смещается вверх и при давлении около 500 бар совмещается с началом нижней пограничной кривой, а при еще более высоких давлениях изобары начинаются уже выше него, тем дальше, чем выше давление. Например, изобара, соответствующая давлению 1 000 бар, начинается на оси ординат при температуре около 0,2 °С.
Для иллюстрации на рис. 7.10 показаны в крупном масштабе начальные участки нижней пограничной кривой и нескольких изобар в сверхкритической области давлений.

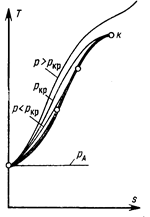
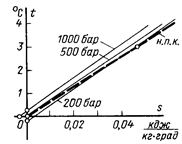 Учитывая, что при температуре тройной точки энтропия воды для давлений до 650 бар очень мала и не превышает по абсолютной величине 0,0012 кДж/(кг·град), с достаточной для современной паротехники точностью аномалией воды можно пренебречь и считать, что начало всех изобар совпадает с началом нижней пограничной кривой, как показано на рис. 7.11. Изобары располагаются левее нижней пограничной кривой, тем дальше от нее, чем выше давление и температура. При сверхкритических давлениях изобары минуют нижнюю пограничную кривую, оставляя ее справа и постепенно принимая вид экспоненциальных кривых, как у идеального газа.
Учитывая, что при температуре тройной точки энтропия воды для давлений до 650 бар очень мала и не превышает по абсолютной величине 0,0012 кДж/(кг·град), с достаточной для современной паротехники точностью аномалией воды можно пренебречь и считать, что начало всех изобар совпадает с началом нижней пограничной кривой, как показано на рис. 7.11. Изобары располагаются левее нижней пограничной кривой, тем дальше от нее, чем выше давление и температура. При сверхкритических давлениях изобары минуют нижнюю пограничную кривую, оставляя ее справа и постепенно принимая вид экспоненциальных кривых, как у идеального газа.

7.6 is – диаграмма водяного пара
Аналитические расчеты процессов водяного пара с помощью табличных данных, часто осложняются возможностью фазовых переходов при изменении его состояния (например, превращения перегретого пара во влажный или наоборот). Соотношения между параметрами пара в различных его фазах выражаются разными формулами, поэтому, исследуя какой-либо процесс, приходится прежде всего выяснять, не происходит ли в нем переход пара из одной фазы в другую, что зачастую связано с громоздкими вычислениями.
В связи с этим в паротехнике широко применяется графический метод расчета, в котором используется is – диаграмма.
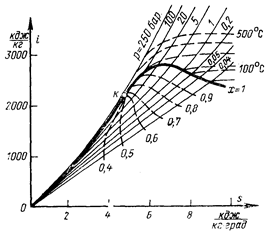
Построение этой диаграммы, общий вид которой приведен на рис. 7.12, осуществляется таким образом.
По табличным значениям 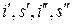 строятся нижняя и верхняя пограничные кривые ОК. и КL, затем точки на этих кривых, соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами.
строятся нижняя и верхняя пограничные кривые ОК. и КL, затем точки на этих кривых, соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами.
 Действительно, из уравнения
Действительно, из уравнения
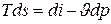
при p= const получаем
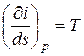 .
.
Но частная производная в левой части полученного уравнения представляет собой угловой коэффициент касательной к изобаре, а поскольку температура в изобарном процессе влажного пара постоянна и равна температуре кипения Тн, постоянным будет и этот коэффициент, т. е. изобара изображается прямой линией.
С увеличением давления температура Тн повышается, поэтому изобары становятся более крутыми и вся совокупность их образует пучок расходящихся кверху прямых.
В области перегретого пара изобары строятся по точкам, наносимым в соответствии с табличными значениями параметров i и s для разных температур. По мере удаления от верхней пограничной кривой температура пара возрастает, поэтому крутизна изобар увеличивается, т. е. за этой кривой они теряют прямолинейный характер и плавно изгибаются кверху.
Изотермы в области перегретого пара строятся по тем же точкам, которые были нанесены для построения изобар. При этом оказывается, что на верхней пограничной кривой они имеют излом, расходятся с изобарами и идут вначале с некоторым подъемом (тем более крутым, чем выше давление насыщения), а затем, по мере удаления от пограничной кривой, принимают почти горизонтальное направление.
Такое расположение изотерм объясняется тем, что вблизи состояния насыщения водяной пар существенно отличается от идеального газа и у него при изотермическом расширении внутренняя энергия не остается постояной, а возрастает за счет потенциальной составляющей, связанной с наличием сил взаимного притяжения. Как видно из диаграммы рυ = р, изображенной на рис. 6.3, возрастает и произведение рυ, а следовательно, энтальпия 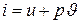 и увеличивается. По мере удаления от состояния насыщения водяной пар приближается по своим свойствам к идеальному газу, для которого энтальпия является функцией одной лишь температуры, поэтому вдали от верхней пограничной кривой изотермы и приближаются по характеру к горизонтальным прямым.
и увеличивается. По мере удаления от состояния насыщения водяной пар приближается по своим свойствам к идеальному газу, для которого энтальпия является функцией одной лишь температуры, поэтому вдали от верхней пограничной кривой изотермы и приближаются по характеру к горизонтальным прямым.
Обращает на себя внимание положение критической точки, которая в is-диаграмме смещена влево и вниз. Это связано с уменьшением энтальпии сухого насыщенного пара по мере приближения его давления к критическому, объясняемого резким падением теплоты парообразовния, которая в критической точке становится равной нулю.
В области влажного пара наносится система линий постоянной степени сухости (x= const). Построение их основано на том, что каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки, в чем нетрудно убедиться, используя формулу
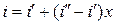 .
.
Обычно на is-диаграмму наносится и система изохор υ= const, которые по своему характеру близки к изобарам, но идут несколько круче и в области влажного пара не прямолинейны.
Нижняя часть is – диаграммы практического интереса не представляет и ее не строят: это дает возможность выполнить рабочую часть диаграммы в более крупном масштабе, удобном для пользования.
Впервые is – диаграмма водяного пара была построена Молье в 1906г. для давлений до 20 ат. В настоящее время применяется is –диаграмма Вукаловича, построенная для давлений до 1 000 бар и температур до 1000°С.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 5159; Нарушение авторских прав?; Мы поможем в написании вашей работы!