
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние рН на скорость ферментативной реакции
|
|
|
|
Важным фактором, оказывающим влияние на скорость ферментативной реакции, является рН среды. Для каждого фермента существует оптимальное значение рН, т.е. такая величина рН, или зона рН, при которой катализируемая ферментом реакция протекает с наибольшей скоростью.
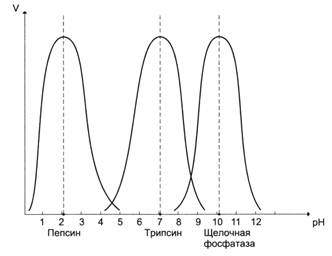
Большинство ферментов имеют максимальную каталитическую активность в зоне рН около 7; в резко кислой (пепсин при рН=2) или резко щелочной среде (щелочная фосфатаза, аргиназа рН = 10,0).
За пределами оптимальной зоны рН, т.е. при отклонениях в сторону снижения или в сторону повышения от этого значения, скорость ферментативной реакции снижается.
При изменении pH от оптимальных значений происходит изменение иони- зации функциональных групп белковой молекулы фермента. Например, при закислении среды происходит протонирование свободных аминогрупп (NH3+), а при защелачивании происходит отщеплен протона от карбоксильных групп (СОО-). Это приводит к изменению конформации молекул фермента и конформации активного центра, следовательно, нарушается присоединение субстрата, кофакторов и коферментов к активному центру. При значительном отклонении от оптимального значения pH может происходить денатурация белковой молекулы с полной потерей ферментативной активности.
6.6. Влияние на каталитическую активность ферментов ингибиторов и активаторов
Скорость ферментативной реакции (равно активность ферментов) определяется присутствием в среде ингибиторов и активаторов, среди которых могут быть как посторонние для организма вещества, так и природные продукты обмена.
И н г и б и т о р а м и называют вещества, вызывающие частичное или полное торможение химических реакций, включая и ферментативные.
Ферменты теряют каталитическую активность при воздействии различных факторов, вызывающих денатурацию (нагревание, кислоты, щелочи, соли тяжелых металлов и др.). Подобное разрушение фермента не рассматривается как ингибирование, так как оно не связано с механизмом действия фермента. Ингибиторы действуют на скорость реакции определенным химическим путем.
Механизм действия ингибиторов может быть самым разнообразным, но в общей форме можно сказать, что ингибитор вступает в соединение с ферментом, образуя соединение фермент-ингибитор.
Различают о б р а т и м о е и н е о б р а т и м о е ингибирование фермента.
- При обратимом ингибировании активность фермента восстанавливается по мере удаления свободного ингибитора диализом или иным способом, т.е. при обратимом ингибировании существует равновесие между свободным ингибитором и ферментом.
- При необратимом ингибировании равновесие между свободным ингибитором и ферментом не устанавливается и активность фермента не удается восстановить диализом. Напротив, если ингибитор присутствует в избытке по сравнению с ферментом, то со временем наступает полное торможение активности фермента.
Обратимое ингибирование ферментативных реакций бывает к о н к у р е н т н ы м и н е к о н к у р е н т н ы м.
Конкурентное ингибирование может быть вызвано веществами, похожими по своей структуре на субстрат. Эти вещества, конкурируя с субстратом, соединяются с активным центром фермента, но не подвергаются ферментативному превращению и новые продукты из них не образуются. В связи с тем, что часть фермента при конкурентном ингибировании расходуется на образование комплеса фермент-ингибитор, скорость ферментативной реакции снижается. Конкурентное ингибирование обратимо, так как при увеличении концентрации субстрата скорость реакции возрастает.
Неконкурентное ингибирование вызывают вещества, не имеющие структурного сходства с субстратом. Причем эти вещества обратимо присоединяются к ферменту не в активном центре, где обычно связывается субстрат, а совсем в другом месте и, следовательно, конкуренция между субстратом и ингибитором отсутствует. Неконкурентные ингибиторы связываются обратимо как со свободным ферментом, так и с фермент-субстратным комплексом, образуя неактивные фермент-ингибитор (ЕJ) и (или) фермент-субстрат-ингибитор (ESJ).
Наряду с ингибиторами существует целый ряд активаторов ферментов.
А к т и в а т о р а м и называют вещества, увеличивающие каталитическую активность ферментов. Среди активаторов встречаются самые разнообразные вещества. Особенно часто роль активаторов ферментов выполняют ионы металлов: калия, кальция, магния, цинка, меди, железа, марганца, кобальта, а из анионов - хлора. Для проявления максимальной активности ферментов требуется определенная концентрация ионов-активаторов в среде.
Усиление активности ферментов под действием ионов металлов объясняется тем, что в одних случаях ионы металлов выполняют роль кофактора, в других - облегчают образование фермент-субстратного комплекса, в третьих - способствуют присоединению кофермента к апоферменту, в четвертых обеспечивают становление четвертичной структуры фермента или же действуют иными путями.
Мощное действие на ферменты оказывают вещества, присоединяющиеся к ним в особых участках, удаленных от активного центра, называемых а л л о с т е р и ч е с к и м ц е н т р о м. Эти вещества влияют на активность фермента, вызывая обратимое изменение в структуре его активного центра. Называют такие вещества а л л о с т е р и ч е с к и м и э ф ф е к т о р а м и. Если эти эффекторы увеличивают сродство фермента к субстрату, то их называют а л л о с т е р и ч е с к и м и активаторами, если уменьшают - а л л о с т е р и ч е с к и м и ингибиторами. Ферменты, активность которых регулируется аллостерическими активаторами или ингибиторами называют а л л о с т е р и ч е с к и м и. Большинство аллостерических ферментов представляют собой белки-олигомеры.
Аллостерические ферменты имеют важное значение в регуляции ферментативных процессов в клетке. Это связано с тем, что эффекторами могут быть различные промежуточные продукты обмена веществ, называемые м е т а б о л и т а м и.
7. Номенклатура и классификация ферментов.
В настоящее время известно более 2400 ферментов. Каждый фермент, как правило, имеет две номенклатуры; одна из них рабочая (тривиальная), а другая - систематическая.
Рабочее наименование фермента составляют путем прибавления к корню слова латинского, греческого или химического названия субстрата, на который действует фермент, или к названию процесса, катализируемого данным ферментом окончания “-аза”. Вещество, имеющее это окончание, является ферментом.
Фермент, действующий на крахмал (amylum), называется – амилаза;
на сахарозу - сахараза, на мочевину (urea) - уреаза; на пептиды – пептидаза.
Ферменты, катализирующие процессы гидролиза называют - гидролазами, процессы окисления - оксидазами, перенос групп - трнсферазами и т.д.
Есть исключения: для некоторых ферментов сохранены названия, не подчи-няющиеся этому правилу: пепсин, трипсин, химотрипсин и др.
В названии ряда ферментов указывают как характер субстрата, так и тип катализируемой реакции. Фермент, катализирующий отнятие водорода от спирта, называют алкогольдегирогеназа.
Рабочим названием ферментов пользуются в повседневной практике.
В 1961 г. Международная комиссия по ферментам, созданная в 1956 г., предложила новую схему номенклатуры и классификации ферментов, которая была принята Международным биохимическим союзом. Согласно этой схемы каждый фермент имеет как рекомендуемое (рабочее) название, так и систематическое название, которое составляется в определенном порядке и подчеркивает тип катализируемой реакции (см. классы ферментов).
В принятой классификации все ферменты на основании катализируемых реакций разделены на шесть классов, расположенных в следующем порядке:
1) оксидоредуктазы, 2) трансферазы,
3) гидролазы, 4) лиазы,
5) изомеразы, 6) лигазы (синтетазы).
Каждый класс подразделяется на подклассы, а каждый подкласс - на подподклассы. Индивидуальный фермент имеет кодовое число (шифр) со стоящими перед ним буквами КФ (англ. ЕС). Шифр каждого фермента содержит четыре числа, разделенных точками. Первое число указывает к какому из шести классов принадлежит данный фермент. Второе число обозначает подкласс. Третье число обозначает подподкласс, а четвертое - порядковый номер фермента в данном подподклассе. Например, фермент КФ.1.1.1.1 имеет рекомендуемое (рабочее) название алкогольдегидрогеназа, систематическое название алкоголь:НАД оксидоредуктаза. Этот фермент относится к классу оксидоредуктаз (1), действует на СН-ОН группу доноров водорода (1.1), акцептором водорода служит НАД (1.1.1); четвертая цифра шифра - порядковый номер фермента в пределах подподкласса.
8. Классы ферментов и их отдельные представители
8.1.Оксидоредуктазы(1)
К классу оксидоредуктаз принадлежат все ферменты, катализирующие окислительно-восстановительные реакции. Субстрат, подвергающийся окислению рассматривается как донор водорода. Систематическое название составляется по типу “донор:акцептор оксидоредуктаза”. Термины “донор” и “акцептор” введены потому, что происходит реакция переноса двух восстановительных эквивалентов в той или иной форме (атомов водорода, электронов, гидрид-ионов и т.д.) от одного субстрата (окисляемого) к другому (восстанавливаемому).
В зависимости от природы окисляемых групп в молекуле донора оксидоредуктазы разделили на 19 подклассов. Деление на подподклассы произведено в зависимости от природы акцепторов, которыми могут быть кофермент (НАД или НАДФ), цитохром, молекулярный кислород и т.д.
Рекомендуемое название включает следующие термины. Оксидоредуктазы всех подподклассов, для которых акцептором водорода служит любое соединение, но не кислород, называют дегидрогеназами, а в случаях, когда донор водорода точно не установлен, используют термин редуктаза. Если акцептором служит кислород, то ферменты, катализирующие перенос водорода на него, называют оксидазами. Реакции прямого включения кислорода в молекулу органического субстрата катализируют оксигеназы; при этом происходит включение либо двух атомов кислорода (диоксигеназы), либо одного атома кислорода (монооксигеназы). Термин пероксидаза относится к ферментам, использующим в качестве окислителя пероксид водорода.
Многие дегидрогеназы в качестве акцептора водорода используют коферменты НАД (никотинамид-аденин-динуклеотид) и НАДФ (никотинамид-аденин-динуклеотид-фосфат), содержащие в своих молекулах производное пиридина - никотинамид. В связи с чем эти ферменты получили название пиридиновых (пиридинзависимых) дегидрогеназ, или пиридин-протеинов. Приводим структурную формулу окисленной формы НАД и НАДФ (обозн. НАД+ и НАДФ+).
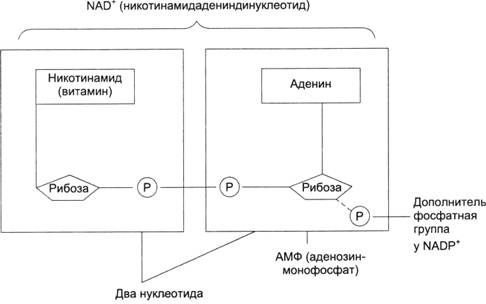
|
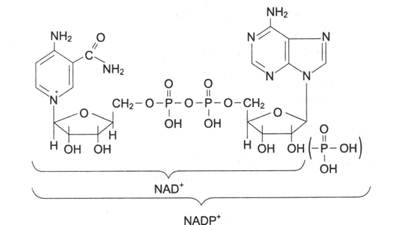
Пиридиновые дегидрогеназы отнимают от своих субстратов по два водородных атома. Один из них в виде гидрид-иона (Н-) присоединяется непосредственно к пиридиновому кольцу НАД+ или НАДФ+, а второй в виде Н+-иона переходит в среду.
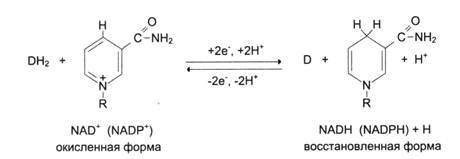
(Восстановленная форма нуклеотидных коферментов обозначается НАД·Н + Н+ (сокр. НАД·Н) и НАДФ·Н+Н+ (сокр. НАДФ·Н).
Восстановительные эквиваленты от НАД·Н расходуются для запаса энергии в виде АТФ, а от НАДФ·Н для восстановительных этапов процессов биосинтеза.
Наряду с пиридиновыми дегидрогеназами в окислительно-восстановительных реакциях участвуют флавиновые (флавинзависимые) дегидрогеназы, или флавопротеины. Такое название эти ферменты получили в связи с тем, что в качестве простетической группы (прочно связанного с белковой частью кофермента) содержат флавин-моно-нуклеотид (ФМН) или флавин-аденин-динуклеотид (ФАД):
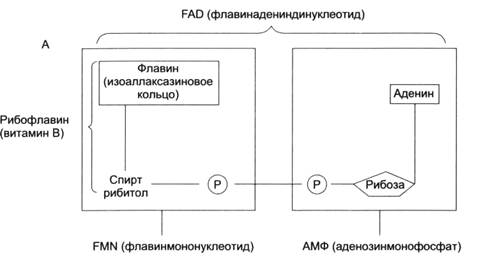
|
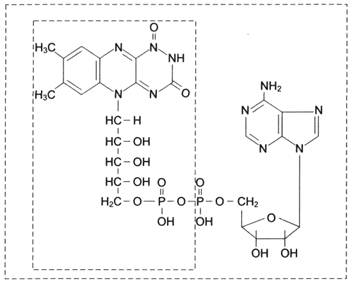















 Большинство флавиновых дегидрогеназ содержит в своем составе ФАД.
Большинство флавиновых дегидрогеназ содержит в своем составе ФАД.
Катализ окислительно-восстановительных реакций флавиновыми дегидрогеназами обусловлен последовательным окислением и восстановлением изоаллоксазинового кольца рибофлавина:
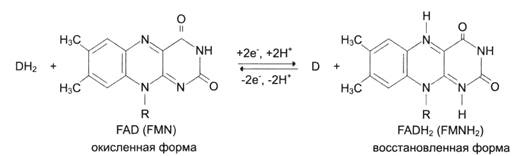
К а т а л а з а (КФ 1.11.1.6; пероксид водорода: пероксид водорода оксидоредуктаза) катализирует следующую реакцию:
 Н2О2 + Н2О2----> 2Н2О + О2
Н2О2 + Н2О2----> 2Н2О + О2
Каталаза - двухкомпонентный фермент, простетической группой которого является гематин, представляющий протопорфирин, содержащий атом трехвалентного железа.Этот фермент широко распространен в природе и найден у животных, растений, аэробных бактерий. Роль каталазы в организме связывают с расщеплением образующегося в процессе окисления ядовитого для клеток пероксида водорода.
Следующий фермент этого подкласса п е р о к с и д а з а (КФ 1.11.1.7; донор:пероксид водорода оксидоредуктаза). Пероксидаза содержится в тканях животных и растений, молоке, лейкоцитах, некоторых бактериях; катализирует окисление фенолов, аминов, некоторых гетероциклических соединений (например, индола) по схеме:
д онор + 2Н2О2--> окисленный донор + 2 Н2О.
онор + 2Н2О2--> окисленный донор + 2 Н2О.
Пероксидаза - двухкомпонентный фермент, ее простетическая группа представлена гематином. Гематин каталазы и пероксидазы имеет одинаковое строение. Следовательно, различия в каталитической функции этих ферментов определяются исключительно белковой частью.
Пероксидаза играет важную роль в дыхании растений. В молочной промышленности реакцию на пероксидазу используют для контроля эффективности пастеризации молока (пероксидаза молока инактивируется при температуре около 80ОС). Реакцию на пероксидазу применяют для оценки свежести мяса птицы. Свежее мясо дает положительную реакцию; мясо подозрительной свежести - отрицательную.
Ц и т о х р о м н а я с и с т е м а. Эта система состоит из цитохромов и фермента цитохромоксидазы. Цитохромы принадлежат к сложным белкам; их железопорфириновая простетическая группа, называемая гем, по своему строению очень близка к простетической группе гемоглобина (см. хромопротеины). Все известные цитохромы в зависимости от природы гема разделены на четыре группы: а, в, с и d.
Цитохромы - переносчики электронов в процессах окисления и восстановления. Они обнаружены во всех аэробных клетках. В ходе переноса электронов железо простетической группы цитохромов попеременно переходит из ферриформы [Fе (III)] в ферроформу [Fе (II)], содержит два атома меди.
8.2. Т р а н с ф е р а з ы (2)
К классу трансфераз принадлежат ферменты, катализирующие перенос различных остатков или групп от одного соединения, расматриваемого как донор группы (остатка), к другому соединению, рассматриваемому как акцептор.
В зависимости от характера переносимых остатков (одноуглеродные, альдегидные и кетонные, ацильные, гликозильные и др.) или групп (содержащие азот, фосфор или серу) класс разделили на восемь подклассов. Подклассы выделены в зависимости от химической природы переносимых групп (например, одноуглеродный остаток может быть метилом, формилом или карбоксилом; гликозильный остаток - гексозилом или пентозилом и т.п.).
Среди трансфераз имеются ферменты, катализирующие реакции с элементами синтеза. Чтобы подчеркнуть элемент синтеза в катализируемой реакции, для названия таких ферментов (как и фермент других классов, кроме синтетаз) применяют термин “ синтаза “. Рассмотрим некоторые из таких ферментов.
Г л и к о г е н (крахмал) - с и н т а з а (КФ 2. 4.1.11; УДФглюкоза: гликоген 4-a-глюкозилтрансфераза) катализирует следующию реакцию:
УДФглюкоза + (1,4-a-D-глюкозил)n ® (1.4-a-D-глюкозил)n+1 + 1 +УДФ
В зависимости от синтезируемого продукта рекомендуемое название фермента уточняется. Биосинтез крахмала катализирует крахмалсинтаза, гликогена - гликогенсинтаза.
8.3. Гидролазы (3)
Ферменты этого класса катализируют реакции гидролиза, т.е. расщепление сложных соединений на более простые с присоединением ионов воды:
RR1 + HOH = ROH + R1H. В зависимости от типа гидролизуемой связи (сложноэфирная, гликозидная, пептидная и т.д.)гидролазы разделены на 11 подклассов. Подподклассы выделены с учетом природы субстрата.
Гидролазы имеют огромное значение не только для живых организмов, но и для биосферы в целом. Без этих ферментов невозможен круговорот биогенных элементов. Многие из гидролаз имеют промышленное значение.
8.4. Лиазы (4)
Ферменты этого класса катализируют удаление из субстратов определенных групп (СО2, Н2О, NH3, альдегид) путем простого отщепления с образованием двойной связи или присоединение группы к двойной связи. Систематическое название фермента складывается из названия субстрата, названия удаляемой группы и через дефис слова “лиаза”. В рекомендуемых названиях используется термин “декарбоксилаза”, “альдолаза”, “дегидратаза”. В зависимости от типа разрываемых связей (С-С, С-О, С-N, C-S и др.) выделено семь подклассов. Деление на подподклассы произведено в зависимости от отщепляемой группы.
8.5. Изомеразы (5)
Ферменты этого класса катализируют изомеризацию, т.е. геометрические или структурные изменения, происходящие в пределах одной молекулы. Эти изменения могут происходить вследствие внутримолекулярного перемещения атомов водорода, фосфатных и ацильных групп, различных радикалов, двойных связей и т.п. В зависимости от типа катализируемой реакции изомеразы разделены на пять подклассов; подподклассы выделены в зависимости от характера превращения субстрата.
Фермент, катализирующий внутримолекулярный перенос групп называют мутазой. Изомеразы, катализирующие реакции инверсии при центрах асимметрии, называют рацемазами и эпимеразами. Рацемазы катализируют взаимные превращения D- и L-изомеров, эпимеразы - реакции изменения взаимного расположения атома водорода и гидроксильной группы у одного из углеродных атомов моносахоридов или их производных.
8.6. Л и г а з ы или с и н т е т а з ы (6)
Эти ферменты катализируют реакции присоединения друг к другу двух молекул, сопряженные с гидролизом пирофосфатной связи в АТФ или в другом нуклеозидтрифосфате. Образуемые в этих реакциях связи часто являются высокоэнергетическими. В зависимости от типа вновь образуемой связи (- С- О-, -С-S-, -С-N- и др.) лиазы разделили на пять подклассов. Подподклассы выделены в зависимости от природы образующегося соединения. Систематическое название составляется по схеме Х: У лигазы (образующая Z), где Х и У - соединяющие молекулы; в скобках указывается продукт расщепления нуклеозид-три- фосфата, участвующего в данной реакции в качестве источника энергии. В рекомендуемых названиях применяется термин синтетаза”.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 3332; Нарушение авторских прав?; Мы поможем в написании вашей работы!