
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
|
|
|
|
Последовательность заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах определяют:
1. принцип наименьшей энергии;
2. правило Клечковского;
3. принцип запрета Паули;
4. правило Гунда.
Принцип наименьшей энергии: максимуму устойчивости системы соответствует минимум её энергии.
Следовательно, в соответствии с данным принципом электроны будут вначале располагаться на атомных орбиталях, имеющих минимальную энергию, в этом случае связь электронов с ядром наиболее прочная и атомная система находится в состоянии максимальной устойчивости.
В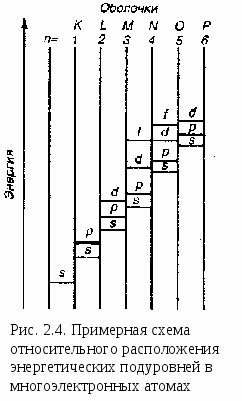 многоэлектронных атомах электроны испытывают не только притяжение ядер, но и отталкивание электронов, находящихся ближе к ядру и экранирующих ядро от более далеко расположенных электронов. Поэтому последовательность возрастания энергии орбиталей усложняется.
многоэлектронных атомах электроны испытывают не только притяжение ядер, но и отталкивание электронов, находящихся ближе к ядру и экранирующих ядро от более далеко расположенных электронов. Поэтому последовательность возрастания энергии орбиталей усложняется.
Порядок возрастания энергии атомных орбиталей в сложных атомах описывается правилом Клечковского: при увеличении заряда ядра атома заполнение орбиталей происходит в порядке возрастания суммы главного и орбитального квантовых чисел (n+l), а при равных значениях суммы (n+l) – в порядке возрастания n.
Соответственно этому правилу подуровни выстраиваются в следующий ряд (рис. 2.4.): 1s<2s<2p<3s<3p<4s≈3d<4p<5s≈4d<5p<6s≈4f≈5d<6p<7s≈5f≈6d.
Исключение составляют d и f – элементы с полностью и наполовину заполненными подуровнями, у которых наблюдается так называемый провал электронов, например: Cu, Ag, Cr, Mo, Pd, Pt (это явление будет рассмотрено позднее).
Принцип запрета Паули гласит: в атоме не может быть двух электронов с одинаковым набором четырех квантовых чисел.
Согласно этому принципу, на одной орбитали, характеризуемой определенными значениями трех квантовых чисел n, l и m l, могут находиться только два электрона, отличающихся значением спинового квантового числа ms, а именно ms=+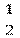 и ms= –
и ms= –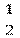 , т.е. спины которых противоположно направлены.Это можно символически представить следующей схемой.
, т.е. спины которых противоположно направлены.Это можно символически представить следующей схемой.
Заполнение и не допускается.
Принцип запрета Паули определяет электронную емкость энергетических уровней и подуровней. На s – подуровне (одна орбиталь) может быть лишь два электрона, на p – подуровне (три орбитали) – шесть, на d подуровне (пять орбиталей) – десять, на f – подуровне (семь орбиталей) – четырнадцать электронов. Вообще, максимальное число электронов на подуровне с орбитальным квантовым числом l равно 2(2 l +1). Поскольку число орбиталей данного энергетического уровня равно n2, емкость энергетического уровня составляет 2n2 электронов, где n – соответствующее значение главного квантового числа.
Правило Гунда: устойчивому (невозбужденному) состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спинового числа их (│∑ms│) максимально.
Другими словами: заполнение орбиталей одного подуровня в основном состоянии атома начинается одиночными электронами с одинаковыми спинами. После того как одиночные электроны займут все орбитали в данном подуровне, заполняются орбитали вторыми электронами с противоположными спинами.
1.8. Электронные семейства элементов
В зависимости от того, какой подуровень последним заполняется электронами, все элементы делятся на четыре типа – электронные семейства:
1. s – элементы; заполняется электронами s – подуровень внешнего уровня. К ним относятся первые два элемента каждого периода. Валентными 1 являются электроны внешнего уровня.
2. p – элементы; заполняется электронами р – подуровень внешнего уровня. Это последние шесть элементов каждого периода (кроме I и VII). Валентными являются s- и p- электроны внешнего уровня.
3. d – элементы; заполняется электронами d – подуровень второго снаружи уровня, а на внешнем уровне – один или два электрона (y 46Pd – нуль). К ним относятся элементы вставных декад больших периодов, расположенных между s – и p – элементами (их также называют переходными элементами). Валентными являются s – электроны внешнего уровня и d – электроны предвнешнего уровня (второго снаружи).
4. f – элементы; заполняется электронами f – подуровень третьего снаружи уровня, а на внешнем уровне остается два электрона. Они расположены в 6 – м (4f – элементы) и 7 – м (5f – элементы) периодах периодической системы. 4f – элементы объединяют в семейство лантаноидов, а 5f – элементы – семейство актиноидов.
В периодической системе s – элементов 14, p – элементов 30, d – элементов 38, f – элементов 28.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 24941; Нарушение авторских прав?; Мы поможем в написании вашей работы!