
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительная демеркаптанизация сжиженных газов и бензино-керосиновых фракций
|
|
|
|
Окислительная конверсия сероводорода в элементную серу (процесс Клауса)
Сероводород, получаемый с гидрогенизационных процессов переработки сернистых и высокосернистых нефтей, газоконденсатов и установок аминной очистки нефтяных и природных газов, обычно используют на НПЗ для производства элементной серы, иногда для производства серной кислоты.
Наиболее распространенным и эффективным промышленным методом получения серы является процесс каталитической окислительной конверсии сероводорода Клауса.
Процесс Клауса осуществляется в две стадии:
1) стадия термического окисления сероводорода до диоксида серы
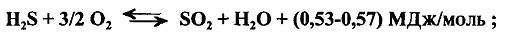
2)стадия каталитического превращения сероводорода и диоксида серы
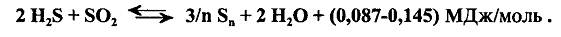
По реакции 1 расходуется до 70 % масс, сероводорода и при этом выделяется значительное количество тепла, которое перед каталитической стадией должно быть утилизировано. Тепло, выделяющееся по реакции 2 (1/5 от всего тепла), позволяет вести каталитический процесс при достаточно низких температурах и большой объемной скорости без системы съема тепла.
Процесс термического окисления H2S осуществляют в основной топке, смонтированной в одном агрегате с котлом-утилизатором. Объем воздуха, поступающего в зону горения, должен быть строго дозирован, чтобы обеспечить для второй стадии требуемое соотношение SO2 и H2S (по стехиометрии реакции 2 оно должно быть 1:2). Температура продуктов сгорания при этом достигает 1100-1300°С в зависимости от концентрации H2S и углеводородов в газе.
Вывод серы из реакционной системы, образовавшейся при реакции 2, благоприятствует увеличению степени конверсии H2S до 95%. Поэтому стадию каталитической конверсии принято проводить в две ступени с выводом серы на каждой ступени.
Зависимость степени конверсии H2S в серу от температуры и давления на обеих стадиях представлена на рис. 9.4. На графике показаны две зоны, разделенные пунктиром: высокотемпературная термического окисления (870-426 °С) и низкотемпературная каталитическая (426-204 °С).
В высокотемпературной зоне с повышением давления степень превращения H2S в серу снижается. В каталитической зоне повышение давления, наоборот, ведет к увеличению степени конверсии, так как давление способствует конденсации элементной серы и более полному выводу из зоны реакции.
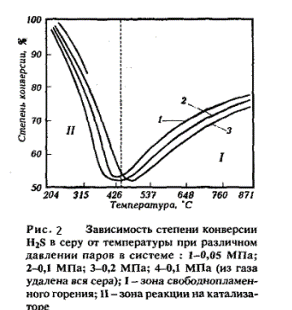
Элементная сера существует в различных модификациях - S2, S6 и S8: при высоких температурах газообразная сера в основном состоит из S2, а при снижении температуры она переходит в S6, затем в S8. Жидкая сера представлена преимущественно модификацией S8.
На практике увеличение степени конверсии H2S достигается применением двух или более реакторов-конверторов с удалением серы конденсацией и последующим подогревом газа между ступенями. При переходе от одного реактора к другому по потоку газа температуру процесса снижают.
Традиционным катализатором в процессах Клауса вначале являлся боксит. На современных установках преимущественно применяют более активные и термостабильные катализаторы на основе из оксида алюминия.
Технологическая схема установки производства серы по методу Клауса
Продукты термической конверсии H2S из печи-реактора П-1 проходят котел-утилизатор Т-1, где они охлаждаются до =160°С (при которой жидкая сера имеет вязкость, близкую к минимальной). Сконденсированная сера поступает через гидрозатвор в подземный сборник серы. В Т-1 генерируется водяной пар с давлением 0,4 - 0,5 МПа, используемый в пароспутниках серопроводов. Далее в реакторах Р-I и Р-2 осуществляется двухступенчатая каталитическая конверсия Н2S и SO2 с межступенчатым нагревом газов в печах П-2 и П-3 и утилизацией тепла процесса после каждой ступени в котлах-утилизаторах Т-2 иТ-3. Сконденсированная в Т-2 и Т-3 сера направляется в сборник серы.
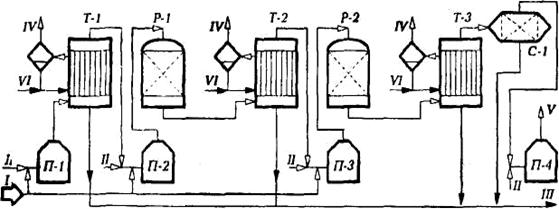
|
Рис. 3. Принципиальная технологическая схема установки получения серы из сероводорода по методу Клауса: I - сероводород; II - воздух; III - сера; IV - водяной пар; V - газы дожила; VI - конденсат
Газы каталитической конверсии второй ступени после охлаждения в котле-утилизаторе Т-3 поступают в сепаратор-скруббер со слоем насадки из керамических колец С-1, в котором освобождаются от механически унесенных капель серы.
Газы каталитической конверсии второй ступени после охлаждения в котле-утилизаторе Т-3 поступают в сепаратор-скруббер со слоем насадки из керамических колец С-1, в котором освобождаются от механически унесенных капель серы.
Технологический режим установки
Давление избыточное, МПа 0,03-0,05
Температура газа, °С
в печи-реакторе П-1 1100-1300
на выходе из котлов-утилизаторов 140-165
на входе в Р-1 260-270
на выходе из Р-1 290-310
на входе в Р-2 225-235
на выходе из Р-2 240-250
в сепараторе С-1 150
Сера широко применяется в народном хозяйстве - в производстве серной кислоты, красителей, спичек, в качестве вулканизирующего агента в резиновой промышленности и др.
Для сырьевой базы отечественной нефтепереработки характерно непрерывное увеличение за последние годы и в перспективе объемов добычи и переработки новых видов нефтей и газовых конденсатов из месторождений, прилегающих к прикаспийской впадине. Ряд из них, например, Оренбургский, Карачаганакский и Астраханские газоконденсаты, характеризуются аномально высоким содержанием в них меркаптанов (40 – 70 % от общего содержания серы) при относительно низком содержании общей серы (0,8 – 1,5%). По этому признаку их выделяют в особый класс меркаптансодер-жащего сильно аозииионно-активного углеводородного сырья. Мер-каптановая сера, обладающая неприятным запахом, вызывающая интенсивную коррозию оборудования и отравляющая катализаторы, концентрируется преимущественно в головных фракциях газоконденсатов – сжиженных газах и бензинах.
В отечественной и зарубежной нефтезаводской практике часто используют, помимо гидроочистки, процессы окислительной каталитической демеркаптанизации сжиженных газов – сырья алкилирования и бензинов, реже авиакеросинов. Среди них наибольшее распространение получили процессы «Бендер» и «Мерокс».
Процесс «Бендер» используется для очистки газовых бензинов и бензинов прямой гонки и термодеструктивных процессов, а также реактивного топлива от меркаптанов при малом их содержании в сырье (не более 0,1 %).
Процесс «Мерокс» применяется преимущественно для демеркаптанизации сжиженных газов и бензинов. Процесс окислительной демеркаптанизации сырья осуществляется в следующие три стадии:
1) экстракция низкомолекулярных меркаптанов раствором щелочи:
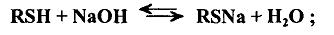
2) превращение меркаптидов натрия в дисульфиды каталитичеса окислением кислородом воздуха:
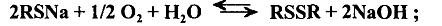
3)перевод неэкстрагированных щелочью высокомолекулярных меркаптанов сырья в менее активные дисульфиды каталитическим окислением кислородом воздуха:

Наиболее активными и распространенными катализаторами процесса «Мерокс» являются фталоцианины кобальта (металлоорганические внутрикомплексные соединения – хелаты) в растворе щелочи или нанесенные на твердые носители (активированные угли, пластмассы и др.).
Технологическая схема представлена на рис.4
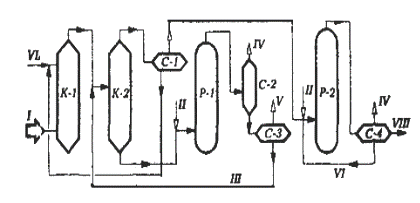
Рис.4. Принципиальная технологическая схема процеса каталитической окислительной демеркаптанизации углеводородного сырья «Мерокс»: I – сырье; II – воздух; III – регенерированный раствор щелочи («Мерокс»); IV – отработанный воздух; V— дисульфиды; VI— циркулирующий раствор щелочи («Мерокс»); VI – свежая щелочь; VIII— очищенный продукт
Исходное меркаптансодержащее сырье предварительно очищается от сероводорода и органических кислот в колонне 1 промывкой раствором щелочи, затем поступает в экстрактор К-2, где из него раствором щелочи экстрагируются низкомолекулярные меркаптаны. Экстрактный раствор из К-2 поступает в реактор Р-1, где производится каталитическое окисление меркаптидов натрия в дисульфиды кислородом воздуха с одновременной регенерацией раствора щелочи (или раствоа «Мерокс» в случае применения растворимогокатализатора). Реакционная смесь далее проходит сепараторы С-2 и С-3 для отделения отработанного воздуха и дисульфидов, после чего регенерированный раствор щелочи (или «Мерокса») возвращается в экстрактор К-2.
Очищенное от низкомолекулярных меркаптанов сырье (рафинатный раствор) поступает в сепаратор щелочи С-1, далее в реактор Р-2 для перевода высокомолекулярных меркаптанов, не подвергшихся экстракции в К-2, в дисульфиды каталитическим окислением кислородом воздуха. Реакционная смесь из Р-2 поступает в сепаратор С-4, где разделяется на отработавшийся воздух, циркулирующий раствор щелочи («Мерокс») и очищенный продукт.
Для очистки низкомолекулярных фракций (например, сырья алкилирования), не содержащих высокомолекулярных меркаптанов, используется упрощенный (экстракционный) вариант процесса, где стадия дополнительной окислительной демеркаптанизации в реакторе 2 исключена.
Ниже приведены данные по содержанию меркаптанов после окислительной демеркаптанизации различного сырья в процессе «Мерокс»:
Таблица1 Содержание меркаптнов г/т
| В сырье | В очищенном продукте | |
| Сжиженный газ | ||
| Бензин термического крекинга | ||
| Бензин каталитического крекинга | ||
| Керосин | Отрицательная докторская проба |
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 989; Нарушение авторских прав?; Мы поможем в написании вашей работы!