
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тепловой баланс выпарного аппарата
|
|
|
|
Материальный баланс выпарного аппарата
Обозначим начальное (до выпарки) и конечное (после выпарки) количество раствора (в кг) через G1 и G2, его начальную и конечную концентрацию (в весовых долях) через с1 и с2 и количество выпаренной воды (в кг) через W.
Тогда можно написать уравнения материального баланса по всему количеству вещества:
G1 = G2 +W
и по растворенному веществу
G1с1 = G2с2
В приведенные уравнения входят пять величин; три величины должны быть заданы, а остальные две можно определить из этих уравнений. Обычно бывают известны G1 a1 и а2, тогда, решая совместно уравнения (13-5) и (13-6), находим
G2 = G1с1 / с2
W = G1- G2 = G1(1 - с1 / с2)
Уравнение дает возможность определить количество выпаренной воды.
Для обогрева выпарных аппаратов чаще всего используется водяной пар. В некоторых случаях, когда необходимо проводить выпаривание при повышенной температуре, применяют топочные газы и специальные высокотемпературные теплоносители (например, АМТ-300), и в особых случаях используют электрический обогрев.
Составим уравнение теплового баланса выпарного аппарата для выпариваемого раствора:
Qпотерь


 Греющий пар пар соковый
Греющий пар пар соковый


 Раствор на выпарку
Раствор на выпарку
. Приход тепла
Отдается нагревающим агентом Qгр.п= Gгр.п iгр.п
С поступающим раствором G1с1 t1
Расход тепла
С вторичным паром.. Wiв.п
С уходящим раствором G2c2t2
Потери в окружающую среду Qn
С конденсатом вторичного пара Gконд c кондt конд
Таким образом
Qnр = Qрасх
Gгр.п iгр.п + G1с1 t1 = Wiв.п + G2c2t2 + G гр.п c кондt конд + Qn
Gгр.п iгр.п - G гр.п c кондt конд = Wiв.п + G2c2t2 - G1с1 t1 + Qn
где с1 и с2—удельные теплоемкости поступающего и уходящего растворов, дж/кг-град;
t1 и t2 — температуры поступающего и уходящего растворов, град;
iв.п —энтальпия вторичного пара, дж/кг.
Потери тепла принимаются 3-5 % от полезно затрачиваемого тепла, а затем рассчитывается изоляция (0,03-0,05 Qnр).
Gгр.п = (Wiв.п + G2c2t2 - G1с1 t1 + Qn)/ (iгр.п - c кондt конд)
Рассматривая поступающий раствор как смесь упаренного раствора и испаренной воды, можно написать:
G1с1 t2= G2c2t2+ Wсв. t2
откуда
G2c2 = G1с1 — WcB
где св — удельная теплоемкость воды, дж/кг • град.
Подставляя значение G2c2 в уравнение (13-10), получим
Gгр.п = (Wiв.п + (G1с1 — WcB) t2 - G1с1 t1 + Qn)/ (iгр.п - c кондt конд)
Gгр.п = (Wiв.п + G1с1 t2— WcB t2 - G1с1 t1 + Qn)/ (iгр.п - c кондt конд)
Gгр.п = (W(iв.п — cB t2)+ G1с1 (t2 - t1) + Qn)/ (iгр.п - c кондt конд)
Расчет выпарных аппаратов
Температура кипения растворов
Давление пара растворителя над раствором всегда ниже, чем давление над чистым растворителем. Вследствие этого температура кипения раствора выше температуры кипения чистого растворителя при том же давлении. Например, вода кипит под атмосферным давлением при 100° С, так как давление ее пара при этой температуре равно 1 am; для 30% раствора NaOH давление водяного пара над раствором будет при 100° С ниже 1 am, и раствор закипит при более высокой температуре (117°С), когда давление пара над ним достигнет 1 am.
Разность между температурами кипения раствора (t) и чистого растворителя (г)) называется температурной депрессией:
Δ tДЕПР =tраствор -tрастворитель
Температурная депрессия зависит от свойств растворенного вещества и растворителя; она повышается с увеличением концентрации раствора и давления. Определяется температурная, депрессия опытным путем (большинство опытных данных относится к температурной депрессии при атмосферном давлении).
Гидростатическая депрессия Δ t" вызывается тем, что нижние слои жидкости в аппарате закипают при более высокой температуре, чем верхние (вследствие гидростатического давления верхних слоев). Если, например, нагревать при атмосферном давлении воду до температуры кипения в трубе высотой 10 м, то верхний слой воды закипит при температуре 100° С, а нижний слой, находящийся под давлением 2 am, при температуре ~120оС. В данном случае гидростатическая депрессия изменяется по высоте трубы от 0°С (вверху) до 20° С (внизу) и в среднем составляет 10° С. Расчет гидростатической депрессии в выпарных аппаратах невозможен, так как жидкость в них (в основном в виде парожидкостной смеси) находится в движении. С повышением уровня жидкости в аппарате гидростатическая депрессия возрастает. В среднем она составляет 1—3°С.
Гидравлическая депрессия Δ t "' учитывает повышение давления в аппарате вследствие гидравлических потерь при прохождении вторичного пара через ловушку и выходной трубопровод. При расчетах Δ t "' принимают равной 1 С.
Полная депрессия Δt равна сумме температурной, гидростатической и гидравлической депрессий:
Δt = Δ t ' + Δt" + Δ t "'
Температура кипения раствора t определяетсяпо формуле:
tраствоитель =tраствоитель+Δt
Пример 13-1. Определить температуру кипения 40%-ного раствора NaOH при абсолютном давлении 0,196 бар (0,2 am).
Δ'=28°С при атмосферном давлении
Δ'=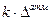 k=0,76 при 0,2 атм
k=0,76 при 0,2 атм
Δ'=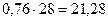
Δ''=2°С
Δ'''=1°С
Δ=15,2+2+1=24,28°С
tкип.р-ля(Н2О)=60°С при Р=0,2 атм
tкип.р-ля=24,28+60=84,28
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 2626; Нарушение авторских прав?; Мы поможем в написании вашей работы!