
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 9 !!!
|
|
|
|
Жиры
Классификация карбоновых кислот
Карбоновые кислоты классифицируют по двум структурным признакам.
1. По числу карбоксильных групп кислоты подразделяются на:
o одноосновные (монокарбоновые)
Например:
o многоосновные (дикарбоновые, трикарбоновые и т.д.).
o По характеру углеводородного радикала различают кислоты:
o предельные (например, CH3CH2CH2COOH);
o непредельные (CH2=CHCH2COOH);
o и ароматические (RC6H4COOH).
Карбоновые кислоты содержат карбоксильную группировку –COOH. Свойства кислоты определяются природой радикала R, обычно это слабые кислоты, pH = 4–5. Название происходит от соответствующего углеводорода с добавлением окончания «-вая кислота» или окончания «-карбоновая кислота» к углеводороду на один атом меньше:
R = H – метановая кислота, муравьиная кислота;
R = CH3 – этановая кислота, метанкарбоновая кислота, уксусная кислота;
R = C2H5 – пропановая кислота, этанкарбоновая кислота, пропионовая кислота;
R = C6H5 – бензойная кислота, фенилкарбоновая кислота;
R = (C6H5)3C – трифенилуксусная кислота.
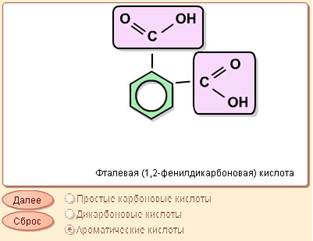
|
| Модель 12.4. Карбоновые кислоты. |
Большое значение в биохимии имеют дикарбоновые кислоты: алифатические насыщенные HOOC–(CH2)n–COOH (n = 0, 1, 2,...), алифатические ненасыщенные (HOOC)2CnH2n–2 (n = 2, 3, 4,...), ароматические C6H4(COOH)2.
В растворах кислоты диссоциируют:
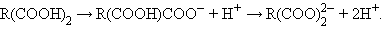
|
Карбоновые кислоты в свободном состоянии и в растворах склонны к димеризации или ассоциации за счет сильной водородной связи.
2. Оксикислоты window.top.document.title = "12.5.1. Оксикислоты";
Оксикислоты характеризуются наличием в молекуле кроме карбоксильной еще гидроксильной группы О–Н, их общая формула R(OH)n(COOH). Формально простейшей оксикислотой будет хорошо известная неорганическая угольная кислота (оксометановая кислота). Поскольку функции двух О–Н-групп, связанных с одним атомом углерода, одинаковы, то любая из них может входить в карбоксильную группировку и диссоциировать по механизму двухосновной кислоты. Собственно первым представителем органических оксикислот будет оксиэтановая кислота (оксиуксусная, оксиметанкарбоновая, гликолевая кислота).
Наиболее важными из оксикислот, участвующих в процессах жизнедеятельности, являются:
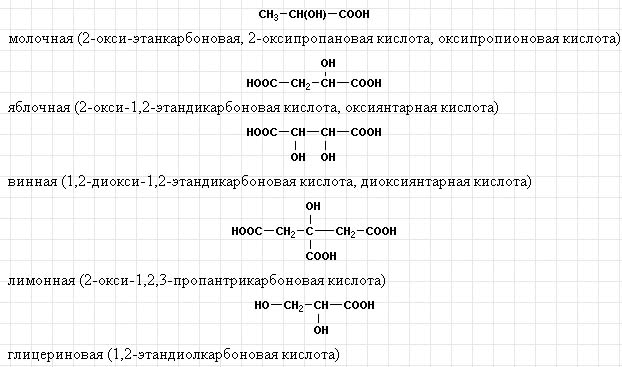
3.Эфиры window.top.document.title = "12.4.4. Эфиры";
Сложные эфиры содержат группировку
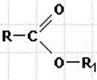
При этом R и R1 могут быть одинаковыми или разными.
Сложные эфиры образуются в результате реакции этерификации:
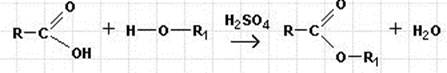
Название начинается с радикала спирта и заканчивается названием кислоты с добавлением суффикса -ат.
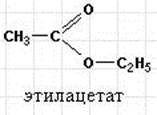
Под действием кислот, а особенно оснований, идет обратная реакция гидролиза (омыления). Сложные эфиры относятся к органическим растворителям. Взаимодействие дикарбоновой кислоты с диолом приводит к образованию полиэфиров (полимеров):
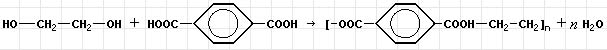
Простые эфиры содержат группировку R–O–R1. Получаются они отщеплением воды от двух молекул спирта:
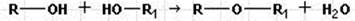
При R = R1 эфир называется симметричным, если радикалы разные – несимметричным. Название – по радикалам с добавлением слова «эфир»:
C2H5–O–C2H5 – диэтиловый эфир, C2H5–O–CH3 – метилэтиловый эфир.
Жиры – сложные эфиры глицерина и высших одноосновных карбоновых кислот.
Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты -C(O)R.
В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C15H31COOH, стеариновой C17H35COOH и др.) и ненасыщенных (олеиновой C17H33COOH, линолевой C17H31COOH, линоленовой C15H29COOH).
Жиры содержатся во всех растениях и животных.
Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение – рыбий жир). Жиры состоят главным образом из триглицеридов предельных кислот.
Растительные жиры – масла (подсолнечное, соевое, хлопковое и др.) – жидкости (исключение – кокосовое масло). В состав триглицеридов масел входят остатки непредельных кислот.
Жидкие жиры превращают в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел.
Продукт гидрогенизации масел – твердый жир (искусственное сало, саломас). Маргарин – пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла – соли высших карбоновых кислот и щелочных металлов.
Натриевые соли – твердые мыла, калиевые – жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 394; Нарушение авторских прав?; Мы поможем в написании вашей работы!