
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные понятия химии
|
|
|
|
Основные понятия и количественные законы химии. Фактор эквивалентности. Его нахождение для реакций ионного обмена и окислительно-восстановительных процессов. Вычисление эквивалентных масс и эквивалентных объемов. Закон эквивалентов. Его применение.
Лекция 1.Введение.
Химия – наука о веществах и законах, по которым происходят превращения одних веществ в другие. Вещество и поле - две формы существования материи. Вещество – форма материи, которая обладает собственной массой, т.е. массой покоя. Состоит из элементарных частиц: электронов, протонов, нейтронов, мезонов и др.Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы. Поле – форма существования материи, которая тесно связана с энергией. Важнейший закон природы - закон сохранения массы и энергии был сформулирован в 1760 г. М.В. Ломоносовым. Современная формулировка: в изолированной системе сумма масс и энергий постоянна. Изолированной системой является та система, у которой нет обмена с окружающей средой ни массой, ни энергией. Между массой и энергией существует взаимосвязь согласно уравнению Е = mc2. Объект изучения химии – элементы и их соединения. Элемент – определенный вид атомов, обладающих определёнными зарядами ядер. Атом – мельчайшая частица элемента, сохраняющая все его химические свойства. Атомы складываются в молекулы.
Молекулой называется наименьшая частица вещества, которая может существовать самостоятельно, обладает химическими свойствами данного вещества и состоит из атомов одного или нескольких элементов. Молекулы, состоящие из атомов одного элемента, образуют простые вещества (Cu, H2, O3). Простые вещества образованы атомами одного химического элемента и потому являются формой его существования в свободном состоянии, например, сера, железо, озон, алмаз. Сложные вещества образованы разными элементами и могут иметь состав, постоянный или меняющийся в разных пределах. Молекулы, состоящие из атомов различных элементов, образуют сложные вещества (HCl, Н2O, C17H35, COOH) Химические свойства вещества характеризуют их способность участвовать в химических реакциях, т.е. превращениях одних веществ в другие. Для понимания этих свойств необходимо знать не только состав, но и строение веществ.
Например:
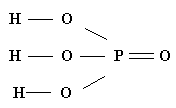
| ||
| Н3РО4 | ||
В химии существует очень важное понятие - количество вещества. Количество вещества – число структур единиц молекул, атомов. ионов и т. д. в системе. Единицей количества вещества является моль.
Моль – это количество вещества системы, равное 6,022.1023 структурных единиц данного вещества. Количество структурных единиц равно количеству атомов, содержащихся в 0,012 кг 6C12. При использовании термина "моль" следует указывать частицы (моль молекул, атомов...). Масса одного моль вещества называется молярной массой, размерность: кг/моль или г/моль. Объем одного моль вещества называется молярным объемом, размерность: м3/моль или л/моль. При нормальных условиях (273,15 К(0°С); 1,0133·105Па (760 мм рт.ст.). 1 моль различных газов занимает объем 22,4 л.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 1106; Нарушение авторских прав?; Мы поможем в написании вашей работы!