
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы повышения жаростойкости металлов
|
|
|
|
Во многих химических процессах металлические конструкции и изделия эксплуатируются в жестких условиях, при повышенных температурах, больших давлениях, высокой агрессивности среды.
Чистые металлы, как правило, являются коррозионностойкими и требуют дополнительных мер защиты.
Современная техника противокоррозионной защиты располагает рядом эффективных способов для увеличения стойкости металлов и сроков их эксплуатации. Применительно к условиям газовой коррозии одним из наиболее часто используемых способов является жаростойкое легирование с целью получения сплавов, обладающих повышенной коррозионной устойчивостью.
В настоящее время существует три наиболее обоснованные теории жаростойкого легирования, которые не противоречат, а скорее дополняют друг друга.
Согласно первой теории, разработанной Вагнером и Хауффе, небольшая добавка легирующего элемента окисляется и, растворяясь в оксиде основного металла, уменьшает число дефектов в кристаллической решетке основного металла. Это приводит к упорядочиванию структуры и снижает скорость диффузии ионов в защитной пленке.
Данная теория имеет довольно ограниченную область применения. Если скорость окисления металла определяется не диффузией ионов или при легировании в оксидной пленке образуется новая фаза, то изложенные выше предположения жаростойкого легирования неприменимы.
Согласно второй теории, разработанной А.А. Смирновым, Н.Д. То-машовым и др., на поверхности металла образуется защитный оксид легирующего элемента, который препятствует окислению основного металла.
Применительно к этой теории легирующий компонент должен обладать перечисленными ниже основными свойствами.
1. Оксид легирующего элемента должен удовлетворять условию сплошности, т.е. отношение объемов оксида и металла должно быть больше единицы: Vок/Vме > 1. В табл. 3.6 приведены обобщающие данные по некоторым свойствам оксидов хрома, алюминия и кремния. Эти элементы являются основными добавками для повышения жаростойкости железа. Как показывают данные таблицы это условие для вышеназванных элементов выполняется.
2. Легирующий элемент должен образовывать оксид с высоким электрическим сопротивлением. Большое омическое сопротивление (низкая электропроводимость) является одним из основных условий для формирования защитных свойств пленки, так как при этом движение ионов в слое оксида затрудняется.
3. Энергия образования оксида легирующего элемента должна быть больше энергии образования оксида основного металла, т.е.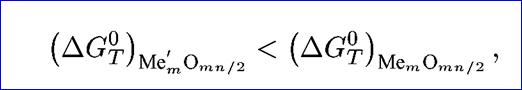
где Me’ — легирующий компонент; Me — основной металл.
Это условие обеспечивает стойкость оксида легирующего компонента в присутствии основного металла. Оксид компонента добавки оказывается более устойчивым, чем оксид основного металла. Если это условие не соблюдается, то оксид легирующего элемента будет восстанавливаться основным металлом.
Приведенные в таблице 3.6 данные по теплотам образования оксидов железа, AI2O3, Сr2О3 и SiO2 подтверждают сформулированное выше правило. Более того, если первоначально образуется смешанный оксид, то в дальнейшем в соответствии с условиями термодинамического равновесия, он переходит в чистый оксид легирующего компонента.
Например, при окислении железа легированного алюминием, имеет место образование оксида железа FeO. Но далее возможен процесс:
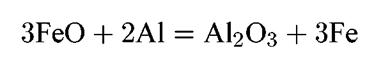
4. Размер ионов легирующего элемента должен быть меньше, чем размер иона основного металла (см. табл. 3.6). Это облегчает диффузию легирующего элемента к поверхности сплава, на котором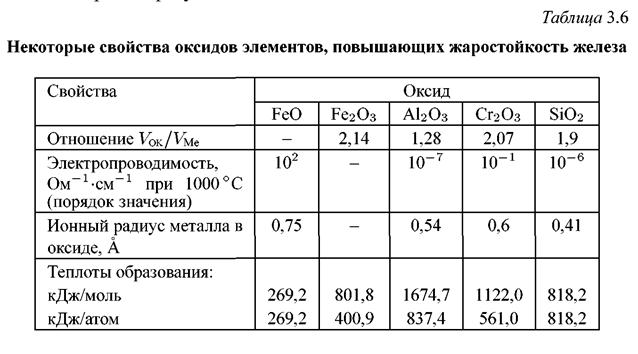
образуется защитная пленка.
5. Оксиды легирующих компонентов должны иметь высокие температуры плавления и возгонки и не образовывать низкоплавких эвтектик. Это требование обеспечивает сохранение оксида при высоких температурах в твердой фазе. Переход оксида в жидкое состояние облегчил бы протекание в нем диффузионных процессов. Частичная возгонка оксида увеличила бы пористость пленки, что способствует снижению ее защитных свойств.
6. Легирующий компонент и основной металл должны образовывать твердый раствор при данном составе сплава. Только при этом условии удается обеспечить сплошную пленку оксида легирующего компонента по всей поверхности сплава.
Эта теория жаростойкого легирования находится в хорошем согласии с целым рядом практических данных.
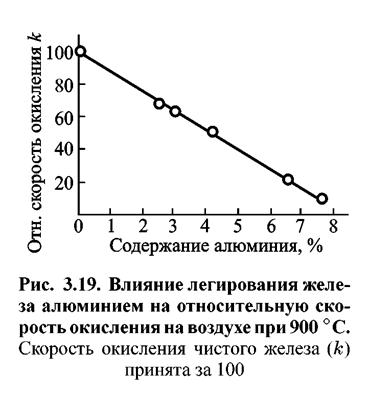
Экспериментально было установлено наличие защитного слоя оксида, преимущественно образованного легирующим компонентом сплава (хрома или алюминия) для ряда жаростойких железных сплавов. На рис. 3.19 показано значительное снижение скорости окисления железа от концентрации легирующей добавки — алюминия.
Третья теория жаростойкого легирования основана на постулате об образовании двойных оксидов, обладающих высокими защитными свойствами.
Эта теория применительно к сплавам железа была наиболее полно сформулирована В.И. Архаровым. Повышение жаростойких свойств железных сплавов может быть достигнуто при соблюдении двух условий:
• устранение при окислении железа на поверхности соединений со структурой вюстита;
• образование на поверхности сплава оксидов типа шпинели с возможно меньшими параметрами кристаллической решетки.
Как известно, при окислении железа образуются различные оксиды, отличающиеся по составу и защитным свойствам. Оксиды со структурой вюстита (FeO) обладают меньшим защитным действием при газовой коррозии, чем другие оксиды железа со структурой шпинели (Fe3O4, Fe2O3).
Пониженные защитные свойства вюстита объясняются тем, что в структуре FeO легко осуществляется диффузия ионов металла. Скорость окисления железа заметно возрастает при температурах 500-600 °С. Этот эффект совпадает с началом образования вюститной фазы.
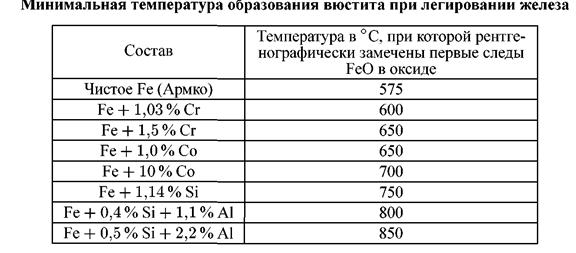
 Если в состав железа ввести легирующие элементы, способствующие образованию двойных оксидов типа FeCr2O4, FeAl2O4, NiFe2O4, NiCr2O4 и др., то возможность возникновения вюститной фазы будет затруднена. Экспериментально это выражается в повышении температуры образования вюстита, фиксируемого рентгенографическими методами (табл. 3.7).
Если в состав железа ввести легирующие элементы, способствующие образованию двойных оксидов типа FeCr2O4, FeAl2O4, NiFe2O4, NiCr2O4 и др., то возможность возникновения вюститной фазы будет затруднена. Экспериментально это выражается в повышении температуры образования вюстита, фиксируемого рентгенографическими методами (табл. 3.7).
Данные таблицы показывают, что даже при низкопроцентном легировании основные легирующие компоненты жаростойких железных сплавов заметно повышают температуру начала появления вюститной фазы.
 |
Более высокие защитные свойства наблюдают у оксидов Fe3O4 и γ~Fe2O3, характеризующихся структурой шпинели. Эта структура имеет более плотную решетку с меньшими расстояниями между от
дельными узлами и характеризуется отсутствием дефектов. Поэтому шпинельная структура препятствует диффузии ионов.
Установлено, что железо в пассивном состоянии, а также легированные стали имеют поверхностные слои с кристаллографической решеткой шпинельного типа.
Еще более высокими защитными свойствами обладают поверхностные сложные оксиды типа FeО.Мe2О3 или Fe2O3.MeO, если легирующий компонент имеет меньший ионный радиус по сравнению с железом (см. табл. 3.6).
Отмечают закономерную связь между уменьшением параметров кристаллической решетки и эффектом повышения жаростойкости. Очевидно, что внедрение в структуру шпинели новых катионов с меньшим ионным радиусом будет уменьшать параметры решетки и затруднять диффузию ионов кислорода и основного металла.
Установлено, что слой оксидной пленки, примыкающий к поверхности высокохромистой стали, имеет состав FeО.Cr2О3, а внешний слой — a(Fe, Сr)2О3.
На хромоникелевых сплавах при высоких температурах образуется защитная пленка шпинельной структуры — NiО.Cr2О3, а на хромоалюминиевых железных сплавах — сложные оксиды: m(FeO· Cr2O3)+n(FeO.Al2O3).
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 2042; Нарушение авторских прав?; Мы поможем в написании вашей работы!