
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Очаговая гнойная инфекция. 4 страница
|
|
|
|
Клинические проявления. После инкубационного периода продолжительностью от 3 до 10 дней на месте внедрения инфекции появляется маленькая воспалительная папула, которая изъязвляется в течение 2—3 дней. Классическая характерная для мягкого шанкра язва (рис. 110-1), как правило, поверхностна, размеры ее варьируют от нескольких миллимегров до нескольких сантиметров в диаметре. Края неровные и подрытые, дно покрыто некротическим экссудатом. Язвы часто бывают множественными и могут сливаться, образуя гигантские, или ползучие, язвы. Иногда очаги поражения остаются пустулезными и напоминают фолликулиты или пиогенную инфекцию. В противоположность сифилису язвенные поражения при мягком шанкре у мужчин очень болезненны и не имеют плотной консистенции; наиболее часто язвы локализуются по краю крайней плоти, на ее
Рис. 110-1. Классический мягкий шанкр.
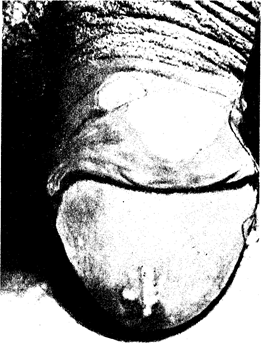
внутренней поверхности и на уздечке. У женщин поражаются половые губы, уздечка половых губ и перианальная область; очаги поражения более поверхностные и менее болезненные.
Почти у 50% больных развивается острая, болезненная воспалительная аденопатия паховых лимфатических узлов, чаще односторонняя, сопровождающаяся их уплотнением. Если своевременно не начать лечение, вовлеченные в процесс лимфатические узлы сливаются, формируя однофокусный гнойный бубон. Покрывающая его кожа натягивается, становится эритематозной и в конце концов прорывается, формируя глубокую одиночную язву.
Диагностика. Диагностика, основанная на оценке морфологии очагов поражения, расположенных на половых органах, чревата ошибками, и многие очаги, диагностируемые как проявления мягкого шанкра, на самом деле являются генитальными проявлениями герпеса или сифилиса. В одном проведенном в США исследовании из 100 последовательно включенных в него мужчин с наличием язвы на половом члене у 22 обнаружен генитальный гсрпес, у 17—сифилис, у 8— травматические очаги. Классические для мягкого шанкра язвы были отмечены у 12, но только у 2 из них из язв был выделен возбудитель. В другом исследовании у 2 больных с подозрением на паховую гранулему выделена культура Н. ducreyi. Эти поражения были определены как паховая гранулема мягкого шанкра. В противоположность этому в Кении из 97 мужчин с изъязвлением полового члена 60 были инфицированы Н. ducreyi, у 11 был диагностирован сифилис и только у 4 — генитальный гсрпес.
Первичная инфекция половых путей вирусом простого герпеса также вызывает болезненную паховую аденопатню, но может быть распознана по особенностям начала заболевания с везикулярных очагов или по наличию в анамнезе данных о возможном заражении вирусом герпеса и по присутствию системных симптомов, таких как лихорадка и миалгия. Мягкий шанкр системных симптомов, как правило, не вызывает.
Шанкр первичного сифилиса отличается плотной консистенцией, сопровождается двусторонней аденопатией, безболезненный, без нагноения. Для исключения сифилиса у всех больных, имеющих язвы на половых органах, необходимо произвести два последовательных (в разные дни) бактериоскопических исследования в темном поле отделяемого язв, а также троекратное (с интервалами в один месяц) серологическое исследование сыворотки крови на наличие антител к возбудителю сифилиса.
При венерической лимфогранулеме (LGV) в отличие от мягкого шанкра аденопатия развивается после заживления язвы. Она безболезненна, часто имеет двустороннюю локализацию и характеризуется многоочаговыми нагноениями и свищами.
Диагноз мягкого шанкра подтверждается выделением возбудителя Н. ducreyi из язв или бубонов. Экссудат следует высевать непосредственно на шоколадный агар, обогащенный 1% Isovitalex и 5% сыворотки барана с добавлением 3 мкг/мл ванкомицина. Видимый рост колоний обычно появляется через 48 ч инкубации в атмосфере, содержащей 5% двуокиси углерода при 100% влажности, но иногда для появления видимого роста может потребоваться 4—5 сут. Серологических тестов для диагностики мягкого шанкра в распоряжении медицинских работников нет.
Лечение. Без соответствующего лечения язвы мягкого шанкра персистируют длительное время и часто прогрессируют. Малые очаги поражения могут заживать в течение 2—4 нед. Хотя сульфаниламиды и препараты группы тетрациклина считаются активными при лечении мягкого шанкра, в ряде случаев лечение оказывается неэффективным вследствие множественной лекарственной устойчивости возбудителя. Многие выделенные от больных штаммы Н. ducreyi обладают плазмидами, опосредующими устойчивость к сульфаниламидам, тетрациклинам, левомицетину, ампициллину и канамицину. Центр по контролю заболеваний рекомендует применять для лечения мягкого шанкра триметоприм — сульфаметоксазол (320 мг триметоприма и 1600 мг сульфометоксазола ежедневно) или эритромицин в дозе 2 г в сутки в течение недели. Применение триметоприма — сульфаметоксазола не оказывает влияния на результаты проводимых во время лечения исследований по выявлению Treponema pallidum (в темном поле зрения) и на развитие положительных серологических реакций на сифилис. Время, необходимое для заживления очагов поражения, обычно составляет 9 дней с момента начала их лечения. В Кении доказана высокая эффективность применения при мягком шанкре нескольких медикаментозных режимов, состоящих из однократного приема лекарственного препарата, в частности 640 мг триметоприма и 3200 мг сульфометоксазола, 2 г спектомицина внутримышечно и 250 мг цефтриаксона (Ceftriaxone) внутримышечно. При появлении флюктуации бубонов, а также в том случае, если диаметр бубона более 5 см, их содержимое необходимо аспирировать во избежание разрыва. Нагноение лимфатических узлов может прогрессировать, несмотря на то что другие очаги поражения успешно излечиваются.
Половых партнеров лиц, больных мягким шанкром, следует обследовать с целью выявления язв. Рекомендуется лечение контактных лиц. Хотя эпидемиология мягкого шанкра основана на том, что эффективные превентивные меры, направленные на ограниченные специфические контингенты населения (проститутки, установленные половые партнеры), могут остановить распространение болезни, требуются перспективные эпидемиологические исследования.
ГЛАВА 111. ДОНОВАНОЗ (ВЕНЕРИЧЕСКАЯ ГРАНУЛЕМА)
Кинг К. Холмс (King К. Holmes)
Определение. Донованоз (венерическая гранулема) — это слабоконтагиозное, хроническое, вялопрогрессирующее язвенное заболевание, поражающее кожные покровы и лимфатические узлы генитальной и перианальной области. Заболевание передается половым путем и обусловлено присутствием в клетках пораженных тканей микроорганизмов, которые морфологически самоидентифицируются как тельца Донована. Возможно самозаражение.
Этиология. Донованоз был описан McLeod в Индии в 1882 г., а в 1905 г. Донован выделил внутриклеточные тельца, которые считаются причиной болезни. Инкапсулированные бактерии, напоминающие тельца Донована, были выделены из очагов поражения и псевдобубонов паховой гранулемы путем введения их содержимого в желточный мешок куриных эмбрионов или при посеве на яично-агаровую среду. Эти бактерии, известные как Calymmatobacterium granulomatis, размером 1,5Х 0,7 мкм, по составу своих антигенов приближаются к клебсиеллам, однако при внутрикожном введении их человеку воспроизвести заболевание не удается. Точно не известно, являются ли эти микроорганизмы возбудителем данного заболевания. Электронно-микроскопические исследования телец Донована подтверждают их морфологическое сходство с грамотрицательными бактериями.
Эпидемиология. Донованоз — эндемическая тропическая болезнь, особенно широко распространенная в Новой Гвинее, среди индусов в Индии, в странах Карибского бассейна и в Африке. В США встречается редко. Большинство случаев донованоза наблюдается в юго-восточных штатах и преимущественно у гомосексуалистов. Среди описанных случаев соотношение частоты заболеваний среди мужчин и женщин соответствует 10:1. У кавказских народов заболевание встречается редко. Известная частота донованоза в супружеских парах хронических больных колеблется от 1 до 64%. Доказательства распространения заболевания половым путем основаны на следующих факторах: возрастная специфичность, соответствующая таковой при других передающихся половым путем инфекциях; частое сочетание с сифилисом; склонность к поражению половых органов у гете росексуалистов и к инфекции в аноректальной области у активных гомосексуалистов.
Клинические проявления. Инкубационный период колеблется от 8 до 12 нед, но большинство очагов появляется в течение 30 дней после полового контакта с больным.
Болезнь начинается с появления папулы, которая затем изъязвляется и превращается в безболезненную несколько приподнятую над окружающими тканями очищенную зону рыхлой грануляционной ткани мясисто-красного цвета. Края язвы имеют неправильную форму; рост язвы осуществляется per continuitatem, часто в результате аутоинфекции в процесс вовлекаются прилежащие участки кожных покровов. Присоединяющаяся вторичная анаэробная инфекция вызывает болезненные ощущения и выделение зловонного экссудата. Реже наблюдаются осложнения в виде глубоких изъязвлений, хронического рубцевания очагов, фимоза, лимфатического отека, избыточной пролиферации эпителия, напоминающей карциному. У мужчин очаги поражения обычно локализуются на головке или теле (рис. Ill-la) полового члена, на крайней плоти или в перианальной области, тогда как для женщин наиболее характерно поражение половых губ. У женщин очаг поражения часто возникает в районе заднего соединения половых губ (уздечки) и затем прогрессирует в переднем направлении вдоль половой щели. Вторичные очаги поражения могут обнаруживаться на лице, шее, в ротовой полости, на других участках тела. Хроническое течение заболевания имеет важное диагностическое значение, так как часто проходит несколько месяцев, прежде чем больной получает лечение. Распространение процесса на паховую область при самозаражении, по продолжению или по лимфатическим путям, приводит к возникновению внутрикожных и подкожных очагов припухлости или нагноения, известных как «псевдобубоны», так как вовлечение в процесс прилежащих лимфатических узлов обычно бывает минимальным. Локальные деструктивные поражения или вторичная инфекция могут вызвать тяжелое заболевание или смерть. Описаны фатальные диссеминированные формы донованоза с вовлечением в патологический процесс костей, суставов или печени, развившиеся в результате длительной (иногда многолетней) хронической локальной инфекции. Взаимоотношения между донованозом и последующим развитием карциномы гениталий точно не установлено.
Диагностика. Ранние проявления донованоза могут быть ошибочно диагностированы как первичный шанкр или широкая сифилитическая кондилома. Напоминающая карциному пролиферация эпителия в области гениталий или пери-анальной зоне (особенно у молодых людей) должна всегда вызывать подозрение на донованоз. При этом, если нет необходимости, следует по возможности избегать хирургических вмешательств. Хронические язвенные или рубцовые изменения могут напоминать венерическую гранулему.
Очаги поражения мужского полового члена, напоминающие донованоз, могут быть вызваны амебиазом. В США из очагов, похожих на донованозные, нередко выделяются Haemophilus ducreyi. Гистологические исследования при донованозе выявили выраженный акантоз и псевдоэпителиоматозную гиперплазию. В дерме обнаруживаются воспалительные инфильтраты, состоящие главным образом из плазматических клеток и гистиоцитов. Так как тельца Донована редко выявляются в срезах тканей, окрашенных гематоксилином и эозином, эти изменения могут привести к ошибочному диагнозу карциномы и к ненужному хирургическому вмешательству. Несмотря на то что метод импрегнации серебром позволяет эффективно выявлять тельца Донована в срезах, диагноз лучше всего удается установить при исследовании мазков-отпечатков, приготовленных из материала, полученного при пункционной биопсии грануляционной ткани с периферии очага. Небольшие кусочки биоптата растирают между двумя стеклами, высушивают на воздухе, фиксируют в метиловом спирте и окрашивают красителем Райта — Гимзы. Тельца Донована выявляются при этом в виде округлых коккобацилл размером 1 X 2 мкм, располагающихся в кистевидных полостях цитоплазмы больших мононуклеарных клеток (рис. 111-2). Капсула окрашивается как плотная ацидофильная зона, окружающая бактерию, которая благодаря биполярному скоплению хроматина напоминает закрытую английскую булавку. Патогномоничная мононуклеарная клетка имеет 25—90 мкм в диаметре и содержит в цитоплазме многочисленные кистозные полости с тельцами Донована.
Рис. 111-1. Обширная паховая гранулема, распространяющаяся вдоль мошонки и вовлекающая пахово-мошоночные складки с приподнятой, очищенной, разросшейся грануляционной тканью. я — до лечения; б — после лечения (с любезного согласия A. Brathwaite).
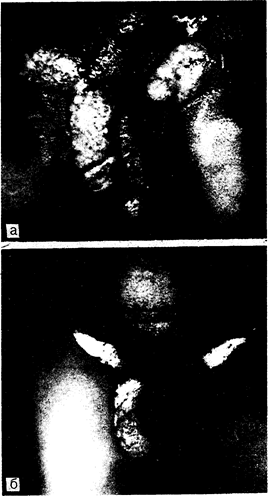
Перианальный. донованоз напоминает широкую кондилому вторичного сифилиса. Донованозу часто сопутствуют другие венерические заболевания, в частности сифилис. В связи с этим перед началом лечения необходимо проводить повторные исследования в темном поле очагов поражения, а также серологические реакции на сифилис. В этом случае, если предполагаемая широкая кондилома не излечивается после соответствующего применения пенициллина по поводу сифилиса, следует вполне обоснованно предположить наличие донованоза. Это заключение особенно актуально для стран, где донованоз является эндемической болезнью.
Лечение. Наиболее эффективен тетрациклин в дозе 2 г ежедневно на протяжении по крайней мере 10 дней. Риск рецидива снижается, если лечение продолжается до полного выздоровления. Излечение обычно наступает в течение 3 нед, патологические очаги бледнеют, по краям их появляются признаки реэпителизации (см. рис. 111-16). Тельца Донована исчезают из очагов поражения через несколько дней после начала лечения. Если по каким-либо причинам тетрациклин не может быть применен, рекомендуется использовать стрептомицин внутримы 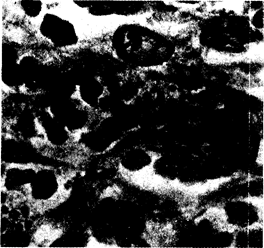
Рис. 111-2. Биопсия из язвы паховой гранулемы. Показаны мононуклеарные клетки, содержащие тельца Донована. Окраска по Райту — Гимзе.
шечно в дозе 1 г каждые 12 ч в течение 10—15 дней. В Новой Гвинее при подозрении на наличие устойчивости возбудителя к тетрациклину применяется левомицетин перорально по 500 мл через 8 ч или гентамицин в дозе 1 мг/кг дважды в сутки. Сообщают также об эффективности ко-тримоксазола (триметоприм 160 мг, сульфаметоксазол 800 мг) дважды в сутки в течение 10 дней. Беременным женщинам с успехом рекомендуют эритромицин в дозе 500 мг через каждые 6 ч. Более детально лечение рассматривается в главе, написанной Hart (1984).
ГЛАВА 112. БРУЦЕЛЛЕЗ
Дональд Кайе, Роберт Г. Петерсдорф (Donald Kaye, Robert G. Petersdorf)
Определение. Бруцеллез (ундулирующая лихорадка, мальтийская лихорадка, средиземноморская лихорадка) — инфекционная болезнь, вызываемая микроорганизмами рода Brucella, передающимися людям от домашних животных. Характеризуется лихорадкой, повышенным потоотделением, генерализованной слабостью, недомоганием и потерей массы тела, часто при отсутствии очаговых изменений.
Этиология. Бруцеллез у человека вызывает один из четырех видов возбудителя: В. melitensis (патогенные для мелкого рогатого скота), В. suis (патогенные для свиней), В. abortus (патогенные для крупного рогатого скота) и В. canis (патогенные для собак). Зарегистрировано относительно мало случаев инфекции, вызываемой В. canis, однако распространена она, вероятно, намного больше, чем ее диагностируют.
Хотя циркуляция указанных видов возбудителей происходит главным образом между их специфическими хозяевами, возможны случаи инфицирования свиней В. abortus или крупного рогатого скота В. suis, кроме того, случаи бруцеллеза зарегистрированы и у животных других видов. Дифференциация видов бруцелл основана на биохимических и серологических реакциях. Бруцеллы — мелкие, неподвижные, неспорообразующие, грамотрицательные коккобациллы, растущие лучше всего при температуре 37°С в триптиказном соевом бульоне или в трип-тозпом фосфатном бульоне при рН от 6,6 до 6,8 и повышенном содержании двуокиси углерода.
Эпидемиология. Естественным резервуаром бруцеллеза являются домашние животные, в частности крупный и мелкий рогатый скот, свиньи. Бруцеллез у естественных хозяев — весьма контагиозная инфекция. Вместе с тем она может поражать и вторичных хозяев, таких как человек. Передача инфекции от человека человеку происходит редко. От животного к животному инфекция передается половым путем или при употреблении инфицированных кормов или молока. Заражение людей чаще всего происходит при употреблении инфицированных молока, продуктов животного происхождения или непосредственно через поврежденную кожу.
В США ежегодно регистрируется в среднем около 200 случаев бруцеллеза, что по имеющимся оценкам составляет только примерно 4% всех случаев. В целом распространенность болезни тесно коррелирует с уровнем пораженности животных в том или ином регионе. В ряде стран Европы, где бруцеллез почти полностью ликвидирован, заболеваемость животных также находится на очень низком уровне. В США более высокий уровень заболеваемости бруцеллезом отмечается в районах, специализирующихся на животноводстве.
Бруцеллезом чаще всего заражаются лица, имеющие контакт с инфицированным бруцеллами сырьем, молоком или молочными продуктами — работники мясокомбинатов (боен), мясники, фермеры, животноводы, ветеринарные врачи, а также лица, употребляющие непастеризованные молочные продукты. В большинстве случаев, когда заражение бруцеллезом произошло в результате употребления непастеризованных молочных продуктов, последние были приобретены в зарубежных (по отношению к США — перев.) странах, особенно Средиземноморского бассейна, Дальнего Востока, Южной Америки и в Мексике. В США бруцеллез распространен главным образом среди мужчин трудоспособного возраста, большую часть которых составляют работники мясокомбинатов (боен). К счастью, при охлаждении мяса содержащиеся в нем бруцеллы частично погибают, однако большая частота случайных порезов и контактов с кровью и лимфой только что убитых животных обусловливают особенно высокий риск заражения бруцеллезом работников скотобоен. На Аляске отмечались случаи передачи бруцеллеза при употреблении сырого мяса оленей карибу и американских лосей.
В США бруцеллез чаще всего вызывает В. abortus, затем В. suis, реже — В. melitensis и В. canis. Примерно 2—3% случаев заражения бруцеллезом в
США происходит в лабораториях, часто среди ветеринарных врачей, которые инфицируются (через загрязненные иглы, путем попадания возбудителя на конъюнктиву или аэрогенным путем) живой вакциной. Заболевание, вызванное вакцинами, обычно протекает легко.
Патогенез и патологические изменения. Бруцеллы попадают в организм хозяина через поврежденную кожу и реже через ротоглотку, конъюнктиву или дыхательные пути. Они взаимодействуют с ссгментоядерными лейкоцитами (СЯЛ) и тканевыми макрофагами. Часть микроорганизмов фагоцнтируются, однако если инфицирующая доза достаточно велика, они проникают по лимфатическим сосудам в регионарные лимфатические узлы, чаще в подмышечные, шейные и надключичные. При дальнейшем распространении бруцеллы с током крови попадают в содержащие ретикулоэндотслиальные элементы органы и ткани, такие как костный мозг, печень и селезенка, а также в почки, кости, яички и эндокард. Бруцеллы могут размножаться в СЯЛ, тканевых макрофагах, а также в клетках ретикулоэндотелиальной системы и разрушать их. Благодаря внутриклеточной локализации бруцеллы защищены от воздействии антител и противомикробных препаратов.
Характерная, но не специфическая реакция тканой на присутствие бруцелл — это появление эпителиоидных клеток, гигантских клеток чужеродных тел и клеток Лангханса, а также лимфоцитов и плазмоцитов с формированием гранулем. Хотя значительная часть бруцелл уничтожается сегментоядерными лейкоцитами, основными клетками, вызывающими гибель возбудителя, являются макрофаги. В. abortus вызывает легко протекающее заболевание с формированием в печени и других ретикулоэндотелиальных органах гранулем без казеозного некроза. В. suis вызывает более тяжелые процессы с очаговыми гнойными осложнениями и гранулемами, которые могут подвергаться казеозному некрозу. Наиболее тяжелые формы бруцеллеза, способные привести к ннвалндизации больного, вызывает В. melitensis. Инфекция В. canis, как и В. abortus, носит достаточно легкую форму. Заживление гранулем при бруцеллезе происходит с формированием на их месте фиброзной ткани и кальцификации.
Хотя бруцеллез служит частой причиной абортов у крупного рогатого скота, свиней и коз, нет данных о том, что аборты у женщин при этой инфекции происходят чаще, чем при других бактерисмиях.
Клинические проявления. Бруцеллез может протекать бессимптомно и выявляться только по положительным результатам серологических реакций. Выраженные формы инфекции можно разделить на три группы — острый, локализованный и хронический бруцеллез.
Острый бруцеллез. Инкубационный период при этой форме инфекции обычно колеблется от 7 до 21 дня, но иногда продолжается и несколько месяцев. Начало может быть острым с выраженными явлениями интоксикации, особенно в случае инфекции, вызванной В. melitensis. Однако чаще болезнь развивается постепенно с небольшим подъемом температуры тела. Больные жалуются на недомогание, утомляемость, головную боль, слабость, повышенное потоотделение, озноб, боли в области поясницы, кашель, артралгии и миалгии при отсутствии признаков локальных поражений; возможна анорсксия и потеря массы тела.
Типичным является обилие жалоб при немногочисленности объективных данных. Из числа последних наиболее выраженными можно считать спленомегалию (у 10—20% больных), лимфаденопатию (у 15% больных) и гепатомегалию (менее чем у 10%).
Локализованный бруцеллез. Патологический процесс может локализоваться почти в любой анатомической области, однако наиболее часто отмечаются следующие формы заболевания -- остеомиелит, абсцесс селезенки, поражение мочеполовых органов, изменения в легких, эндокардит. Остеомиелит, как правило, поражает позвоночник, чаще пояснично-крестцовый отдел, с вовлечением в патологический процесс межпозвоночных дисков и прилежащих к ним позвонков. Ранние изменения в костях выявляются сканированием, в дальнейшем при рентгенографии обнаруживаются признаки остеопороза, эрозия передней пластинки позвонка и формирование остеофитов в виде «клюва попугая». Значительно реже наблюдаются артриты, в основном поражающие коленные суставы. В селезенке возможно развитие абсцессов, на месте которых впоследствии формируются участки обызвествления. Бруцеллы могут вызывать эпидидимоорхиты и реже клинически выраженные поражения предстательной железы или почек. К неврологическим осложнениям бруцеллеза относят менингоэнцефалит, миелит, радикулит или невропатию. Редкими клиническими проявлениями бруцеллеза являются экссудативный плеврит и пневмония.
Наиболее частая причина смерти больных при бруцеллезе — бактериальный эндокардит. Регистрируется он главным образом у мужчин, характеризуется вялым течением, часто сопровождается недостаточностью кровообращения и артериальной эмболией. Для полного излечения этой формы бруцеллеза требуется как хирургическая замена пораженных клапанов, так и терапия противомикробными средствами.
Хронический бруцеллез. К данной форме инфекции относят случаи заболевания, длящиеся более года после заражения. В эту группу включают больных с рецидивирующим течением болезни без признаков очаговой инфекции, в случае локализации инфекционного процесса в одном или нескольких органах, а также больных, у которых не наблюдается объективных признаков болезни (например, отсутствует лихорадка) и нет указаний на активный бруцеллез (согласно результатам серологических реакций и посевов на наличие бруцелл). Весьма вероятно, что у лиц, относящихся к этой группе, в основе жалоб на утомляемость и общую слабость лежат цсихоневротические нарушения, а не активный бруцеллез.
У ветеринарных врачей, занимающихся удалением плаценты у инфицированных животных, встречается необычное проявление инфекции — появление на кистях рук эритематозных, папулезных или пустулезных высыпаний, происхождение которых, возможно, связано с реакциями повышенной чувствительности к антигенам бруцелл.
Диагноз. Бруцеллез--относительно редкое заболевание, и имеется ряд болезней, имеющих сходные с ним клинические признаки: например, грипп, инфекционный мононуклеоз, токсоплазмоз, вирусный гепатит, генерализованная гонококковая инфекция, ревматизм, системная красная волчанка, туберкулез, лептоспироз и брюшной тиф. При наличии соответствующей клинической картины есть больше оснований предположить инфицированность бруцеллами у фермеров, работников скотобоен, а также у других лиц, имеющих контакты с контаминированным сырьем и продуктами животного происхождения.
Основное доказательство наличия бруцеллезной инфекции заключается в выделении возбудителя. Следует помнить о том, что проведение посевов инфицированного материала может представлять опасность для персонала лабораторий. Весь посевной материал должен быть четко маркирован «возможен бруцеллез», и все манипуляции с ним должны проводиться в стерильных условиях в специальном вытяжном шкафу, соответствующем требованиям для работы с инфекциониыми агентами III класса. В лабораториях, не имеющих указанных условий, выделение и культивирование бруцелл проводить не рекомендуется.
Культивирование бруцелл. Примерно в 50% случаев при посевах крови, взятой на ранних стадиях болезни от не получавших антибиотики больных, в триптиказный соевый бульон и культивировании их в присутствии 5—10% двуокиси углерода через 1—3 нед удается получить чистую культуру бруцелл. Однако во многих лабораториях посевы крови уничтожаются после 10-дневной инкубации. Поэтому лечащий врач должен сообщить в лабораторию и подозрении на бруцеллез и убедить врача-лаборанта наблюдать за подобными посевами не менее 4 нед. При остром течении болезни в ряде случаев при посевах крови получают отрицательный результат, а при посевах костного мозга — положительный. На более поздних стадиях- болезни бактериемия отмечается реже, и в этом случае возбудитель может быть выделен из инфицированных лимфатических узлов или из гранулем н селезенке, печени и костной ткани. В целом диагноз бруцеллеза подтверждается результатами посевов только в 15—20% случаев. При установлении диагноза локализованных форм инфекции может возникнуть необходимость в проведении биопсии для выделения возбудителя. В большинстве случаев заболевания диагноз ставят на основании результатов серологических исследований.
Серологические исследования. Повышение титров антител начинается в течение 1-й недели болезни, достигая пика к 3-му месяцу, и затем в течение нескольких месяцев снижаются. Иммуноглобулины этого класса способны сохраняться в организме сроком до нескольких лет. Антитела IgG появляются на 2—3-й неделе от начала заболевания, титры их достигают максимума примерно через 8 нед и сохраняются весь период активной инфекции, благодаря чему они свидетельствуют о продолжающемся активном инфекционном процессе. На фоне проводимого лечения титры антител IgG быстро снижаются и в течение года приближаются к нулю. В случае рецидивов уровни антител IgM и IgG повышаются. Самым надежным серологическим тестом является реакция агглютинации (РА) с бруцеллами в пробирке, посредством которой определяют уровень антител, реагирующих главным образом с липополисахаридными антигенами бруцелл. Увеличение титров антител в 4 и более раз в пробах сыворотки крови, полученных с интервалом 1—4 нед, свидетельствует о недавнем контакте с антигенами бруцелл или сходных с ними микроорганизмов. Реакции должны проводиться с обеими пробами одновременно в одной и той же лаборатории при одинаковых условиях. По данным реакции агглютинации, у большинства больных повышение титров специфических антител отмечается на I—2-й неделе заболевания, а на 3-й неделе фактически у всех происходит сероконверсия. Причиной ложноположительных результатов могут служить проведение кожной пробы на бруцеллез, вакцинация против холеры, а также инфекции, вызванные холерным вибрионом, Francisella tularensis или Yersinia enterocolitica. Причины указанных перекрестных реакций обычно легко выявляются.
Значение результатов серологических исследований. Повышение титров антител в РА до 1: 160 и выше свидетельствует о контакте с антигенами бруцелл или перекрестно реагирующих с ними возбудителей в прошлом или настоящем времени. При достаточно обоснованном подозрении на бруцеллез реакцию следует ставить сывороткой, разведенной до 1:1280, поскольку при наличии блокирующих антител в титрах 1:640 отмечаются ложноотрицательные результаты. Фактически все больные с бруцеллезом имеют положительные результаты в РА в титре ^1:160. Более низкие титры не имеют диагностического значения.
Агглютинирующие антитела IgG можно определить в РА путем экстрагирования с 2-меркаптоэтанолом (2-МЭ). При этом агглютинирующие антитела IgM разрушаются, что позволяет определить активность только агглютинирующих антител IgG. Наличие однократного повышения титра (>1:160) в РА с бруцеллами с использованием 2-МЭ является надежным объективным указанием на текущую или имевшую недавно место инфекцию и необходимость проведения лечения. В большинстве случаев даже после предполагаемого полного излечения в течение нескольких лет сохраняется повышенный уровень агглютинирующих антител IgM. Благодаря этому РА с бруцеллами с использованием 2-МЭ, позволяющая определять уровень только антител IgG, является самым надежным индикатором излечения больного.
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 176; Нарушение авторских прав?; Мы поможем в написании вашей работы!