
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Урок: Ковалентная полярная связь 7 страница
|
|
|
|
11. Шувалова Н.Н. Административная этика / Н.Н. Шувалова: Учеб. Пособие. – 2012. – 79 с.
12. Этика государственного служащего / Рос. акад. гос. службы при Президенте РФ; Подгот. Араповой Н.П. и др.; Отв. ред. Г.И. Иванов. – М.: Издательство РАГС, 2013. – 183 с.
13. Этика деловых отношений. / Под ред. Кибанова М., Инфра-М, 2013, 360 с.
[1] Ботавина Р.Н.Этика деловых отношений: Учебное пособие для вузов / Р.Н. Ботавина – М.: Финансы и статистика, 2012. – 206с.
[2] Этика государственного служащего / Рос. акад. гос. службы при Президенте РФ; Подгот. Араповой Н.П. и др.; Отв. ред. Г.И. Иванов. – М.: Издательство РАГС, 2013. – 183 с.
[3] Ботавина Р.Н.Этика деловых отношений: Учебное пособие для вузов / Р.Н. Ботавина – М.: Финансы и статистика, 2012. – 206с.
[4] Этика государственного служащего / Рос. акад. гос. службы при Президенте РФ; Подгот. Араповой Н.П. и др.; Отв. ред. Г.И. Иванов. – М.: Издательство РАГС, 2013. – 183 с.
1. Введение понятия ковалентной полярной связи
Тема сегодняшнего урока «Ковалентная полярная связь». На прошлом уроке вы познакомились с моделью химической связи, которая реализуется в простых веществах-неметаллах. Такой вид связи называется «ковалентная неполярная связь».
Сегодня вы узнаете о другом виде ковалентной связи, которая образует молекулы сложных веществ.
2. Ковалентная полярная связь в молекуле хлороводорода
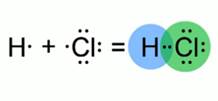
Рис. 1. Образование молекулы хлороводорода
Зная, что ковалентная связь образуется за счет общих электронных пар, изобразим модель молекулы хлороводорода. Атом водорода имеет на внешнем электронном слое всего один электрон. Атом хлора – семь электронов. Эти атомы приобретут энергетически выгодное состояние, если атому водорода будет принадлежать два электрона, а атому хлора – восемь. Такое возможно при образовании одной общей электронной пары.
Связь, образующаяся между водородом и хлором, в молекуле хлороводорода отличается от той химической связи, которая реализуется в молекулах простых веществ водорода и хлора. Это подтверждают экспериментальные данные. Например: атом водорода в молекуле HCl, может замещаться на атомы металла, а раствор хлороводорода в воде проводит электрический ток.
2HCl + Zn = ZnCl2 + H2↑
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 134; Нарушение авторских прав?; Мы поможем в написании вашей работы!