
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Регулирование процесса твердения цементного раствора
|
|
|
|
Рассмотрение кинетики процесса гидратации цемента позволяет рассчленить его на отдельные этапы:
- растворение твердой фазы и образование пересыщенного раствора;
- образование из пересыщенного раствора зародышей новой фазы кристаллогидратов;
- образование коагуляционной и кристаллизационной структуры.
Наиболее медленной стадией всего суммарного процесса твердения цемента является первая - растворение твердой фазы, и именно эта стадии определяет суммарную скорость процесса твердения. Скорость растворения клинкерных минералов, а, следовательно, и скорость процесса твердения зависят от следующих факторов:
- удельной поверхности цемента;
- фазового состава цементного клинкера;
- водоцементного отношения;
- температуры гидратации;
- вида и количества добавок.
С увеличением удельной поверхности цемента увеличивается поверхность реакции гидратации:


где:  - константа равновесия;
- константа равновесия;
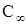 - растворимость исходной фазы;
- растворимость исходной фазы;
 - текущая концентрация;
- текущая концентрация;
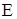 - энергия активации;
- энергия активации;
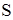 - удельная поверхность
- удельная поверхность
 - температура.
- температура.
В результате ускоряется появление новообразований. Кроме того, с повышением дисперсности цемента при постоянном В/Ц уменьшается расстояние между ними и в системе раньше образуются "стесненные" условия, приводящие к образованию коагуляционной и кристаллизационной структур. На этом принципе основано получение быстротвердеющих портландцементов, имеющих удельную поверхность в 1,5-2,0 раза большую по сравнению с обычными. В то же время слежавшиеся, комковатые цементы отличаются замедленными сроками твердения. С уменьшением активной удельной поверхности связано и замедление процесса твердения при добавке к клинкеру двуводного гипса.
При креплении высокотемпературных скважин практически всегда возникает вопрос о замедлении процессов структурообразования и твердения растворов с целью обеспечения нормального процесса цементирования. Наиболее широкое применение для этой цели находят добавки ПАВ, электролиты и их композиции. В этом случае отмечается эффект синергизма. Механизм замедления процесса твердения добавками ПАВ и электролитов одинаков - блокировка поверхности исходного цемента. Механизм же взаимодействия их с вяжущим может быть разным, например, добавки ПАВ блокируют поверхность, адсорбируясь на поверхности цемента моно- и полимолекулярным слоем, а добавки электролитов, являющихся хорошо растворимыми соединениями, вступают в химическую реакцию с Ca(OH)2, и уже уменьшение активной поверхности цементных частиц происходит за счет образовавшихся в результате этого взаимодействия малорастворимых соединений.
Кравцовьм В. М. и др. получено уравнение, позволяющее расчетным путем определить количество добавки для замедления процессов структурообразования на заданный промежуток времени:
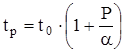 ,
,
где: 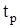 - начало схватывания раствора при введении добавки;
- начало схватывания раствора при введении добавки;
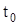 -начало схватывания раствора без добавок;
-начало схватывания раствора без добавок;
P - концентрация добавки, г/см3;
a - постоянная Лангмюра, г/см3.
Полученное уравнение справедливо для добавок, адсорбирующихся на поверхности твердой фазы мономолекулярным слоем, например, ССБ, Н3ВО3,. СuSO4 (рис.3,5). Для этих добавок процесс структурообразования описывается уравнением (3.5). При малых концентрациях добавки ССБ ее: молекулы адсорбируются, подчиняясь мономолекулярному механизму. Борная кислота и медный купорос - электролиты, взаимодействующие с Са(ОН)2. Для добавок, адсорбирующихся полимолекулярным слоем, уравнения более сложные и в настоящее время теоретически еще не получены.
Скорость гидратации составляющих цементного клинкера определяется их химической активностью. Быстрее других протекают реакции гидратации трехкальциевого алюмината, в то же время гидратация белита при нормальных температурах очень замедлена. На рис. 3.6 приведены результаты исследований по изучению прочностных свойств мономинералов, являющихся основными составлявшими портландцемента. Показано, что главными носителями прочности являются гидросиликаты кальция.
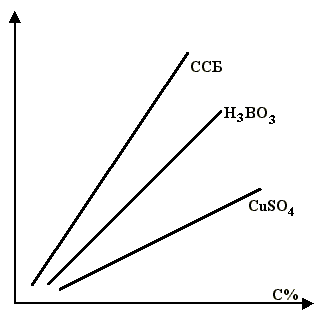
Рис. 3.5. Влияние замедляющих добавок на сроки схватывания раствора из портландцемента при температуре 90°С.
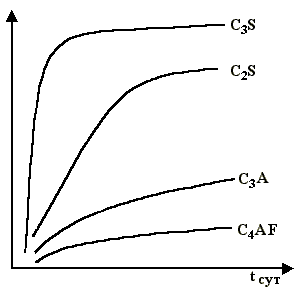
Рис. 3.6. Влияние времени твердения на прочностные свойства камня из мономинералов.
Гидроалюминаты кальция имеют низкую прочность, однако, набирают максимальную прочность на ранних стадиях твердения и именно они определяют скорость структурообразования и твердения цемента на ранних стадиях. Поэтому цементы с повышенным содержанием алюминатов и алита относятся к. быстротвердеющим, а цементы, с увеличенным содержанием белита - медленнотвердеющим и применяются, в основном, в интервалах повышенных температур.
При применении цементов полиминерального состава следует также учитывать тепловыделение в процессе гидратации вяжущего. По интенсивности тепловыделения клинкерные минералы располагаются в такой последовательности: С2 - 206 Дж/г; С4АГ - 419 Дж/г; С3 - 502 Дж/г; С3А - 867 Дж/г.
Этот факт необходимо учитывать особенно при креплении скважин в зоне многолетнемерзлых пород.
Влияние водоцементного отношения на скорость твердения достаточно существенно. При постоянном фазовом составе клинкера уменьшенное содержание воды приводит к более быстрому образованию необходимого пересыщения раствора и возникновению "стесненных" условий, а следовательно, к ускорению сроков схватывания растворов. Этот факт может иметь место лишь при низких водоцементных отношениях (В/Ц = 0,3), а при В/Ц, используемых в практике цементирования скважин (0,45-0,55), изменение сроков схватывания при уменьшении В/Ц не столь значительно. В то же время, эффект ускорения твердения при снижении В/Ц может иметь место в скважинах против проницаемых отложений, когда из-за отфильтровывания в пласт жидкости затворения, возможны серьезные нарушения процесса цементирования - увеличение давления на цементировочных агрегатах. Положительная сторона этого явления нашла применение при создании пакер - фильтров.
Наибольшее влияние на скорость твердения цементных растворов оказывает температура твердения. При повышении или понижении температуры резко изменяется константа скорости растворения К, что в свою очередь, изменяет скорость растворения вяжущего, и, следовательно, скорость твердения раствора.
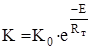
При креплении глубоких скважин большинство рассмотренных выше факторов являются фиксированными, т.е. независимыми от исполнителей. Температура в скважине определяется геологическими особенностями разреза, удельная поверхность и фазовый состав вяжущего - технологией изготовления. Такимобразом, наиболее приемлемый путь оптимизации свойств, цементного раствора - это ввод добавок регуляторов твердения. Влияние добавок замедлителей было рассмотрено выше. Остановимся на добавках - ускорителях твердения и механизме их действия. Повышение скорости растворения вяжущего может достигаться уменьшением энергии активации - потенциальной энергии, препятствующей началу химической реакции. Физический смысл "энергии активации" можно проиллюстрировать схемой, показанной на рис. 3.7.
По оси ординат отложены значения суммарной энергии системы до реакции Е1 и после реакции Е2. Таким образом, разность Е=Е1 - Е2 характеризует термодинамическое условие, необходимое для самопроизвольного протекания химической реакции. Однако на ее пути имеется энергетический барьер Е (или Е1), преодолев который можно осуществить реакцию. Таким образом, энергия активации реакции - это та избыточная энергия, которую нужно приложить, чтобы реакция началась.
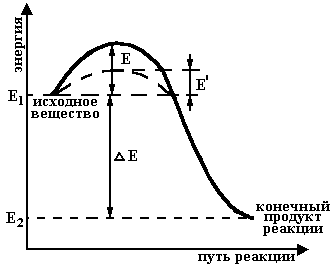
3.7. Схема, объясняющая понятие потенциального энергетического барьера.
В принципе этот процесс можно сравнить с энергией для поднятия в гору шара, который уже затем сам скатится с горы. Увеличение температуры обеспечивает энергию, необходимую для преодоление этого барьера. При постоянной температуре процесса, когда для преодоления барьера энергия извне не сообщается, процесс твердения может быть ускорен уменьшением барьера, для этой цели используется различные виды добавок.
Механизм воздействия добавок в тампонажный раствор весьма сложен, отдельные его аспекты еще полностью не выяснены. Попытки объяснения влияния различных добавок зачастую противоречат друг другу и не раскрывают природы провеса. Поэтому они не могут служить основанием при разработке методики универсального подхода к регулированию процессов структурообразования и обоснования выбора реагентов. Сказанное обусловлено прежде всего отсутствием единого мнения относительно механизма твердения, значительным влиянием условий исследований и другими факторами.
Исследованиями Ребиндера показана возможность управления процессами структурообразования при схватывании и твердении добавками ПАВ и электролитами.
ПАВ изменяют течение всего процесса твердения. В начальный период гидратации они повышают растворимость исходных частиц цемента за счет их химического диспергирования и пептизации. При коллоидации, когда дальнейшее растворение частиц в насыщенном растворе замедляется, ПАВ, образуя адсорбционные пленки на поверхности исходного материала, замедляет их гидратацию, а на поверхности новообразований изменяет величину силы взаимодействия между частицами новообразований и тем самым изменяет в ту или иную сторону скорость образования кристаллизационной структуры.
Ускорение сроков схватывания под действием электролитов некоторыми исследователями объясняется коагуляционным действием за счет изменения двойного электрического слоя. Так, например, Аяпов У. С. считает, что главная причина ускорения сроков схватывания при введении электролитов это повышение концентрации коагуляционных катионов AI3+, Са2+ и т.п. Механизм этого явления представляется следующим образом: неорганические электролиты образует на поверхностях зерен вяжущего ионные оболочки, толщина и заряд которых определяется как концентрацией ионов в жидкой фазе, так и их свойствами и. в первую очередь валентностью. С увеличением содержания электролитов 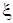 - потенциал уменьшается, цементные частицы коагулируют.
- потенциал уменьшается, цементные частицы коагулируют.
По мнению Ребиндера, действие электролитов сводится только к уменьшению 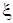 - потенциала. Они влияют и на растворимость новообразований, а следовательно, на пересыщение и кинетику кристаллизации, либо непосредственно участвуют в химическом процессе гидратации с возникновением новых высоководонасыщенных комплексных гидратов, образование которых интенсифицирует диспергирование и ускоряет твердение.
- потенциала. Они влияют и на растворимость новообразований, а следовательно, на пересыщение и кинетику кристаллизации, либо непосредственно участвуют в химическом процессе гидратации с возникновением новых высоководонасыщенных комплексных гидратов, образование которых интенсифицирует диспергирование и ускоряет твердение.
Так установлено, что CaCI2 ускоряет процесс гидратации и структурообразование силикатов кальция,не вступая с ними в химическое взаимодействие. Его влияние объясняется снижением величины метастабильной растворимости силикатов кальция, а на процессы структурообразования алюминатов кальция - образованием нового соединения гидрохлоралюмината кальция. Аналогичное положение отмечено и для хлоридов калия и натрия.
В. Эйтель отмечает, что ускорители, и в частности хлорид кальция, понижают концентрации ионов гидроксила в растворе и усиливают растворимость реагирующих силикатов и алюминатов, в результате чего происходит быстрое осаждение частиц. Небольшие добавки. CaCl2 оказывают замедляющее действие за счет образования двойной комплексной соли.
Результатами исследований установлено, что скорость твердения сокращается:
- вследствие нейтрализации щелочей, содержащихся в цементе;
- снижения пересыщения гипсом под действием добавок - готовых центров кристаллизации;
- образования комплексных солей алюминатов кальция;
- катализа образования гидросульфоалюмината;
- модифицированной кристаллизации С3АН6
Замедление же процессов твердения будет происходить:
- в результате повышения рН 12;
- пересыщения раствора гипсом;
- образования нерастворимых соединений на поверхности цементных частиц и новообразований;
- модифицирования кристаллизации С3АН.
Установлено,что ускорение в основном обусловлено: коагулирующим воздействием вводимых ионов; интенсификацией растворимости клинкерных, минералов; образованием новых центров кристаллизации, снижением рН среды.
Замедление определяется в основном поверхностной активностью замедлителей. Под этим понимается способность молекул или ионов этих реагентов адсорбироваться под действием меж- и внутримолекулярных сил у поверхности раздела фаз. Абсорбция может быть как физическая так и химическая. Первая обусловлена Ван-дер-ваальсовыми силами, вторая - ионными и ковалентными связями. Образующиеся соединения блокируют активные центры дисперсной фазы и тормозят процессы схватывания и твердения.
В результате исследований механизма физико-химического воздействия добавок на гидратационное твердение вяжущих материалов предложен ряд их классификаций. Так, например, В. Гансеном, замедлители классифицируются на:
- крахмал или продукт целлюлозы, сахара;
- оксикислоты и их смеси.
Основываясь на том, что все рассмотренные вещества содержат группу
НО-С-Н, он делает вывод, что благодаря ей эти органические соединения действуют как. Замедлители. Механизм их влияния он также объясняет возникновением защитного слоя на поверхности алюминатов и силикатов кальция, препятствующий реакции с водой.
Стейнер Г. большую роль отводит в образовании защитного слоя группе ОН. На примере спиртов, сахаров и других добавок, он показал возрастание эффективности замедлителей с увеличением числа групп ОН в составе их молекул.
Вивнак Г. и Таплин Д. дополняют влияние замедлителей карбоксильной группой. По их мнению органические замедлители проявляют высокую активность при наличии в молекуле, двух атомов кислорода, связанных с близлежащими атомами углерода следующим образом НО-С-С = 0. При этом они не делают различия между тем как атом кислорода связан с атомом углерода.В одном случае может входит в состав карбоксильных в другом - альдегидной группы.
Каких либо детальных исследований по подтверждению своих выводов они не приводят, не дано объяснение различной активности реагентов, содержащих группу НО-С-С-Н. Не объяснено отсутствие замедляющего действия щавелевой и молочной кислоты, нет анализа между вводимыми реагентами и продуктами твердения и, поэтому эти исследования широкого развития не получили
Рахимбаев Ш. М и Баш С. М. предложили также классифицировать добавки по составу функциональных групп, но получилось, что в одной группе располагаются вещества, отличающиеся по составу, свойствам, эффективности и поэтому эта классификация тоже оказалась не приемлемой.
Анализ литературных данных позволяет установить, что механизм замедления в основном объясняется образованием защитного слоя и при этом значительную роль играют внутрикомплексные соединения, интенсивность которых обуславливается характером связей, возникающих между ними и реакционноспособными ионами кристаллической решетки клинкерных минералов. Наиболее важные характеристики иона - комлексообразователя - его размер, потенциал и электронная конфигурация. В зависимости от этих параметровон способен группировать вокруг себя атомы, ионы или молекулы, называемые лигандами или аддендами.
Комплексные соединения, в состав которых входят циклические группировки, включающие комплексообразователь называются хелатными (клешневидными). Внутрикомплексные соединения, полученные в результате взаимодействия Са, AI,Si, Fe цементных частиц с молекулами органических замедлителей схватывания, представляет собой хелаты, полидентатные лиганды которых сдержат группы, способные сочетаться с ионом-комплексообразователем одновременно двумя видами связей. Одни образованы за счет сил главной валентности с замещением катиона. К таким группам относятся карбоксильная, сульфановая, в некоторых случаях аминные (первичная и вторичная) группы. Другие - благодаря побочным валентностям, без замещения катиона. Это группы: спиртовый гидроксил, карбоксильная и т. д.
Устойчивость внутрикомплексного соединения зависит от величины и сопряженности цикла. Из них энергетически выгодны те, у которых сохраняются нормальные валентные углы и длины связей. Таким образом, устойчивость внутрикомплексных соединений зависит от пространственного построения циклов, числа членов в них, активности и количества групп, сочетающихся с центральным ионом силами главных и побочных валентностей. Замедлители схватывания,как правило, взаимодействуют с основными ионами минералов клинкера за счет карбоксильных, гидроксильных, аминных и амидных групп. Причем одна и та же группа может сочетаться с ионом комплексообразователя несколькими входящими в ее состав функциональными группами, образуя хелатные группы. Общее число связей называется координационным числом. На процесс комплексообразования существенное влияние оказывают пространственные факторы - размеры ионов, степень свободы пространственного перемещения функциональных групп и т.д. Учитывая изложенное, а также энергетическое состояние комплексообразующих атомов Мариамполъским Н. А. было показано:
1. Конфигурация молекул, расстояние между реакционноспособными атомами функциональных групп и звеньев главной цепи определяет способность вещества замедлять схватывание цементных растворов.
2. Замедляющий эффект проявляется во взаимодействии молекул реагирующего вещества с активными центрами кристаллической решетки за счет нескольким сил связей. Интенсивность действия реагента зависит от прочности образующих хемосорбционных хелатных соединений.
3. Наиболее благоприятным сочетанием групп в молекуле алифатическое строение являются - СНОН-СНОН-ССОН, - СНОН-СН2-СООН, -
CООH-CH-CООH.
С увеличением числа звеньев -НСООН- эффективность замедляющего действия оксикислот повышается. Включение в цепь вместо инактивных мостиков -СН2- звеньев, содержащих кислород и азот повышает активность добавки.
4. Алифатические соединения, в составе которых имеются только гидроксилы (спирты) не могутслужить в качестве замедлителей. Положение изменяется, если в молекуле содержится карбоксильная группа (сахара).
Вещества ароматического строения обеспечивает высокую эффективность замедления. При наличии карбоксилов, а также дополнительной гидроксильной аминной, амидной, карбоксильной групп. Увеличение числа ароматических ядер с указанными функциональными группами повышает активность реагента.
5. Вещества, являвшиеся эффективными заменителями, как правило, Отличаются способностью к образованию прочных внутрикомплексных соединений.
Изложенное послужило основой для классификации замедлителей на следующие 8 групп:
1. Оксиаминоалкилфосфоновые кислоты (оксиэтилы, дендифосфоновая, нитрилотриметилфосфоновая и их соли, образующие при гидратации минералов клинкера прочные клешневидные внутрикомплексные соединения - хелаты).
2. Окси, аминокислоты (виннокаменная, лимонная триоксиглутаровая, глюконовая, этилендиаминтетрауксусная и их соли - образуют также хелаты).
3. Сахара, которые за счет большого числа связей образуют вокруг зерен вяжущего пленки значительной прочности.
4. Фосфаты, бораты - реагирующие и связывающие с продуктами гидратации так же как и органические вещества предыдущей группыв основном благодаря наличию в составе гидроксильных групп.
5. Природные и синтетические танниновые реагенты, продукты на основе лигнина (ПФЛК, сулькор, пекор, синтан-5, нитролигник, ССБ), способные так же как и многоосновные окси и аминокислоты сочетаться с продуктами гидратации во внутрикомплексные производные.
6. Высокомолекулярные соединения - крахмал, КМЦ, полиакрилнитрил и другие подобные им, так называемые защитные полимеры, создающие вязкие слои на поверхности частиц, которые являются барьером для проникновения воды.
7. Двуводный гипс, и некоторые другие соединения кальция, которые сочетаются с гидратами клинкера в комплексные соли и образуют пленки на частицах.
8. ПА мылообразные вещества (сульфанол ОП-IO) значительноснижающие межфазовое натяжение и адсорбирующиеся на цементных зернах.
В практике крепления, скважин принята следующая классификация реагентов:
Добавки - пластификаторы. Раннее было показано, что высокое водоцементное отношение тампонажных растворов - одна из основных причин получения ухудшенной структуры затвердевшего камня. В строительной практике значительно раньше, чем в креплении скважин стали применять растворы и бетоны с пониженным водосодержанием. Для сохранения требуемой подвижности растворов при малом содержании, воды затворения применяются пластифицирующие добавки. Пластификаторами называют вещества, адсорбирующиеся на поверхности зерен цемента и уменьшавшие силу трения между ними. С другой стороны, введение пластификаторов, увеличивает смачивающую способность воды и понижает ее вязкость. Все это приводит к тому, что растворы необходимой подвижности могут быть получены, при значительно меньшем количестве воды затворения. В качестве пластификаторов применяются: сульфит - спиртовая барда (ССБ), конденсированная сулфит - спиртовая. барда (КССБ), полифенол лесохимический (ПФХЛ), дубители (Д-4 и Д-12) и др. Применяя их, можно получать, высокоподвижные тампонажные растворы с В/Ц равном 0,3 -0,35. Количество вводимой добавки составляет
от 0,1 до 1,0 % от веса сухого элемента. Поэтому на практике рекомендуют совместно с пластификаторами вводить реагенты пеногасители. В качестве пластификаторов широко используются поверхностно-активные вещества. Работами НИИцемента установлено, что адсорбция пластифицирующих ПАВ на поверхности твердой фазы цемента (C3) сопровождается ослаблением водородных связей между молекулами воды, прилегающими к адсорбционному слою, что и обуславливает пластифицирующее действие ПАВ. Освобождение части воды из потенциального слоя поверхности твердой фазы при адсорбции ПАВ на активных участках поверхности исходных минералов и продуктов гидратации вносит дополнительный вклад в пластифицирующий эффект.
Отсюда следует, что решающее воздействие на пластифицирующее действие ПАВ оказывает строение их молекул. Подтверждением этого являются результаты изучения влияния строения молекул ПАВ на их пластифицирующее действие, позволившие сформулировать пять основных условий пластификации:
- хемосорбция ПАВ на цементе и продуктах его гидратации;
- компенсация (уравновешивание) имеющихся и возникающих зарядов поверхности цемента противоположными по знаку зарядами из адсорбционного слоя ПАВ;
- проводимость адсорбционного слоя ПАВ;
- растворимость в воде;
- наличие в адсорбционном слое физически сорбированных молекул ПАВ.
Пластифицирующее действие ПАВ объясняется также высвобождением части воды из диффузионных слоев вокруг твердых частиц за счет замены в приповерхностном слое молекул воды на ПАВ и ослаблением связей твердой поверхности с водой.
ПАВ, адсорбируясь на поверхности зерен цемента, удаляют с нее тонкую воздушную пленку, благодаря чему повышается смачиваемость частиц. Вследствие освобождения некоторого количества воды, смесь разжижается. Пузырьки воздуха, как микрокатки, облегчают скольжение частиц, подобно тому, как это наблюдается для мелких зерен плавленой золы ("батавских слезок"), оказывающих заметное пластифицирующее действие на бетонные смеси. Однако Ж. Брюэр опроверг все эти умозрительные взгляды путем измерения пластифицирующего действия ПАВ в вакууме, показавшего, что воздушные пузырьки не оказывают заметного влияния на пластифицирующий эффект, если он наблюдается.
Кроме того, ПАВ приводит к пептизации твердых частиц, а пептизация приводит к двум эффектам, способствующим пластификации системы: разрушению агрегатов частиц, сопровождающемуся высвобождением части свободной воды, находящейся внутри них, и уменьшением коэффициента твердения.
Выделяют несколько групп ПАВ, применяемых в качестве пластификаторов цемента.
Первая группа включает в себя полимеры, полученные конденсацией с формальдегидом сульфированных, конденсированных полициклических бензолов и их аналогов или их водорастворимых солей.
Во вторую группу входят комплексные добавки, состоящие из2-3и более специально подобранных компонентов. Одним из компонентов является ПАВ, обладающие высокой пластифицирующей способностью. Другим компонентом в состав добавки могут входить: пеногасители, замедлители схватывания, ускорители твердения цемента и т.д., выбираемые в зависимости от назначения-добавки.
Третья группа включает в себя технические ЛСТ и их модифицированные аналоги.
Наибольший интерес представляют добавки I и 3 групп. За рубежом широко применяется ряд суперпластификаторов на основе маламин- и нафталинформальдегидных смол: мелмент - 10, майти ББП-1, сульфометиламин, алкиломин, меламиноформальдегидный поликонденсати др.
В СССР известны аналогичные продукты: С-3, МФ-АР, 10-03, 40--03, дофен, из которых наибольшее применение получила добавка С-3. Более подробно о ПАВ будет изложено ниже, поскольку они выделены в отдельную группу.
К следующей группе относятся добавки, влияющие на процесс твердения тампонажного раствора.
Влияние некоторых добавок на процессы твердения гипса и портландцемента уже рассматривалось. Однако большое количество добавок и различный механизм влияния на процесс твердения вызывают настоятельную необходимость более подробно остановиться на них.
Исходя из механизма действия добавки можно условно разделить на четыре класса: первый - добавки, изменяющие растворимость вяжущих веществ и не вступающие с ними в химическую реакцию; второй - добавки, реагирующие с вяжущим с образованием труднорастворимых или малодиссоциирующих соединений; третий - добавки - готовые центры кристаллизации; четвертый - добавки, адсорбирующиеся на поверхности зерен вяжущих.
Добавки первого класса
Добавки первого класса можно разделить на две группы. К первой относятся соли, не содержащие одноименных с вяжущим ионов. В качестве примера нами уже рассматривалось влияние повареннойсоли на твердение гипса. Подобным же эффектом по отношению ксиликатной части портландцемента обладают хлориды натрия и калия,азотнокислый натрий и некоторые другие соли. Все эти, добавки повышают растворимость исходного вяжущего, увеличивают степень пересыщения раствора, благодаря чему ускоряются процессы твердения. Следует отметить, что добавки первого класса не должны понижать щелочность раствора, т.е. быть солями сильных оснований.
Ко второй группе добавок рассматриваемого класса относятся вещества, содержащие одноименные с вяжущим ионы, например, соли кальция (хлорид, нитрид, нитрат и др.) при действии их на гипс, алит, белит, Эти добавки в малых количествах понижают растворимость вяжущих. Их действие как ускорителей твердения, по-видимому, обусловлено тем, что они увеличивают скорость кристаллизации новообразований из раствора.
Добавки второго класса
Напомним, что к тому классу добавок отнесем вещества, реагирующие с вяжущим с образованием труднорастворимых или малодиссоциируемых соединений. Добавки второго класса можно разделить на три группы. К первой относят вещества, вступающие с жидкой фазой цемента в реакцию нейтрализации, т.е. уменьшающие щелочность среды. В эту группу добавок попадают кислоты (например соляная кислота, иногда вводимая как ускоритель твердения) и гидролизующие соли сильной кислоты и слабого основания, в основном соли многовалентных металлов, например хлорное железо или сернокислый алюминий. Гидролиз подобных солей сопровождается увеличением кислотности, т.е. понижением рН среды за счет образования полностью диссоциированной сильной кислоты:
1) 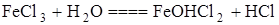 ;
;
2) 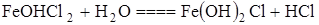 ;
;
3) 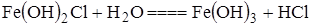 ;
;
или суммарно в ионной форме:
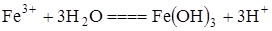
На последней стадии гидролиза образуются труднорастворимые гидрооксиды металлов, способные кольматировать поры цементного камня.
Обoим признаком добавок первой группы этого класса является их способность к реакциям нейтрализации с щелочью поровой жидкости цементного камня и образование труднорастворимых многовалентных оснований.
В дальнейшем гидрооксиды амфотерных; веществ, взаимодействуя с гидрооксидом кальция, находящимся в поровой жидкости цементного камня, образуют комплексные соли:

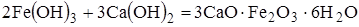
Добавки этой группы весьма перспективны, т.к. они не только ускоряют твердение цемента и понижают проницаемость цементного камня, но и придают ему другие ценные свойства. Например, некоторые соли трехвалентного железа увеличивают деформативность цементного камня. Из числа добавок этой группы широкое применение имеют хлорное железо, сульфаты трехвалентного железа и алюминия.
Ко второй группе добавок рассматриваемого класса относятся соли, вступающие с гидрооксидом кальция в обменные реакции с образованием труднорастворимых соединений, например, поташ (K2СО3), кальцинированная сода (Na2СО3), алюминат и фторид натрия. Реакции нейтрализации протекает по схеме:

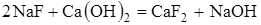
Существенным отличием этих добавок от добавок первой группы является то, что добавки второй группы повышают рН среды, как за счет обменной реакции, так и за счет гидролиза самой соли

Это весьма важный, фактор, т.к. понижение щелочности среды при использовании добавок первой группы, может вызвать коррозию обсадной колонны.
Из числа добавок второй группы широко используют кальцинированную соду, поташ, алюминат натрия. Помимо ускорения твердения они понижают температуру замерзания воды и могут использоваться при цементировании скважин в зоне многолетнемерзлых пород.
К третьей группе добавок второго класса относятся вещества, взаимодействующие с алюминий и железосодержащими фазами цемента, с образованием труднорастворимых комплексных солей. Основное отличие добавок этой группы - это участие в реакциях гидратации цемента и выкристаллизовывание комплексные солей - гидратов из пересыщенных растворов.
Следует оговорить, что нередко добавки третьей группы могут приводить к эффектам, характерным для других категорий добавок.
Представителями добавок этой группы являются СaSO4, CaCI2, Ca(NO3)2, NаNО2 и др. При взаимодействии с минералами - плавнями цементного клинкера они способны образовывать комплексные соли, хотя по отношению к силикатной, части клинкера часть рассматриваемых добавок может быть отнесена к первому классу.
Уравнения реакции взаимодействия добавок третьей группы второго класса с алюминатами и алюмоферритами кальция запишутся в виде:
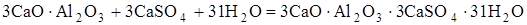


Соответственно при реакции алюмината и нитрата кальция выкристаллизовывается гидроалюминат кальция  отличающийся от гидроалюмината тем, что хлор внем заменен на группу
отличающийся от гидроалюмината тем, что хлор внем заменен на группу 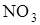 Близкие по составу и свойствам двойные соли (гидраты) образуются и при участии железосодержаших фаз, клинкера, например, гидросульфоферриты кальция
Близкие по составу и свойствам двойные соли (гидраты) образуются и при участии железосодержаших фаз, клинкера, например, гидросульфоферриты кальция 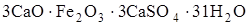 ;
;  Соответственно реагируют железосодержащие фазы цемента и-с другими добавками.
Соответственно реагируют железосодержащие фазы цемента и-с другими добавками.
Все рассмотренные соли - гидраты, осаждаясь на поверхности зерен цементов, могут тормозить процесс гидратации алюминатной и алюмоферритной фаз за счет создания экранизирующих пленок, ограничивающих доступ воды к зернам цемента.
В то же время известно, хлориды кальция, натрия, калия, азотнокислый кальций, карбонат кальция и др. способны к образованию с алюминатами кальция комплексных соединений и они относятся к ускорителям твердения. Это объясняется тем, что при совместном, присутствии в цементе двух или более перечисленных добавок они конкурируют между собой при взаимодействии с С3А и С4АР. При этом раньше взаимодействуют те добавки, которые с составляющими образуют наиболее труднорастворимые соли и за счет большего пересыщения кристаллизуются с большей скоростью. Поскольку в цементе всегда содержится гипс, а гидросульфоалюминат имеет меньшую растворимость по сравнению с другими комплексными солями, то именно гипс первым вступает в реакции взаимодействия с алюминатами кальция. В это время другие добавки, например CaCI2, Ca(NO3)2, оставаясь в жидкой фазе цементного раствора в виде соответствующих ионов, ускоряют твердение силикатной части клинкера, т.е. действуют как добавки первого класса.
Добавки третьего класса
К этому классу добавок относятся вещества, являющиеся готовыми центрами кристаллизации.
Механизм действия добавок можно объяснить следующим образом.
Ранее было показано, что для того, чтобы происходил процесс твердения вяжущих веществ, необходимо образование новой фазыизпересыщенного раствора. Для этого нужно затратить некоторую энергию образования зародыша. Она равна потенциальному барьеру, препятствующему формированию новой поверхности и играет ту же роль, что и энергия активации в кинетике химической реакции.
Процесс получения зародышей новой фазы значительно облегчается, если имеются границы раздела фаз, т.к. уменьшается поверхность новообразований и, следовательно, необходимо затратить меньшую энергию. Потенциальный энергетический барьер, необходимый для образования новой фазы уменьшается, причем в тем большей степени, чем больше границ твердой фазыи чем ближе по своим кристалло - химическим характеристикам материал, создающий эти границы, к аналогичным характеристикам возникающей новой фазы.
Этим объясняется ускорение процесса формирования камня из полуводного гипса при добавке к нему двуводного и ускоряющая роль песка, особенно тонкомолотого, в твердении цементов. Добавки гидросиликатов кальция могут существенно сократить сроки схватывания вяжущих гидротермального твердения, а добавки гидросульфоалюмината кальция - вяжущих сульфоалюминатного твердения.
Обычно рассматриваемые добавки вводятся в количестве 3-5 % и главным образом в тонкомолотом состоянии. Увеличение добавка свыше, 5 % не оказывает влияния на процесс твердения по сравнению, с ее меньшим количеством, но может снизить прочность полученного камня за счет уменьшения количества гидратной фазы.
Добавки четвертого класса
К этому классу добавок относятся поверхностно-активные вещества, адсорбирующиеся на поверхности зерен исходного, вяжущего. Это добавки-пластификаторы и гидрофобизаторы. Большинство добавок этого класса полифункциональны, т.е. наряду с пластификацией и гидрофобизацией они являются эффективными замедлителями твердения.
ПАВ это вещества, способствующие снижению поверхностного натяжения вследствие адсорбции и ориентации молекул на поверхности раздела фаз. Они характеризуются незначительной величиной максимально возможной концентрации их в растворе в молекулярной форме, способностью образовывать мицеллы выше определенной концентрации - КЛМ, связанной с уменьшением свободной энергии системы, а также солюбизацией водонерастворимых веществ внутри мицелл. ПАВ в основном органические соединения, их молекулы имеют дифильное строение, т.е. содержат лиофильные и лиофобные группы атомов. Гидрофильные группы способствуют растворению ПАВ в воде, гидрофобные - в неполярных средах. При адсорбции ПАВ гидрофильные группы ориентируются в сторону полярной фазы (водной), а гидрофобные - в сторону неполярной.
Гидрофильная, полярная группа обладает значительным дипольным моментом и хорошо гидратируется, что обуславливает сродство ПАВ к воде. К ПАВ-ам относят многие органические соединения: жирные кислоты, соли этих кислот, сульфокислоты и их соли, спирты, амины. Гидрофобная углеводородная группа является причиной пониженной растворимости этих соединений.
Полярной частью молекул ПАВ могут быть группы с высоким дипольным моментом: -СООН, -ОН,. -NH2, -NSH, -SN, -NO2, -NCS, -CHO, -SO3H
Неполярной частью ПАВ служат алифатические или ароматические углеводородные радикалы. При этом длина радикала в значительной степени определяет поверхностную активность молекулы.
По способности к диссоциации в водных растворах ПАВ разделяет на ионогенные и неионогенные. Первые диссоциируют в растворе на ионы, одни из которых поверхностно-активные, а другие не обладают поверхностной активностью. В зависимости от знака заряда ионогенные подразделяются на анионные, катионные, амфотерные (амфолитные).
Анионные ГАВ диссоциируют в воде с образованием поверхностно-активных анионов, которые, адсорбируясь на поверхности, заряжают ее отрицательно. К этому типу относят карбоновые кислоты и их соли (мыла), сульфокислоты и их соли с многозарядными катионами, алкисульфаты, фосфаты.
Катионные ПАВ диссоциируют в воде с образованием поверхностно-активных катионов, которые, адсорбируясь на поверхности, заряжают ее положительно. К этому типу относят соли первичных, вторичных, третичных аминов, а также соли алкилзамещенных аммониевых оснований.
Амфотерные ПАВ, содержат две функциональные группы. Они в зависимости от рН среды обладают анион-активными или катион-активными свойствами.
Неионогенные ПАВ - вещества, молекулы которых в растворах не диссоциируют на ионы. Их молекулы состоят из длинной углеводородной цепочки с несколькими полярными не ионными группами на конце, которые и обуславливают растворимость в воде. К этому типу ПАВ относят оксиэтилированные жирные кислоты с различной длиной оксиэтиленовой цепи. Такие ПАВ позволяют при синтезе регулировать гидрофильность путем изменения длины оксиэтиленовой цепи.
Дифильные ПАВ делят на истинно растворимые и коллоидные.
Истинно растворимыми в воде являются органические соединения с небольшим углеводородным радикалом (низшие спирты, фенолы, кислоты, их соли), находящиеся в растворе в молекулярно-дисперсном состоянии вплоть до концентрации их истинной растворимости.
Коллоидные ПАВ способны образовывать термодинамические устойчивые гетерогенные дисперсные системы. Они обладают высокой поверхностной активностью и малой истинной растворимостью. При некоторой концентрации (ККМ) они склонны к мицеллообразованию. Вследствие этого общая растворимость ПАВ, обусловленная образованием наряду с истинным коллоидного раствора, резко, увеличивается. Молекулярная же растворимость остается постоянной.
Поэтому ККМ является характеристикой, определяющей свойства ПАВ - изменение термодинамических функций при мицеллообразовании, зависимость поверхностного натяжения от концентрации ПАВ, влияние добавок на активность ПАВ.
Одна из важных характеристик коллоидных ПАВ - соотношение двух противоположных групп молекул гидрофильной и гидрофобной, называемое гидрофильно - липофильным баллансом (ГЛБ). Он позволяет количественно оценить и выразить в виде условных групповых чисел степень взаимодействия с водой отдельных групп, составляющих ПАВ. Гидрофильные группы имеют положительные групповые числа, а гидрофобные - отрицательные. Чем выше гидрофильность, тем больше ГЛБ, ГЛБ определяет область применения ПАВ.
Поскольку ПАВ изменяют поверхностный заряд, то они оказывают значительное влияниеи на свойства цементного раствора, и формирующегося из него камня.
Добавки органического и неорганического происхождения, вводимые в состав тампонажного раствора на различных стадиях его приготовления, способствуют изменению структуры за счет адсорбционного модифицирования гидратных новообразований, формирующихся при гидратации вяжущего. Они также повышают подвижность раствора, снижают водопотребность, уменьшают водоотделение, повышают морозостойкость и коррозионную стойкость затвердевшего камня, изменяют сроки схватывания.
ПАВ, адсорбция которых на поверхности частиц цемента вызывает дополнительную пептизацию и облегчает диспергирование в водной среде, а также повышает их устойчивость по отношению к процессам коагуляции относятся к гидрофилизирушим или гидрофильным. Другая группа ПАВ, адсорбция которых сопровождается, химической фиксацией их полярных групп с образованием на поверхности частиц нерастворимых в воде соединений относятся к гидрофобизирующимся или гидрофобным.
Гидрофильные ПАВ это соли лигносульфонатов с большим содержанием сахаров, СДБ, глюкозы, глюконата натрия.
Гидрофобизирующие ПАВ - олеиновая кислота, нафтеновые мыла.
Пластифицирующее действие гидрофилизирующих ПАВ обеспечивается образованием на поверхности твердой фазы и новообразованиях адсорбционной пленки, которое удерживает на поверхности достаточно толстый слой воды, связанный с поверхностью молекулярными силами. Образованные таким образом адсорбционно-гидратные оболочки снижают силы сцепления между частицами, повышая подвижность цементно-водной дисперсии, а также замедляют процесс гидратации цемента, вследствие замедления скорости взаимодействия цементных частиц с жидкостью затворения из-за увеличения диффузионных сопротивлений.
Пластифицирующее действие ПАВ, повышается при переходе от неионогенных к анионоактивным. Большей активностью обладают ПАВ, активные полярные группы которых реакционноспособны к гидратирующимся зернам цемента, а радикальные группы имеют линейную структуру с повышенной молекулярной массой. Такие ПАВ называют суперпластфикаторами. Принято считать, что ПАВ, снижающие водопотребность в предела 5 - 20 % относят к обычным пластификаторам, а ПАВ, снижающие водопотребность на
20 - 30 % - к суперпластификаторам. Последние подразделяются на:
1. - сульфированные меламинформальдегидные соединения и комплексы на их основе;
2. - сульфированные нафталинформальдегидные соединения и комплексы на их основе;
3. - модифицированные, не содержащие сахаров, лингосульфонаты;
4 - производные оксикарбонатовых кислот.
Цементно - водная суспензия характеризуется удельной, поверхностью дисперсной фазы около 300 м2 /кг, размером частиц цемента, в предела 10-4¸ 10-6м и меньше, удельной поверхностью, гидросиликатного геля около 2 ´ 105 м2/кг при расстоянии между частицами 15 ¸ 30 ´ 10-10м, что значительно меньше толщины двойного электрического слоя частиц дисперсной фазы.
-потенциал цементно-водной суспензии при pH = 12 ¸ 13 при введении ПАВ изменяется от 11 до 25 ¸ 30 мВ. Вследствие электрических поверхностных явлений происходит экранирование сил межмолекулярного притяжения, обеспечивая дефлокуляцию цементных частиц и их агрегативную устойчивость.
Дефлокуляция гидратированных частиц цемента способствует высвобождению иммобилизованных флокулами молекул воды, увеличивая общий объем дисперсной среды, снижая вязкость цементной суспензии, что обуславливает ее разжижение.
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 3934; Нарушение авторских прав?; Мы поможем в написании вашей работы!