
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физические свойства нормальных алканов
|
|
|
|
| Название | Химическая формула | Температура кипения, 0С | Температура плавления, 0С | Плотность ρ420 |
| Метан | СН4 | - 161,6 | - 182,5 | 0,424 |
| Этан | С2Н6 | - 88,6 | -183,2 | 0,546 |
| Пропан | С3Н8 | - 42,2 | - 187,6 | 0,585 |
| Бутан | С4Н10 | - 0,5 | - 133,3 | 0,579 |
| Пентан | С5Н12 | 36,1 | - 129,7 | 0,626 |
| Гексан | С6Н14 | 68,8 | -95,3 | 0,659 |
| Гептан | С7Н16 | 98,4 | -90,6 | 0,684 |
| Октан | С8Н18 | 125,7 | -56,8 | 0,703 |
| Нонан | С9Н20 | 149,5 | -53,6 | 0,718 |
| Декан | С10Н22 | 173,0 | -30,3 | 0,730 |
| Ундекан | С11Н24 | 195,8 | -25,6 | 0,740 |
| Додекан | С12Н26 | 214,5 | -9,6 | 0,745 |
| Тридекан | С13Н28 | 234,0 | -6,0 | 0,757 |
| Тетрадекан | С14Н30 | 252,5 | 5,5 | 0,764 |
| Пентадекан | С15Н32 | 270,5 | 10,0 | 0,769 |
| Гексадекан | С16Н34 | 287,0 | 18,1 | 0,775 |
| Октадекан | С18Н38 | 317,0 | 28,0 | 0,777 |
| Эйкозан | С20Н42 | 344,0 | 36,5 | 0,778 |
| Пентакозан | С25Н52 | 259/2кПа | 53,3 | - |
| Триаконтан | С30Н62 | 304/2 кПа | 65,9 | 0,780 |
| Пентатриаконтан | С35Н72 | 331/2 кПа | 74,6 | 0,781 |
| Тетраконтан | С40Н82 | - | 80,8 | - |
| Пентаконтан | С50Н102 | 421/2 кПа | 93,0 | - |
Согласно номенклатуре ИЮПАК названия разветвлённых алканов составляют следующим образом:
1. В молекуле углеводорода выбирают главную цепь – самую длинную:

2. Затем эту цепь нумеруют с того конца, к которому ближе заместитель
(радикал, имеющий меньшее число углеродных атомов):

3. Углеводород называют в таком порядке: вначале указывают место
(цифрой) расположения заместителя, затем этот заместитель, а в конце – добавляют название главной (самой длинной) цепи. Вышеприведённый углеводород может быть назван: 2-метил-4-этилгептан.
Если в главной цепи содержится несколько одинаковых заместителей, то их число обозначают греческим числительным (ди-, три-, тетра- и т. д.), которое ставят перед названием этих радикалов, а их положение указывают одной и той же цифрой, повторенной дважды (или несколько раз – в зависимости от количества одинаковых заместителей). Например:
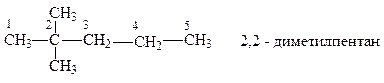
Приведём ещё примеры:

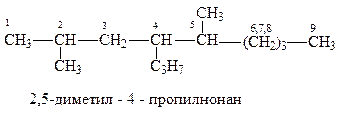
По рациональной номенклатуре предельные углеводороды рассматриваются как производные метана, в молекуле которых один или несколько атомов водорода замещены на радикалы. Названия строят следующим образом. Называют по старшинству все заместители (указывая их количество, если они одинаковые) и основу названия – слово «метан». Приведём примеры углеводородов и назовём их по рациональной и систематической номенклатурам:

Как видно из этих примеров, систематическая номенклатура – более удобная и совершенная.
Физические свойства. Четыре первых представителя ряда метана – газообразные вещества, начиная с пентана (С5) до гексадекана (С16) углеводороды нормального строения – жидкости, С17 и выше – твёрдые вещества. В ряду метана для алканов нормального строения по мере роста молекулярной массы (см. табл. 9) наблюдается увеличение температур кипения и плавления, а также плотности. Разница в температурах кипения соседних гомологов у нормальных алканов С5 – С10 составляет 20 – 30°С и постепенно она уменьшается до 15°С у углеводородов С15 – С20.
Алканы с разветвлённой цепью углеродных атомов кипят при более низких температурах по сравнению с алканами нормального строения; с увеличением числа заместителей, превращением молекул в более разветвлённые разница в температурах кипения алканов нормального и разветвлённого строения возрастает. Эта же закономерность наблюдается и для плотности. Это хорошо видно из табл. 10.
Таблица 10
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 457; Нарушение авторских прав?; Мы поможем в написании вашей работы!