
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ингибиторы ферментов
|
|
|
|
Влияние рН на скорость ферментативной реакции
Для большинства ферментативных реакций оптимальное значение рН среды лежит в интервале 5− 9. Кривая зависимости скорости ферментативной реакции от рН является кривой с максимумом (рисунок)
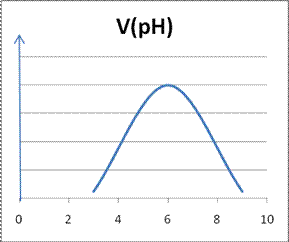
Такой вид кривой обусловлен тем, что существует оптимальное состояние ионизации субстрата и белковой молекулы фермента (её аминокислотных остатков), которое обеспечивает наиболее прочное их соединение в активном центре и, следовательно, наибольшую скорость реакции.
Действие ферментов может быть ослаблено или полностьюподавлено с помощью определенных веществ – ингибиторов. Их действие может быть обратимым и необратимым.
Обратимые ингибиторы обычно связываются с ферментом нековалентными связями и могут быть легко от них отсоединяться, при этом существуют так называемые конкурентные обратимые ингибиторы, которые имеют сходные структуры с субстратом и стремятся, каждый в первую очередь, связаться с ферментом на субстратсвязывающем участкеактивного центра. Если к ферменту Е добавить конкурентный ингибитор I и субстрат S, то образуются два комплекса по реакциям:
Е + S «ES ® Р + Е
Е + I «Е I ≠ Р
Р
Так как образование комплекса ЕI не приводит к образованию продуктов реакции, то скорость реакции их образования уменьшается, так как уменьшается число активных центров фермента, способных взаимодействовать с субстратом. Поскольку конкурентный ингибитор связывается с ферментом обратимо, то уменьшить его действие можно, увеличивая концентрацию субстрата, так как при этом увеличивается вероятность связывания фермента с субстратом. Ингибитор, мешая образованию фермент-субстратного комплекса, он увеличивает константу Михаэлиса Кm, но не изменяет Vmax.
Неконкурентный обратимый ингибитор не сходен поструктуре, с субстратом, поэтому он может связываться с ферментом и в присутствии и в отсутствии субстрата, и обычно связывается с ферментом не в активном центре, а в другом месте, обычно в регуляторном центре. При этом образуется тройной комплекс: фермент-ингибитор-субстрат (ЕSI), который не приводит к образованию продуктов реакции:
Е + S + I ® Е I ≠ Р
При данном типе ингибирования влияние ингибитора не может быть преодолено повышением концентрации субстрата. Неконкурентный обратимый ингибиторуменьшает как Vmax, так и Кm.
Необратимые ингибиторы ферментов – это соединения, которые образуют прочные связи с ферментом, причем именно в активном его центре. Связывая важные группы на субстрат связывающем участке, они необратимо изменяют его конфигурацию. Так необратимо действуют на ферменты ионы тяжелых металлов Hg+2 и Pb+2, чем объясняется их токсическое действие на организм человека.
Регуляция действия ферментов осуществляется гормонами.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 350; Нарушение авторских прав?; Мы поможем в написании вашей работы!