
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Система
|
|
|
|
Химической термодинамики.
Классическая термодинамика (дословно – наука о движении тепла) относится к разделу физических наук, в которых не рассматривается атомная структура материи. Ее основной объект – взаимопревращения различных видов энергии, главным образом теплоты и работы.
Термодинамика – наука, изучающая свойства энергии и законы ее превращения, а также направление и пределы самопроизвольного протекания различных процессов в данных условиях. Термодинамика рассматривает лишь те объекты, которые состоят из большого количества частиц (молекул, атомов, ионов и т.д.), т.е. макроскопические объекты; отдельные частицы не являются предметом ее изучения.
Химическая термодинамика – раздел физической химии, посвященный изучению макроскопических химических систем и процессов на основе общих законов взаимопревращения теплоты, различных видов работы и энергии. Основное содержание настоящего курса составляет исследование закономерностей теплового движения в равновесных системах и при переходе систем в равновесие. При этом возможны два метода исследования – термодинамический и статистический. Первый, термодинамический, не учитывает конкретную природу веществ, квантование энергии, не опирается ни на какие модельные представления об атомно–молекулярной структуре веществ, т.е. является феноменологическим методом, устанавливающим связи между непосредственно наблюдаемыми величинами. Второй, статистический метод, основанный на учете строения вещества и квантовых эффектов, позволяет предсказать макроскопическое поведение на основе анализа процессов, происходящих на микроскопическом уровне. Этот метод составляет предмет статистической термодинамики.
Термодинамический метод характеризуется тем, что для него объектом исследования является тело или группа тел, произвольно выделяемая нами из внешнего мира. Термодинамическая система – совокупность тел, могущих энергетически взаимодействовать между собой и с другими телами иобмениваться с ними веществом. Таким образом, окружающий мир термодинамика делит на две части: систему—любой материальный объект, выделенный для исследования, и окружающую среду. Система отделена от окружающей среды граничной (контрольной) поверхностью, реально существующей или воображаемой. Термодинамическая система всегда является макроскопической и находится в состоянии термодинамического равновесия (в системе не только все параметры постоянны во времени, но и нет стационарных потоков вследствие действия каких-нибудь внешних источников).
Термодинамической системой может быть что угодно: колба с веществом, реактор, кусок металла или сплава, газ в объеме, раствор, твердое тело, система электрических зарядов, расплавы солей и металлов, ректификационная колонна, плазма.
По способу взаимодействия системы с окружающей средой (иначе, по пропускной способности граничной поверхности) или другими системами различают:
а) изолированные системы, которые не обмениваются энергией и веществом;
б) закрытые системы, которые не обмениваются веществом, но обмениваются энергией;
в) открытые системы, в которых имеет место обмен веществом и энергией;
г) адиабатические системы, в которых отсутствует теплообмен с другими системами.
С целью указания способа обмена энергией и веществом применяют понятия теплового (термического), механического и диффузионного контактов:
открытая система имеет диффузионные контакты с внешней средой,
для изолированной системы любые с ней контакты невозможны.
Влияние свойств внешней среды на свойства системы зависят от перечисленных свойств граничной поверхности. Внешняя среда выполняет при этом роль источника или поглотителя энергии и вещества, обладающего неограниченной емкостью. Термодинамические системы могут быть гомогенными, гетерогенными, изотермическими, изобарическими, адиабатическими и т.д., т.е. находиться в различных состояниях.
Следует отметить, что закрытая система может изменять свой состав, если в ней протекает химическая реакция, которую символически можно записать в виде
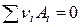 ,
,
где Ai – некоторое химическое соединение, ni – стехиометрический коэффициент; причем для исходных веществ значения ni берутся со знаком «минус», а для продуктов реакции со знаком «плюс», например
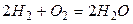
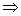
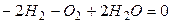 .
.
Это уравнение показывает, что при протекании реакции в системе число молей водорода уменьшилось на 2, кислорода на 1, а число молей воды увеличилось на 2.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 393; Нарушение авторских прав?; Мы поможем в написании вашей работы!