
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диаграммы плавкости бинарных систем с образованием химического соединения, плавящегося конгруэнтно
|
|
|
|
Диаграммы состояния такого типа характерны для систем, в которых исходные компоненты А и В образуют одно прочное химическое соединение А m B n, плавящееся без разложения (конгруэнтно) и не растворимое в компонентах А и В в твердом состоянии.
Во многих случаях кривая ликвидуса двухкомпонентных систем, в отличие от диаграмм 10.4 – 10.6, имеет один (рис. 10.7) или даже несколько максимумов. Поскольку температура затвердевания любого вещества понижается при добавлении к нему других компонентов, то форму таких кривых можно объяснить лишь тем, что в точке максимума образуется химическое соединение. Температура плавления такого соединения понижается при добавлении к нему как компонента А, так и компонента В. Если образовавшееся химическое соединение А m B n устойчиво как твердом, так и в жидком состояниях (например, для систем H2O и FeCl3, уксусная кислота и мочевина), т. е. обладает определенной температурой плавления, то точку максимума называют конгруэнтной. Иными словами, плавление химических соединений, при котором состав твёрдой фазы одинаков с составом расплава, называется конгруэнтным. Примерами систем с одним конгруэнтно плавящимся соединением являются Sn – Mg, Mg – Si и CaCl2 – KCl.
Конгруэнтной точкой на диаграмме 10.7 является фигуративная точка с. В ней система условно инвариантна
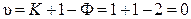 .
.
Фигуративные точки, лежащие на линии cd, соответствуют твердому химическому соединению при различных температурах:
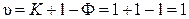 .
.
В различных системах вид максимума на кривой ликвидуса разный и зависит от степени диссоциации соединения при температуре плавления по схеме
А m B n «m A + n B.
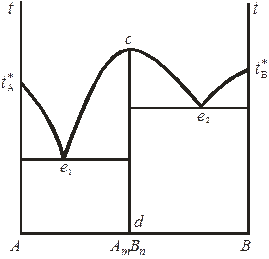
Рис. 10.7. Диаграмма плавкости бинарной системы
с конгруэнтной точкой плавления
Чем больше степень диссоциации химического соединения, тем более пологим будет максимум на кривой ликвидуса (соответственно, чем меньше степень диссоциации, тем острее максимум). Радиус кривизны максимума r и степень диссоциации химического соединения α связаны между собой следующим приближенным соотношением:
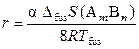 ,
,
где Δfus S (А m B n) и T fus – энтропия и температура плавления соединения.
Результатом частичной диссоциации химического соединения (см. рис. 10.7) является то, что в расплаве левее линии сd присутствуют некоторые количества компонента В, а правее – некоторые количества компонента А.
Если степень диссоциации химического соединения равна нулю, то на кривой ликвидуса наблюдается острый максимум. Фигуративная точка с, отвечающая недиссоциированному химическому соединению, называется сингулярной или дальтоновской точкой, а само соединение – дальтонидом. Характерным признаком образования дальтонидов является то, что их состав не зависит от внешних условий, определяющих равновесие (температура или давление). Примерами систем с образованием дальтонидов являются Mg – Ag, Mg – Au, Au – Zn.
Если на кривой ликвидуса имеется пологий максимум, не соответствующий простому стехиометрическому соотношению исходных компонентов и смещающийся при изменении внешних параметров (например, давления), то твердое соединение в таких системах называется бертоллидом. Бертоллиды – твердые фазы переменного состава, стоящие на границе между химическими соединениями и твердыми растворами. Примерами систем с образованием бертоллидов являются Pb – Na, Al – Fe и Fe – Sb.
Итак, если соединение А m B n имеет определенную точку плавления и ведет себя как индивидуальное химическое соединение, то общая диаграмма состояния (см. рис. 10.7) как бы разделяется на две диаграммы: первая диаграмма – левее линии сd, относящаяся к системе А и А m B n (эвтектическая точка e 1); вторая диаграмма – правее линии сd, относящаяся к системе В и А m B n (эвтектическая точка e 2).
Если исходные компоненты А и В образуют несколько химических соединений, плавящихся конгруэнтно, на диаграмме плавкости каждому из них соответствует свой максимум. Примерами таких систем являются Ag – Ca, Cu – Mg и Al2O3 – CaO.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2815; Нарушение авторских прав?; Мы поможем в написании вашей работы!