
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Краткие сведения об основных параметрах гомеостаза волемия
|
|
|
|
039(01)-84
K-------------------------------- 134-84
4113000000—162
© Издательство «Медицина». Москва. 1984
ПРЕДИСЛОВИЕ
Современной медицине свойственна тенденция к узкой специализации, которая коснулась и хирургии. От нее отделились анестезиология и реаниматология, травматология и ортопедия, возникла органная хирургия — желудочная, легочная, сердечная и др. На фоне этой дифференциации многих клинических дисциплин появилась и успешно развивается новая отрасль медицины — трансфузиология. Ее теоретическими и практическими достижениями в настоящее время широко пользуются врачи почти всех специальностей. В этом отношении трансфузиологии присущи интегральные черты, так как ее клиническая направленность имеет целью влияние на весь организм, а не на отдельные его органы.
Трансфузионная терапия, т.е. воздействие на внутреннюю среду организма посредством внутривенного введения различных препаратов направленного действия, может дать оптимальный лечебный эффект при условии, что врач четко знает цель применения трансфузионного средства и механизм его действия. Арсенал этих средств непрерывно растет и усложняется, что требует постоянного повышения врачебных знаний. Поскольку в больницах еще нет специалистов-трансфузиологов, многие вопросы лечебной тактики врачи решают на основе некоторых общих теоретических сведений и, главное, руководствуясь инструкциями, приложенными к препаратам.
За последние 5—7 лет появилось несколько обстоятельных монографий, посвященных трансфузионной терапии [Головин Г.В. и др., 1975; Вагнер Е.А., Тавровский В.М., 1977; Терехов Н.Т., 1979; Гланц Р.М., Усиков Ф.Ф., 1979; Колесников И.С. и др., 1980, и др.].
В книге, предлагаемой вниманию читателя, сделана попытка обобщить многочисленные, но разрозненные публикации и опыт 1-го хирургического отделения Центрального научно-исследовательского института гематологии и переливания крови Министерства здравоохранения СССР, чтобы снабдить практического врача пособием по использованию современных трансфузиологических средств при комплексном лечении наиболее тяжелых хирургических заболеваний.
Грамотно и ответственно проводить трансфузионную терапию при различных патологических состояниях можно, лишь имея ясное представление о патофизиологических сдвигах в организме. Весьма опасен упрощенный подход к назначению тех или иных препаратов, основанный только на стремлении устранить или возместить возникающий дефицит в гомеостазе (по принципу «сколько больной потерял, столько нужно влить»).
Главной задачей клинициста должно быть четко продуманное лечение посредством трансфузионных средств с целью помочь организму больного максимально использовать собственные защитно-приспособительные реакции, возникающие в ответ на экстремальную ситуацию. Именно поэтому в книге большое внимание уделено описанию патофизиологических синдромов, без понимания которых врач не сможет добиться оптимального эффекта трансфузионной терапии. Изложенные принципы помогут ему при составлении конкретной программы терапии с учетом как теоретических предпосылок, так и клинико-лабораторных данных о больном. Представленные сведения и рекомендации касаются преимущественно состояний и заболеваний, относящихся к разделу неотложной хирургии; но многие из них могут быть использованы и при плановых операциях.
Авторы надеются, что книга, предназначенная прежде всего для хирургов, анестезиологов и реаниматологов, окажется полезной в их практической деятельности.Все критические замечания будут приняты с благодарностью.
Глава I
Объем крови, находящийся в организме, распределяется между двумя секторами — функционирующим и нефункционирующим. Функционирующий сектор — это сердце, крупные и мелкие артерии и вены, а также 10% капилляров. Кровь, заполняющая эту систему, представляет собой объем циркулирующей крови (ОЦК). Нефункционирующий сектор — это 90% остальной капиллярной сети организма, в которой содержится депонированная кровь, используемая в экстремальных состояниях для быстрой компенсации острой кровопотери [Чижевский А.Л., 1959 и др.].
Распределение ОЦК. По данным разных авторов [Albert S.N., 1963, и др.], ОЦК в организме составляет в среднем от 5 до 6 л, или 1/13 или 7% массы тела. Диапазон колебаний средних цифр ОЦК определяется влиянием на него главным образом увеличения массы и поверхности тела. На ОЦК действуют и другие факторы: пол, возраст, профессия, занятия спортом, температура внешней среды, атмосферное давление и т.д.
Распределение крови между паренхиматозными органами и сердечно-сосудистой системой неравномерно. Так, в паренхиматозных органах находится 20% ОЦК, а в сердечно-сосудистой системе — 80%. Более всего крови циркулирует в скелетной мускулатуре (7%) и в печени (5%); на сердце, легкие, мозг, селезенку, почки приходится по 0,5—1%. Неравномерность распределения крови отмечается и в самой системе кровообращения. В большом круге кровообращения содержится 75—80%, а в малом — 20 — 25% ОЦК. В венозной системе находится 65—70%, а в артериальной — 15—20% ОЦК. Меньше всего циркулирующей крови в капиллярной системе — 5—8% (рис. 1).
Регуляция ОЦК. Волемия — величина непостоянная. Она изменяется в зависимости от депонирования или экспонирования крови, транскапиллярного обмена, т.е. увеличения или уменьшения коллоидно-осмотического давления плазмы и других факторов.
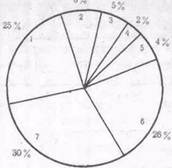
Рис. 1. Распределение ОЦК в сердечно-сосудистой системе [Gelin L.Е., 1969].
1 — сердце и сосуды легких: 2 — большие артерии; 3 — малые артерии; 4 — артериолы; 5 — капилляры; 6 — малые вены, венулы. венозные синусы; 7 — большие вены.
В организме всегда имеется определенное количество крови, которое в общей циркуляции не участвует. Это та часть общего количества крови, которая находится в состоянии застоя в депо, т.е. в не функционирующих капиллярах, преимущественно в скелетной мускулатуре. Емкость нефункционирующих капилляров огромна. Их общее поперечное сечение превышает поперечник аорты в 600—800 раз общая длина равна 100 000 км. В депо организма находится количество крови, равное ОЦК, т. е. 4—5 л под давлением 0,49—0,78 кПа(5—8 мм рт. ст.) [Быков К. М., 1975, Чижевский А. Л., 1959]. Резервы крови в организме весьма значительны, и это вполне укладывается в представления о «запасе прочности» организма, создаваемой природой в процессе филогенеза в ответ на стрессовые ситуации — страх, острую кровопотерю, готовность к защите и т. д.
Регуляция ОЦК путем экспонирования или депонирования может осуществляться довольно быстро с помощью механизма вазомоции, т. е. вазомоторной активности сосудов, регулирующих попеременное продвижение тока крови в капиллярных полях автономно под влиянием местного метаболизма.
При необходимости уменьшить ОЦК (в частности, при переходе от усиленной физической нагрузки к полному покою) из кровообращения могут быть выключены капиллярные поля с содержащейся в них кровью. Наоборот, при необходимости увеличить ОЦК (в случае внезапно возникшей физической нагрузки) в общий кровоток включаются капиллярные поля, содержащие застойную кровь. Эти реакции происходят в организме постоянно.
Патологическое депонирование возникает как реакция на стрессовое состояние — острую кровопотерю, травму, интоксикацию и т.д. Оно отличается нарушениями реологических свойств крови за счет ее сгущения и нарушения микроциркуляции (застойное кровообращение в капиллярном русле). Патологическое депонирование бывает необратимым при резких нарушениях реологических свойств крови вплоть до агрегации эритроцитов.
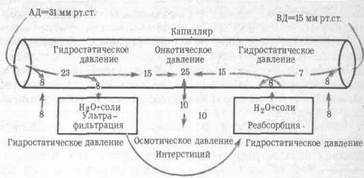
Рис. 2. Схематическая раскладка гидростатического и онкотического давления в механизме транскапиллярного обмена (по Стерлингу).
Знание механизмов депонирования и экспонирования крови, особенно возникающих в стрессовых ситуациях, помогает лучше понимать характер защитно-приспособительных реакций сердечно-сосудистой системы при гипо- и гиперволемических состояниях.
Транскапиллярный обмен. Регуляция ОЦК происходит и на транскапиллярном уровне, где осуществляется обмен между плазмой и интерстициальной жидкостью. В этом обмене важную роль играют белки крови, соли и вода, определяющие коллоидно-осмотическое давление по обе стороны диализирующей мембраны капиллярной стенки (рис. 2).
В зависимости от концентрации белков в плазме может меняться коллоидно-осмотическое давление крови. От этого зависит поступление жидкости из интерстиция в кровеносное русло и в обратном направлении. Ток жидкости через диализирующую мембрану стенки капилляра направлен, как правило, в сторону большей концентрации коллоидов, поэтому снижение концентрации белков в плазме крови и альбуминоглобулинового коэффициента (А/Г) способствует уменьшению ОЦК за счет снижения ОЦП. При повышении концентрации белков в плазме (особенно альбуминов) ОЦП и, следовательно, ОЦК, закономерно увеличиваются.
Критическим для сдвига онкотического давления плазмы является содержание белков ниже 50 г/л, когда начинается усиленный переход жидкости из сосудистого ложа в интерстиций, что снижает ОЦП.
Водно-электролитный обмен на уровне капилляров тесно связан с обменом белков. Анализирующая капиллярная мембрана, относительно непроницаемая для белков, легко пропускает через свои «поры» (2—3 нм) воду, кристаллоиды, мочевину, глюкозу, мочевую кислоту и другие органические молекулы.
Белки, остающиеся во внутрисосудистой жидкости, удерживают возле себя ионы кристаллоидов с противоположным знаком электрического заряда, а в интерстициальное пространство проникают ионы кристаллоидов с таким же знаком зарядности, как ионы белка. Распределение электролитов между секторами создает электролитно-ионное равновесие по обе стороны мембраны. Однако наличие во внутрисосудистой жидкости ионов еще и белковой природы повышает ее онкотическое (коллоидно-осмотическое) давление. Этим и определяется приток жидкости из интерстиция в сосудистое пространство через стенку венозного отдела капилляров.
При гипопротеинемии и снижении онкотического давления плазмы, а также под влиянием относительно возрастающего кровяного (гидростатического) давления внутрисосудистая жидкость начинает проникать в интерсти-ций и ОЦП соответственно снижается. Постоянная конкурентность между гидростатическим и онкотическим давлением характеризует механизм транскапиллярного обмена.
Печень и почки активно участвуют в регуляции волемии в организме. Печень синтезирует белки и этим способствует восстановлению онкотического давления плазмы после кровопотери. Кроме того, печень участвует в регуляции диуреза путем инактивации альдостерона и антидиуретического гормона (АДГ) при снижении ОЦК. Роль почек в регуляции гомеостаза весьма разнообразна. В поддержании волемии почки участвуют главным образом путем сохранения в организме натрия и связанной с ним волы.
Реабсорбция натрия и воды осуществляется в результате секреции альдостерона и антидиуретического гормона (АДГ), сигналами для выделения которых служат рефлексы барорецепторов, заложенных в почечных артериолах, и волюмрецепторов в предсердиях и каротидных синусах [ЗильберА. П., 1977].
При снижении артериального давления (гиповолемия) в примыкающем к артериоле юкстагломерулярном аппарате секретируется и выбрасывается в кровь ренин. Ренин активирует а 2-глобулин плазмы и превращает его в ангиотензин, который, воздействуя на кору надпочечников, способствует выбросу в кровь альдостерона. Альдостерон, как известно, усиливает процесс реабсорбции в канальцах натрия и воды. Кроме того, сигналы с баро- и волюмрецепторов начинают поступать и в гипоталамус, а оттуда в гипофиз. В результате этого в кровь выделяются адрено-кортикотропный (АКТГ) и антидиуретический (АДГ) гормоны. АКТГ усиливает активность альдостерона, а АДГ — гиалуронидазы.
Методы определения ОЦК. В настоящее время методы определения ОЦК в клинике используются довольно широко. От величины ОЦК зависит направление инфузионно-трансфузионной терапии при травматическом шоке, острой кровопотере, интоксикации и т.д. Все методы являются непрямыми, т.е. осуществляются с помощью различных индикаторов, вводимых в кровь больного внутривенно. Принцип определения ОЦК с помощью этих индикаторов единый. Он заключается в разведении в крови больного индикатора, объем которого точно известен. Обычно используют вещества, с помощью которых определяют объем циркулирующей плазмы (ОЦП) или объем циркулирующих эритроцитов (ОЦЭ), а затем через показатель гематокрита высчитывают ОЦК.
Для определения ОЦП в качестве индикатора может быть использована синяя азокраска Т-1824 (синий Эванса), длительно циркулирующая в крови вместе с альбумином, с которым она вступает в тесный контакт. Концентрация краски в крови больного определяется с помощью спектро-фотометрии. Другим индикатором, легко вступающим в соединение с альбумином плазмы и служащим показателем величины ОЦП, является радиоактивный изотоп йода 131I. Для определения ОЦЭ используют изотоп хрома 51Cr или 52Cr.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1906; Нарушение авторских прав?; Мы поможем в написании вашей работы!