
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия. Первый закон термодинамики
|
|
|
|
Основы термодинамики
Термодинамика изучает процессы и явления, происходящие в природе и технике, с точки зрения преобразования энергии, в том числе внутренней энергии тел.
Термодинамическая система – это совокупность тел, способных обмениваться энергией между собой и с другими системами. Замкнутая термодинамическая система не обменивается энергией с другими системами.
Каждое тело имеет вполне определенную структуру, оно состоит из частиц, которые хаотически движутся и взаимодействуют друг с другом, поэтому любое тело обладает внутренней энергией.
Внутренняя энергия — это величина, характеризующая собственное состояние тела, т. е. энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д.) и энергия взаимодействия этих частиц.
Внутренняя энергия идеального газа складывается только из энергии движения молекул, так как взаимодействием молекул можно пренебречь. Внутренняя энергия одноатомного идеального газа определяется по формуле U = 3/2 • m/М • RT. Внутренняя энергия одного моля одноатомного идеального газа:
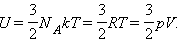
|
Внутреннюю энергию можно изменить двумя способами: путем теплопередачи и путем совершения механической работы
Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты (Q). Принято считать, что Q > 0, если тело получает энергию, и Q < 0, если тело отдает свою энергию
При совершении механической работы должно происходить направленное перемещение тел под действием сил, например, перемещение поршня в цилиндре с газом. Если газ расширяется, то сила давления газа на поршень совершает положительную работу (A > 0) за счет внутренней энергии газа. Если внешние силы больше силы давления газа, то газ сжимается и работа газа будет отрицательной (A < 0), при этом внутренняя энергия увеличивается.
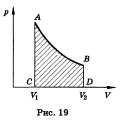
При изобарном нагревании газ совершает работу над внешними силами  , где V1 и V2 — начальный и конечный объемы газа. Если процесс не является изобарным, величина работы может быть определена площадью фигуры ABCD, заключенной между линией, выражающей зависимость p(V), и начальным и конечным объемами газа V
, где V1 и V2 — начальный и конечный объемы газа. Если процесс не является изобарным, величина работы может быть определена площадью фигуры ABCD, заключенной между линией, выражающей зависимость p(V), и начальным и конечным объемами газа V
Первый закон термодинамики:
изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы внешних сил, совершенной над системой. 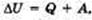 ,
,
где 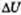 — изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил. А*-работа самой системы, т.е.работа газа. Если система сама совершает работу и получает или отдает теплоту, то изменение ее внутренней энергии ∆U = Q – A.
— изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил. А*-работа самой системы, т.е.работа газа. Если система сама совершает работу и получает или отдает теплоту, то изменение ее внутренней энергии ∆U = Q – A.
Применение первого закона термодинамики к изопроцессам
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид: 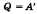 , т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: 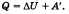 .
.
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0, и уравнение первого закона имеет вид 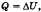 , т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.
, т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.
Адиабатным называют процесс, протекающий без теплообмена с окружающей средой. Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, 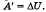
Второе начало термодинамики гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 12213; Нарушение авторских прав?; Мы поможем в написании вашей работы!