
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Особенности реакций в растворах электролитов
|
|
|
|
В растворах электролитов присутствуют ионы, подвижность которых, как правило, выше, чем недиссоциированных молекул. Кроме того, большинство ионов обладают высокой реакционной способностью. Поэтому химические реакции в растворах электролитов протекают, как правило, с высокими скоростями, и химическое равновесие большинства процессов устанавливается быстро.
Химические свойства раствора электролита складываются из свойств образующих его ионов. Группа электролитов, содержащая один и тот же вид ионов, обладает сходными химическими свойствами. Так, все растворы, содержащие хлорид-ионы , при добавлении к ним раствора нитрата серебра
, при добавлении к ним раствора нитрата серебра 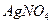 дают белый осадок хлорида серебра AgCl. Подобные качественные реакции на данный вид ионов широко используются в аналитической химии при определении состава растворов.
дают белый осадок хлорида серебра AgCl. Подобные качественные реакции на данный вид ионов широко используются в аналитической химии при определении состава растворов.
Основным фактором, влияющим на смещение равновесия в растворах электролитов, является изменение концентрации ионов. Поэтому обменные реакции в растворах идут в сторону малорастворимых веществ или слабых электролитов. Это правило легко объяснимо, так как в результате протекания таких процессов один или несколько видов ионов выводятся из сферы взаимодействия, что в соответствии с принципом Ле Шателье должно привести к более полному протеканию реакции. Малорастворимые вещества могут выводится из раствора или в виде осадка, или в виде газа. Слабыми электролитами могут быть кислоты и основания, вода и комплексы.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1079; Нарушение авторских прав?; Мы поможем в написании вашей работы!