
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Скорость химической реакции
|
|
|
|
Химическая кинетика
Модуль 3. Химическая кинетика. Окислительно-восстановительные процессы
Кинетикой химических реакций называется учение о скорости их протекания, механизме химического взаимодействия и зависимости их от различных факторов. Эти вопросы представляют большой практический и теоретический интерес. Разные реакции совершаются с самыми различными скоростями.
Предсказания химической термодинамики наиболее верны в своей «запрещающей» части. Если, например, для реакции N2+O2 = 2NO DG0 = +176кДж, то эта реакция не пойдет самопроизвольно, и никакой катализатор ей не поможет. Известный заводской процесс получения NO из воздуха требует огромных затрат энергии и неравновесного процесса («закалка» продуктов быстрым охлаждением после пропускания смеси газов через электрическую дугу).
С другой стороны, далеко не все реакции, для которых DG < 0, «спешат» осуществиться на практике. Куски каменного угля могут веками лежать на воздухе, хотя для реакции:
C+O2 = CO2 DG0 = - 395 кДж.
Химические реакции протекают с различными скоростями. Некоторые из них полностью заканчиваются за малые доли секунды, другие осуществляются за минуты, часы, дни, известны реакции, требующие для своего протекания несколько лет, десятилетий и еще более длительных отрезков времени. Кроме того, одна и та же реакция может в одних условиях, например, при повышенных температурах, протекать быстро, а в других — например, "при охлаждении — медленно; при этом различие в скорости одной и той же реакции может быть очень большим.
Знание скоростей химических реакций имеет очень большое научное и практическое значение. Например, в химической промышленности при производстве того или иного вещества от скорости реакции зависят размеры и производительность аппаратуры, количество вырабатываемого продукта.
Предсказание скорости химической реакции, а также выяснение зависимости этой скорости от условий проведения реакции осуществляет химическая кинетика – наука о химическом процессе, его механизме и закономерностях протекания во времени.
При рассмотрении вопроса о скорости реакции необходимо различать реакции, протекающие в гомогенной системе (гомогенные реакции), и реакции, протекающие в гетерогенной системе (гетерогенные реакции).
Системой в химии принято называть рассматриваемое вещество или совокупность веществ. При этом системе противопоставляется внешняя среда — вещества, окружающие систему. Обычно система физически отграничена от среды.
Различают гомогенные и гетерогенные системы. Гомогенной называется система, состоящая из одной фазы, гетерогенной — система, состоящая из нескольких фаз. Фазой называется часть системы, отделенная от других ее частей поверхностью раздела, при переходе через которую свойства изменяются скачком.
Если реакция протекает в гомогенной системе, то она идет во всем объеме этой системы. Например, при сливании (и перемешивании) растворов серной кислоты и тиосульфата натрия помутнение, вызываемое появлением серы, наблюдается во всем объеме раствора:
H2SO4 + Na2S2O3 = Na2SO4 + H2O + SO2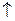 + S
+ S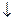 .
.
Если реакция протекает между веществами, образующими гетерогенную систему, то она может идти только на поверхности раздела фаз, образующих систему. Например, растворение металла в кислоте
Fe + 2HCl = FeCl2 + H2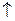
может протекать только на поверхности металла, потому что только здесь соприкасаются друг с другом оба реагирующие вещества. В связи с этим скорость гомогенной реакции и скорость гетерогенной реакции определяются различно.
Скоростью гомогенной реакции называется количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени в единице объема системы.
Скоростью гетерогенной реакции называется количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице площади поверхности фазы:
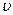 гомог =
гомог = 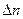 /(V
/(V 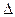 τ);
τ); 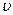 гетерог =
гетерог = 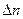 /(S
/(S 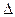 τ). (13.1)
τ). (13.1)
Скорость химической реакции можно определить как изменение концентрации одного из участвующих в реакции веществ (исходное вещество или продукт реакции) в единицу времени.
А®В
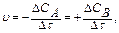
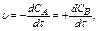 (13.2)
(13.2)
где СА, СВ – изменение концентрации исходного вещества и продукта реакции.
В любой реакции реагенты расходуются, она замедляется (см. рисунок 1).
Поэтому можно говорить только о скорости в данный момент времени. Очевидно, что скорость зависит от концентрации реагирующих веществ.
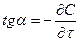

Рисунок 13.1 - Изменение концентрации исходного вещества
в ходе реакции
Если хотя бы одно из реагирующих веществ – газ, то удобно следить за скоростью по изменению объема или давлению в закрытом сосуде при постоянной температуре. Иногда можно наблюдать за изменением окраски, за появлением осадка, за изменением электропроводности и спектральных данных.
От чего зависит скорость химической реакции?
К важнейшим факторам, влияющим на скорость реакции, относятся следующие: природа реагирующих веществ, их концентрации, температура, присутствие в системе катализаторов. Скорость некоторых гетерогенных реакций зависит также от интенсивности движения жидкости или газа около поверхности, на которой происходит реакция.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 434; Нарушение авторских прав?; Мы поможем в написании вашей работы!