
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вандерваальсовы силы
|
|
|
|
Взаимодействие между молекулами. Комплексные соединения
Вопросы
- В чем состоит особенность статического режима астатической САУ?
- Можно ли добиться астатизма без включения интегрирующего звена?
- Как отражается на динамических свойства САУ величина частоты среза?
- Как отражается на динамических свойства САУ наклон высокочастотного участка ЛАЧХ?
- Как отражается на динамических свойства САУ наклон низкочастотного участка ЛАЧХ?
- Что называется демпфированием с поднятием высоких частот?
- Что называется демпфированием с подавлением высоких частот?
- Что называется демпфированием с подавлением средних частот?
- Как изменятся динамические и статические характеристики САР при включении в регулятор интегрирующего звена?
- Как изменятся динамические и статические характеристики САР при включении в регулятор астатического звена?
- Как изменятся динамические и статические характеристики САР при включении в регулятор форсирующего звена?
- Как осуществляется последовательная коррекция по задающему воздействию?
- Как осуществляется коррекция с использованием неединичной обратной связи?
- В чем общий недостаток астатических САУ без интегрирующего звена?
- Как подобрать передаточную функцию корректирующего устройства при компенсации возмущающего воздействия?
В предыдущей главе было рассмотрено взаимодействие атомов с образованием молекул, а также представлены структуры и некоторые свойства молекул. Настоящая глава посвящена взаимодействию молекул.
При сближении молекул появляется притяжение, что обусловливает возникновение конденсированного состояния вещества. К основным видам взаимодействия молекул следует отнести вандерваальсовы силы, водородные связи и донорно-акцепторное взаимодействие.
В 1873 г. голландский ученый И. Ван-дер-Ваальс предположил, что существуют силы, обусловливающие притяжение между молекулами. Эти силы позднее получили название вандерваальсовых сил. Они включают в себя три составляющие: диполь-дипольное, индукционное и дисперсионное взаимодействия.
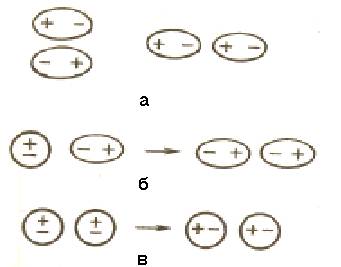
а – диполь-дипольное взаимодействие; б - индукционное взаимодействие;
в – дисперсионное взаимодействие
Рисунок 6.1 – Вандерваальсовы взаимодействия молекул
6.1.1 Диполь-дипольное взаимодействие. При сближении полярных молекул они ориентируются таким образом, чтобы положительная сторона одного диполя была ориентирована к отрицательной стороне другого диполя (рисунок 6.1, а).
Возникающее между диполями взаимодействие называется диполь-дипольным или ориентационным. Энергия диполь-дипольного взаимодействия пропорциональна электрическому моменту диполя в четвертой степени и обратно пропорциональна расстоянию между центрами диполей в шестой степени и абсолютной температуре в первой степени.
6.1.2 Индукционное взаимодействие. Диполи могут воздействовать на неполярные молекулы, превращая их в индуцированные (наведенные) диполи (рисунок 6.1, б). Между постоянными и наведенными диполями возникает притяжение, энергия которого пропорциональна электрическому моменту диполя во второй степени и обратно пропорциональна расстоянию между центрами молекул в шестой степени. Энергия индукционного взаимодействия возрастает с увеличением поляризуемости молекул, т.е. способности молекулы к образованию диполя под воздействием электрического поля. Величину поляризуемости выражают в единицах объема. Поляризуемость в однотипных молекулах растет с увеличением размера молекул (таблища 6.1). Энергия индукционного взаимодействия значительно меньше энергии диполь-дипольного взаимодействия.
6.1.3 Дисперсионное притяжение. В любой молекуле возникают флуктуации электрической плотности, в результате чего появляются мгновенные диполи, которые в свою очередь индуцируют мгновенные диполи у соседних молекул (рисунок 6.1, в). Движение мгновенных диполей становится согласованным, их появление и распад происходит синхронно. В результате взаимодействия мгновенных диполей энергия системы понижается. Энергия дисперсионного взаимодействия пропорциональна поляризуемости молекул и обратно пропорциональна расстоянию между центрами частиц. Для неполярных молекул дисперсное взаимодействие является единственной составляющей вандерваальсовых сил (таблица 6.1).
Таблица 6.1 - Вклад отдельных составляющих в энергию молекулярного взаимодействия
| Вещество | Электри- ческий момент диполя, D | Поляризу- Емость, м3*1030 | Энергия взаимодействия, кДж/моль | Темпера- тура кипения, К | |||
| Ориентации- онная | Индукции- онная | Десперси- онная | суммарная | ||||
| H2 Ar Xe HCl HBr Hl NH3 | 1,03 0,78 0,38 1,52 | 0,8 1,64 4,16 2,64 3,62 5,42 2,23 | 3,3 1,1 0,6 13,3 | 1,0 0,70 0,3 1,5 | 0,17 8,5 18,4 16,8 28,5 60,6 14,7 | 0,17 8,5 18,4 21,1 30,3 61,5 29,5 | 20,2 239,6 |
6.1.4 Энергия вандерваальсова взаимодействия. Энергия всех видов вандерваальсова взаимодействия обратно пропорциональна расстоянию между центрами молекул в шестой степени.
При сильном сближении молекул проявляются силы отталкивания между ними, которые обратно пропорциональны расстоянию между молекулами в двенадцатой степени. Поэтому зависимость результирующей энергии вандерваальсова взаимодействия EB от расстояния между молекулами, IB, выражается уравнением
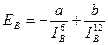 , (6.1)
, (6.1)
где а и b — постоянные.
Минимальная энергия системы обеспечивается при расстояниях между центрами молекул 0,4÷0,5 нм, т.е. существенно больше длины химической связи.
Как видно из таблицы 6.1, с увеличением размера молекул в ряду Аг—Хе и НС1—HI растет их поляризуемость и энергия дисперсионного притяжения. Ориентационное взаимодействие вносит значительный вклад в вандерваальсовы силы лишь в случае молекул с большим электрическим моментом диполя. С увеличением суммарной энергии межмолекулярного взаимодействия возрастет температура кипения жидкостей, а также теплота их испарения. Суммарная энергия вандерваальсового взаимодействия молекул на 1—2 порядка ниже энергии химических связей.
Итак, между молекулами возникают относительно слабые вандерваальсовы взаимодействия, включающие дисперсионные силы, а для полярных молекул и диполь-дипольное притяжение и индукционные взаимодействия.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 573; Нарушение авторских прав?; Мы поможем в написании вашей работы!