
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Радиометрическое титрование
|
|
|
|
Расчеты, используемые в случае стехиометрических реакций.
Пусть, например, осуществляется стехиометрическая реакция типа
А + В = АВ¯
Требуется определить кол-во иона А в растворе: для анализа используется избыток иона В, меченного радиоизотопом. Для обозначения массы ионов будем использовать символ m, для обозначения 1 г-экв соответствующих ионов - символы МА и МВ. Если масса добавленного в раствор иона В равна mВ(0) г, в осадок перешло mВ(АВ) г этого иона, то в растворе останется mВ(р) г; другими словами, уравнение баланса имеет вид:
mВ(0) = mВ(АВ) + mВ(р) (1)
Для баланса активности можно составить аналогичное уравнение
I0 = IАВ + Iр (2)
где I0 - общая добавленная активность; IАВ - активность осадка; Iр -активность раствора после осаждения.
Для осадка АВ справедливо
mА(АВ) mВ(АВ)
-------- - -------- (3)
МА МВ
где mА(АВ) - масса иона А в осадке, равная искомому количеству mх иона А в растворе. Из (3) следует
МА
mх = mА(АВ) = mВ(АВ)----- (4)
МВ
Согласно (1),
mВ(АВ) = mВ(0) - mВ(р) (5)
Если Iуд - весовая удельная активность иона В, то
mВ(р) = Iр / Iуд (6)
Подставляя (5) и (6) в (4), получаем
Iр МА
mх =(mВ(0) - -----) ------ (7)
Iуд МВ
Учитывая, что
Iуд = I0/ mВ(0) (8)
формулу (7) можно преобразовать к виду
МА Iр
mх = mВ(0) -----(1 - ------) (9)
МВ I0
Пример. К раствору, содержащему неизвестное кол-во алюминия, добавили раствор 0,380 мг фосфат-ионов, меченных изотопом 32Р. Общая внесенная в раствор активность составила 11 200 имп/мин. Активность раствора после отделения осадка оказалась равной 4230 имп/мин. Необходимо найти содержание алюминия в анализируемом растворе., учитывая, что реакция между РО43- - ионом и ионом Al3+ протекает по уравнению
Al3+ + РО43- = Al РО4¯
Принимая во внимание, что в данном случае г-экв (M) алюминия равен 27,0 и г-экв иона РО43- равен 95,0 по формуле (9) находим
27,0 4230
mх = 0,380 ------- (1 - -----------) = 0,067 мг
95,0 11 200
При радиометрическом титровании точку эквивалентности определяют с помощью радиоактивных индикаторов. Это дает возможность проводить объемный анализ в тех случаях, когда, например, визуально установить точку эквивалентности по изменению окраски раствора трудно или отсутствует цветной индикатор. Радиометрическое титрование можно применять, если по меньшей мере в одно из реагирующих соединений можно ввести радиоактивную метку, а продукт реакции легко отделяется (выпадает в осадок или экстрагируется).
Рассмотрим, как осуществляют радиометрическое титрование, если продукт реакции выпадает в осадок. Пусть в растворе находится определяемый катион М, а в ходе титрования к нему приливают титрованный раствор осадителя, содержащий анион А, причем либо М, либо А, либо оба иона имеют радиоактивную метку. Осадок МА периодически отделяют и определяют активность раствора I. По полученным данным строят кривые радиометрического титрования в координатах: объем прилитого титрованного раствора - активность раствора.
Наиболее простой вид кривые радиометрического титрования имеют, если, во-первых, растворимость образующегося при реакции соединения незначительна, так что неполнота осаждения не сказывается на результатах измерения активности раствора I, и, во-вторых, объем прибавляемого к анализируемой пробе реагента столь мал, что общий объем раствора в ходе титрования можно считать постоянным. При этих условиях кривая радиометрического титрования состоит из двух прямолинейных участков. В тех случаях, когда изменением объема пренебречь нельзя, в результаты измерения I следует вводить поправку на разбавление. Если объемы проб, активность которых регистрируют, в ходе всего титрования остаются постоянными, то поправку вводят умножая найденные в каждом опыте значения I на величину D, равную
V + Vдоб
D = ------------,
V
где V - исходный объем раствора; Vдоб - объем добавленного раствора осадителя.
Вид кривых радиометрического титрования зависит от того, в какой из растворов (титруемый или титрующий) первоначально введен радиоактивный индикатор, а также от порядка прибавления реагентов. Возможные варианты определения содержания катиона М в исследуемом растворе для наглядности представлены в табл.
| Вариант анализа | Титруемый раствор | Титрующий раствор | Кривая титрования | |||||||||

 

1 | а)активный раствор определяемого элемента (М*) б)активный раствор (А*) известной концентрации | Неактивный раствор (А) известной кон- центрации Неактивный раствор определяемого элемента (М) | ||||||||||
 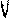 
2 | а)неактивный раст-вор определяемого элемента (М) б)неактивный раст-вор (А) известной концентрации | Активный раствор (А*) известной концентрации Активный раствор определяемого элемента (М*) | ||||||||||
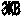 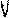   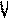
 3 3 | Активный раствор определяемого элемента (М*) | Активный раствор (А*) известной концентрации |
На изображенных в таблице кривых титрования по оси У отложена относительная активность. По оси Х - объем добавленного осадителя.
Точка излома отвечает эквивалентному объему Vэ. Эту точку во всех случаях определяют, экстраполируя прямолинейные участки кривых радиометрического титрования до взаимного пересечения.
Отделять осадок от раствора можно центрифугированием. В этом случае рекомендуется вносить порции растворов определяемого элемента и осадителя в центрифужные пробирки и приливать такое кол-во воды, чтобы объемы растворов во всех пробирках стали одинаковы. После тщательного перемешивания осадки центрифугируют и отбирают равные пробы растворов над осадком для измерения активности. Метод прост в аппаратурном исполнении, но трудоемок.
Для ускорения работы, в целях получения ориентировочных сведений о содержании анализируемого элемента в пробе, расчет можно проводить только по двум точкам. Пусть, например, используют первый вариант радиометрического титрования (см.табл). В этом случае сначала измеряют исходную активность титруемого раствора за вычетом фона I0 затем прибавляют V1 мл раствора осадителя и снова измеряют активность титруемого раствора без фона, внося в результат поправку на изменение объема I1. Как следует из подобия треугольников (рис а),
I0 Vэ I0
---- = --------- (1) откуда Vэ = V1 -------- (2)
I1 Vэ - Vэ I0 - I1
Если титрование выполняют в соответствии со вторым вариантом (см.табл), то прибавляют такие объемы V1 и V2 титрующего раствора, в которых содержится избыток осадителя, определяя соответствующие активности титруемого раствора (за вычетом фона и с учетом поправок на изменение объемов). Тогда, как следует из подобия треугольников (рис б)
I1 V1 - Vэ V1 I2 - V2 I1
---- = --------- (3) откуда Vэ = --------------- (4)
I2 V2 - Vэ I2 - I1
В случаях титрования по третьему способу можно использовать как формулу (2) так и формулу (4), в зависимости от того, на каком участке кривой титрования находятся полученные точки.



 I I
I I

 |
I2 C

 |
I2 D C

 |

 |
I1 E B I1 B
A E D
 | |||
 | |||
 Ip Ip Vэ V1 V2 V,мл
Ip Ip Vэ V1 V2 V,мл
V2 V1 Vэ V,мл
а)Радиоактивен титруемый б) радиоактивен титрующий
раствор раствор.
В тех случаях, когда образующееся при титровании соединение не выпадает в осадок, но может быть отделено экстракцией органическим растворителем графики изменения активности водной фазы (1) сохраняют обычный вид, а кривые активности органической фазы (2) имеют вид, представленный на рисунках штриховыми линиями.
Чувствительность методов анализа, основанных на стехиометрических реакциях, определяется полнотой извлечения определяемого элемента в соответствующем процессе.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 962; Нарушение авторских прав?; Мы поможем в написании вашей работы!




