
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы получения алканов
|
|
|
|
ПРИРОДНЫЕ ИСТОЧНИКИ АЛКАНОВ
Основными природными источниками алканов являются нефть и природный газ.
Состав природного газа зависит от месторождения: обычно в нем содержится от 75% до 95% метана, а этана и пропана значительно меньше. Нефть содержит алканы от С5Н12 до С30Н62 нормального и разветвленного строения. Кроме того, иногда рядом с угольными пластами встречаются и отдельные залежи твердых высших алканов в виде озокерита, или горного воска.
ПРОМЫШЛЕННЫЕ СПОСОБЫ
Основной промышленный способ получения алканов – переработка нефти. Альтернативой может служить прямой синтез из угля и водорода:
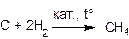
ЛАБОРАТОРНЫЕ СПОСОБЫ
Гидролиз карбида алюминия позволяет получить метан:

Другие алканы этим способом получить нельзя.
Сплавление натриевых солей карбоновых кислот со щелочами. Эта реакция протекает при нагревании смеси порошков соли карбоновой кислоты и гидроксида натрия и сопровождается декарбоксилированием, то есть отщеплением группы
-СООNa от молекулы соли. В молекуле образующегося алкана остается на один атом углерода меньше, чем в молекуле исходной соли, например:
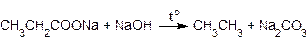
Электролиз водных растворов натриевых или калиевых солей карбоновых кислот (синтез Кольбе) также сопровождается декарбоксилированием. Продуктами реакции являются симметричные углеводороды, например:
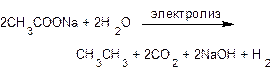
В ходе электролиза на аноде анионы СН3СОО- окисляются до радикалов СН3СОО ∙, которые распадаются с образованием радикалов СН3 ∙ и углекислого газа СО2. Радикалы СН3 ∙ соединяются попарно, и образуется молекула этана.
Реакция галогеналканов с натрием (реакция Вюрца) позволяет получать углеводороды с удвоенным числом атомов углерода по сравнению с исходным соединением, например:
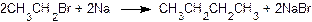
Если в реакцию ввести смесь двух галогеналканов, то образуются одновременно три продукта, например:
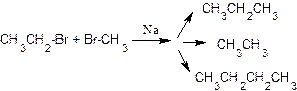
ДОПОЛНЕНИЯ К ЛЕКЦИИ «АЛКАНЫ»
Приложение 1. Первичные, вторичные, третичные и четвертичные атомы углерода. Нормальная и разветвленная углеродная цепь.
В молекулах гомологов метана принято различать первичные, вторичные, третичные и четвертичные атомы углерода в зависимости от числа связей, направленных данным атомом на связь с другими атомами углерода. Первичным называется атом углерода, связанный непосредственно с одним атомом углерода (три оставшиеся валентности направлены на связь с атомами водорода); вторичным – с двумя атомами углерода. Третичный атом углерода связан непосредственно с тремя, а четвертичный – с четырьмя атомами углерода (рис. 1).
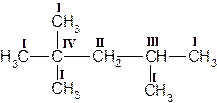
Рисунок 1. Структурная формула молекулы 2,2,4-триметилпентана. Первичные, вторичные, третичные и четвертичные атомы углерода обозначены соответственно цифрами I, II, III, IV.
Углеродную цепь относят к нормальной (неразветвленной), если она содержит только первичные и вторичные атомы углерода, например:
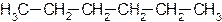
Соответствующий углеводород называют алканом нормального строения или просто нормальным алканом.
Если же в углеродной цепи содержатся третичные или четвертичные атомы углерода, то ее называют разветвленной. Алкан с такой цепью называют разветвленным, например:
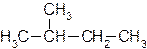
или
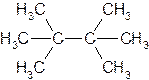 .
.
Приложение 2. Механизм реакции радикального хлорирования метана.
1. Под действием света или нагревания в молекуле хлора разрывается ковалентная связь с образованием двух свободных радикалов:
Cl2 → 2Cl ·
Свободные радикалы ‑ это частицы, содержащие неспаренный электрон. Они очень химически активны и быстро вступают в следующие стадии реакции.
2. Столкновение радикала Cl · с молекулой метана приводит к образованию молекулы HCl и радикала СН3 ∙, который, взаимодействуя со следующей молекулой хлора, дает хлорметан CH3Cl и радикал Cl·:
Cl · + CH4 → HCl + CH3 ·
CH3 · + Cl2 → CH3Cl + Cl ·
Эти процессы могут повторяться многократно, приводя к продолжению реакции (развитию цепи).
3. Возможны и «нежелательные» столкновения, приводящие к гибели свободных радикалов:
Cl · + Cl · → Cl2
CH3 · + Cl · → CH3Cl
CH3 · + CH3 · → СН3СН3
В результате последней реакции соединяются два радикала CH3 ·, поэтому в продуктах реакции хлорирования метана можно обнаружить некоторое количество этана.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 4349; Нарушение авторских прав?; Мы поможем в написании вашей работы!