
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Визначення загальної твердості води
|
|
|
|
Аналіз магнію і лужноземельних металів у розчині
Методом комплексонометрії визначають вміст катіонів багатьох металів: Zn2+, Са2+, Mg2+, Cu2+, А13+, Fe2+, Fe3+, Co2+ та iн.
Визначення вмісту йонів Кальцію у технічному препараті.
Готують розчин солі Кальцію, розчинивши точну наважку q, (г) в мірній колбі місткістю 100 см3. Відбирають піпеткою певний об'єм досліджуваного розчину (Vx, см3) у конічну колбу, добавляють 5–10 см3 амонійного буферного розчину, 2–3 краплі еріохрому чорного і повільно титрують робочим розчином трилону Б до зміни забарвлення від винно-червоного до зеленувато-синього.
Титрування повторюють тричі і для обчислення беруть середнє значення об'єму витраченого розчину трилону Б (VT, см3).
Обчислюють масову частку йонів Кальцію в технічному препараті:
де Сн (Т) – молярна концентрація еквіваленту розчину трилону Б; V(T) – об’єм витраченого розчину трилону Б, см3; me – маса еквівалентна йонів Кальцію; q – маса наважки, яку взяли для досліду.
Визначення твердості води має велике практичне значення в техніці та побуті. Оцінюючи питну воду, доводиться визначати тимчасову і постійну твердість. Комплексонометричне визначення загальної твердості води полягає в титруванні відміреного об’єму води розчином трилону Б з Сн = 0,1 за наявності металіндикатору еріохром чорного Т.
Реакція відбувається за таким рівнянням:
Ca2+ + Na2H2У ® Na2CaУ + 2H+
Реакція відбувається у слабколужному середовищі, для створення якого перед титруванням добавляють буферний розчин (суміш NH4Cl i NH3). Трилон Б відповідає вимогам, які ставляться до вихідних речовин. Робочий розчин трилону Б з Сн = 0,1 готується безпосередньо з наважки (відносна молекулярна маса препарату Mr = 372). З рівняння взаємодії трилону Б із солями кальцію (магнію), видно, що еквівалентна маса трилону Б дорівнює ½ молярної маси. Для виготовлення розчину з Сн = 0,1 на аналітичних терезах зважують з точністю до 0,0001 г 18,6 г трилону Б, переносять у мірну колбу на 1 л, розчиняють у дистильованій воді, доводячи об’єм розчину до риски.
Розчин індикатору готують так: еріохром чорний Т масою 0,5 г розчиняють у суміші буферного розчину об’ємом 20 см3 (20 г NH4Cl + 100 мл 25 %-ного NH3 в 1 л води) і етилового спирту об’ємом 80 см3. Індикатор у лужному середовищі має синій колір.
Для визначення загальної твердості води відбирають 5 см3 води (загальний вміст солей кальцію і магнію повинен не перевищувати 0,5 ммоль∙екв, а на титрування повинно витрачатись не більше 5 см3 розчину трилону Б з Сн = 0,1).
Відібрану пробу досліджуваної води розводять дистильованою водою до об’єму 100 см3, доливають буферний розчин об’ємом 5 см3 і краплями аміачний розчин індикатору до утворення винно-червоного забарвлення. Титрують робочим розчином трилону Б до переходу червоного кольору в синій.
Твердість води в моль/м3 обчислюють за формулою:

де Сн (Т.) і V(Т.) – молярна концентрація еквіваленту і об’єм робочого розчину трилону Б, витраченого на титрування, в см3; 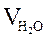 – об’єм проби води, взятої для аналізу, см3.
– об’єм проби води, взятої для аналізу, см3.
F Вода вважається дуже м’якою, якщо загальна твердість становить 1,5 моль/м3; м’якою, якщо загальна твердість 3,0 моль/м3; помірно твердою при загальній твердості 6,0 моль/м3; твердою, якщо загальна твердість 8,5 моль/м3 і дуже твердою, якщо загальна твердість 11 моль/м3 і більше.
Контрольні питання.
1. На чому заснований метод комплексонометричного титрування?
2. Якими способами можна встановити точку еквівалентності при комплексонометричному титруванні?
3. Які сполуки називаються комплексонами? Наведіть приклад.
4. Як готується робочий розчин трилону Б?
5. Складіть схеми йонних рівнянь взаємодії дво-, три- і чотиривалентних катіонів з трилоном Б.
6. Дайте визначення поняття «металіндикатор».
7. В чому полягає специфіка застосування маталіндикаторів?
8. Де застосовується метод комплексонометрії?
9. Наявність йонів яких металів зумовлюють твердість води?
10. В яких межах може коливатися твердість питної води?
| 11 ІНСТРУМЕНТАЛЬНІ МЕТОДИ АНАЛІЗУ |
План
11.1 Електрохімічні методи аналізу.
11.2 Оптичні методи аналізу.
11.3 Хроматографічні методи аналізу.
Фізико-хімічні методи засновані на використанні хімічних реакцій, перебіг яких супроводжується зміною фізичних властивостей аналізованої системи, наприклад її кольору, інтенсивності забарвлення, значення теплової або електричної провідності, прозорості тощо.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 4026; Нарушение авторских прав?; Мы поможем в написании вашей работы!