
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергия Гиббса. Рассмотрим систему, находящуюся при постоянных температуре и давлении
Рассмотрим систему, находящуюся при постоянных температуре и давлении. Объединим вместе соотношения (1.1), (1.3), (1.5) и (1.15):
TDS 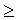 DU + PDV + Aпол . (1.19)
DU + PDV + Aпол . (1.19)
Выражаем величину Апол через термодинамические функции:
–Апол 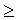 DU + PDV – TDS = U2–U1 + P(V2–V1) – T (S2–S1)=
DU + PDV – TDS = U2–U1 + P(V2–V1) – T (S2–S1)=
=U2+PV2–TS2–(U1+PV1–TS1). (1.20)
Вводим новую термодинамическую функцию, называемую энергией Гиббса:
G º U + PV – TS = H – TS. (1.21)
Из определения этой функции следует, что абсолютное ее значение, как и функций Н и U, неизвестно, изменение этой функции при переходе от начального состояния к конечному не зависит от пути перехода.
Аналогично введенным выше величинам энтальпий образования, энтальпий сгорания, стандартных энтальпий процессов вводим величины энергий Гиббса образования, энергий Гиббса сгорания, стандартных энергий Гиббса процессов. По следствию из закона Гесса энергия Гиббса химической реакции может быть найдена:
DGреакции = 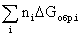 (продуктов) -
(продуктов) - 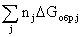 (исходных веществ), (1.22)
(исходных веществ), (1.22)
где ni, nj – числа молей (коэффициенты в уравнении).
Величины стандартных энергий Гиббса образования веществ обычно при 298,15 К табулированы (некоторые значения представлены в табл. 1 приложения).
Физический смысл энергии Гиббса вытекает из соотношения (1.20) –энергия Гиббса в равновесном процессе с точностью до знака равна полезной работе, которую может совершить система. В случае протекания неравновесных процессов энергия Гиббса будет (с обратным знаком) равна максимально возможной полезной работе, которую может совершить система.
|
|
Дата добавления: 2014-01-04; Просмотров: 458; Нарушение авторских прав?; Мы поможем в написании вашей работы!