
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Tермодинамические диаграммы
|
|
|
|
Парокомпрессионных машин
Схемы и циклы одноступенчатых
ТЕМА 4.
Теоретические циклы холодильных машин изображают на термодинамических диаграммах, которые позволяют лучше понять принцип действия холодильных машин. Термодинамические диаграммы, кроме того, служат теоретической базой для расчета холодильных машин в целом и их отдельных элементов.
Наиболее распространены диаграммы давление — энтальпия (lg p-i диаграмма) и температура – энтропия (T-s -диаграмма);
Первую применяют для тепловых расчетов, вторую — для анализа термодинамической эффективности циклов. При этом используют следующие простые измеряемые параметры:
температуру t в °С или абсолютную температуру T в К;
давление p в Па или производных единицах (1 кПа= 103 Па, 1 МПа= 106Па= 10,2 кг с/ см2=10 бар);
удельный объем v в м 3 /кг;
плотность p = 1/ v в кг/м 3, т. е. величину, обратную удельному объему.
Кроме простых измеряемых параметров, используют также сложные расчетные параметры:
энтальпию I в кДж;
энтропию S в кДж/К.
Энтальпия I — это полная энергия рабочего вещества (хладагента), зависящая от его термодинамического состояния. На диаграммах и в расчетах применяют обычно удельную энтальпию i в кДж/кг, т. е. отнесенную к единице массы хладагента.
Удельную энтальпию можно выразить как i=u+pv.
где и — внутренняя энергия хладагента, кДж/кг;
Р — абсолютное давление, Па;
v — удельный объем, m3/kг.
В этом выражении слагаемое pv представляет собой потенциальную энергию давления р. Она расходуется на совершение работы.
Значения i, зависящие от принятого на конкретных диаграммах или в таблицах начала отсчета, в разных источниках (учебниках, справочниках) могут не совпадать при одних и тех же значениях t и p.
Энтропия S — это также расчетный параметр, являющиеся функцией термодинамического состояния хладагента, характеризующий направление, протекания: процесса теплообмена между хладагентом и внешней средой. На диаграммах и в расчетах пользуются удельной энтропией s в кДж/(кг К), т. е. отнесенной к единице массы хладагента. Интерес обычно представляет ее изменение
D s =D q / T m
где Δ q· — теплота, отнесенная к единице массы хладагента, кДж/кг;
Т m — средняя абсолютная температура в течение процесса теплообмена,K
На lg p - i и T-s -диаграммах (рис. 9) из точки К, соответствующей критическому состоянию хладагента (см. тему 3), расходятся две так называемые пограничные кривые, разделяющие поле на три зоны: переохлажденной жидкости (ПЖ), парожидкостной смеси (Ж+П) и перегретого пара (ПП).
Если на lg p - i -диаграмме провести линию постоянного давления (p=const) — изобару, а на T-s -диаграмме линию постоянной температуры (T =const) — изотерму, то они пересекут пограничные кривые в точках А и В. В точке А хладагент находится в состоянии насыщенной жидкости, а в точке В — насыщенного пара.
Фазовый переход от жидкости к пару на диаграммах идет слева направо. При подводе теплоты (энтальпия и энтропия возрастают) переохлажденная жидкость, достигнув состояния насыщения в точке А. начинает кипеть. По мере дальнейшего подвода теплоты содержание жидкости в единице массы хладагента уменьшается, а содержание пара увеличивается ив точке В достигает 100 %. Образуется насыщенный пар. Паросодержание x хладагента на левой пограничной кривой равно 0, а на правой 1. Состояние при x =1 называют также сухим насыщенным паром, чтобы подчеркнуть, что пар не содержит частиц жидкости в отличие от, влажного пара, представляющего собой смесь пара и жидкости (П+Ж).
lg p МПа
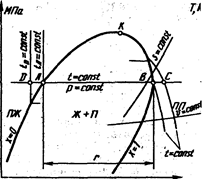
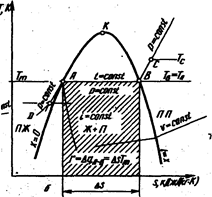
РИС. 9. Изображение теплообменных процессов на термодинамических диаграммах: а —lg p-i -диаграмма; б —T -диаграмма
Фазовый переход от пара к жидкости на диаграммах идет справа налево. При отводе теплоты происходит процесс конденсации хладагента. Он начинается в точке В и заканчивается в точке А.
На lg p-i -диаграмме разность значений энтальпий i в точках A и B будет равна величине r в кДж/кг, которую в зависимости от направления процесса (от A к B или от В к А) называют удельной (скрытой) теплотой парообразования или удельной теплотой конденсации (см. тему 3).
На T-s -диаграмме величине r будет соответствовать площадь (заштрихованная) под процессом А — В, так как
r =ΔqA-B=Δ sT m
Параметры, соответствующие состоянию хладагента на левой пограничной кривой (x =0), обозначают с одним штрихом, а на правой (х=1) — с двумя. Таким образом,
r=i B " -i A '
В процессах кипения и конденсации давление и температура насыщения остаются неизменными, так как подводимая или отводимая теплота расходуется на изменение агрегатного состояния хладагента. При этом температура насыщения зависит от давления. При его увеличении она повышается, а при уменьшении — понижается. Это необходимо твердо помнить для уяснения принципа действия холодильной машины.
Если после подвода определенного количества теплоты и достижения хладагентом состояния насыщенного пара в точке В продолжать подводить теплоту при постоянном давлении (p =const), то этот процесс В — C будет сопровождаться повышением температуры: Т C > Т B. Насыщенный пар перейдет в точке C в состояние, называемое перегретым паром. Перегрев пара Θ C определяется разностью температур:
Θ C,= TC -TB.
Аналогично, если после окончания процесса конденсации В — А продолжать отводить теплоту, то дальнейший процесс А — D будет сопровождаться понижением температуры. Насыщенная жидкость перейдет в точке D в состояние, называемое переохлажденной жидкостью. Переохлаждение жидкости определяется разностью температур:
Θ D =T A -T D
На lg p-i -диаграмме (рис. 9, а) изотермы (T =const) в зоне ПЖ идут почти вертикально вверх, параллельно изоэнтальпам — линиям постоянной удельной энтальпии (i =const), а в зоне. ПП — резко вниз.
На T-s -диаграмме (рис.9,б) изотермы горизонтальны. Изобары (p =const) в зоне ПЖ идут резко вниз и почти совпадают с пограничной кривой (x =o), в зоне ПП — поднимаются круто вверх. Изоэнтальпы (=const) спускаются круто вниз.
Линии постоянной удельной энтропии (s =const) нa T-s -диаграмме вертикальны, а на lg p-i- диаграмме ( рис. 9, а) располагаются примерно под углом 45º к горизонтали.
С небольшим подъемом от горизонтали идут на обеих диаграммахлинии постоянного удельного объема (v =const). Большим давлениям р соответствует меньший удельный объем v.
Поскольку при работе парокомпрессионной холодильной машины в установившемся (стационарном) режиме давления кипения p 0 и конденсации p к, хладагента постоянны, количество подводимой или отводимой теплоты изображается на lg p-i -диаграмме в виде отрезка прямой линии и равно разности энтальпий в начале и конце процесса. В этом заключается достоинство lg p-i -диаграммы, которое обусловило ее широкое использование для расчета парокомпрессионных холодильных машин.
Принципиальная схема и цикл одноступенчатой
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2940; Нарушение авторских прав?; Мы поможем в написании вашей работы!