
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергетический спектр атомов щелочных элементов
|
|
|
|
Краткая теория
Аппаратура
Цель и содержание работы
ИЗУЧЕНИЕ ТОНКОЙ СТРУКТУРЫ СПЕКТРАЛЬНЫХ ЛИНИЙ НАТРИЯ
Ознакомление с тонкой структурой спектральных линий и энергетических уровней атомов щелочных элементов. Экспериментальное изучение дублетной структуры спектральных линий атома натрия. Освоение методики работы на спектрографе большой дисперсии ДФС-8. Получение спектра натрия. Измерение расстояния между компонентами тонкой структуры спектральных линий. Определение величины расщепления Р-термов атома натрия в зависимости от значения главного квантового числа n. Определение величины расщепления 3Р, 3Д, 4Д уровней атома Na, определение поправки экранирования а.
Спектрограф ДФС-8, дуговой генератор УГЭ-4, спектропроектор ДСП-1, измерительный микроскоп МИР-12, атлас и таблица спектральных линий.
| элемент | z | Dl,нм |
| Li | 0,015 | |
| Na | 0,6 | |
| K | 3,4 | |
| Cs | 42,2 |
При более тщательном изучении спектральных линий атомов щелочных элементов была обнаружена так называемая тонкая структура спектральных линий. Применение спектральных приборов с большей дисперсией позволило установить, что линии атомов часто являются двойными, которые очень узки у лития, а с ростом атомной массы становятся шире. Так, для резонансной линии расщепление (Dl, нм) составляет
Естественно предположить, что расщепление спектральных линий обусловлено тем, что расщепляются энергетические уровни электрона, переход между которыми приводит к возникновению данной спектральной линии. Иными словами, тонкая структура спектральных линий должна быть связана с тонкой структурой уровней энергии электрона.
Рассмотрим энергетический спектр атомов щелочных элементов.
Расчет энергетического спектра атома щелочного металла, представляющего собой систему многих электронов в кулоновском поле ядра, является трудной задачей. Поэтому прибегают к такому методу: предполагая, что электроны внутренних оболочек расположены близко к ядру (ядро и электроны внутренних оболочек образует атомной остаток), а внешний (валентный) слабо связанный с атомом электрон, наоборот, находится на достаточно большом расстоянии от ядра, рассматривают атом щелочного металла как некоторую «водородоподобную» систему (внешний электрон - атомный остаток). Такое рассмотрение, учитывающее взаимодействие внешнего электрона с остальными электронами в атоме как небольшое возмущение, налагающееся на кулоновское притяжение атомного остатка, приводит к выражению для энергии, аналогичному выражению для энергии атома водорода:
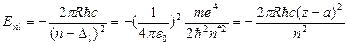 (5.1)
(5.1)
Где 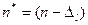 - эффективное квантовое число, n - главное квантовое число,
- эффективное квантовое число, n - главное квантовое число, 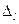 - квантовый дефект,
- квантовый дефект, 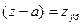 - эффективный заряд ядра, R - постоянная Ридберга
- эффективный заряд ядра, R - постоянная Ридберга
Различие с атомом водорода состоит в том, что n эфф –эффективное квантовое число уже не целое число, как в случае водорода, а отличается от соответствующего квантового числа n на величину 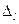 , называемую квантовым дефектом. Величины
, называемую квантовым дефектом. Величины 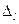 в основном определяются значением орбитального квантового числа l, при данном n квантовый дефект резко уменьшается при увеличении l (см. табл. 4.1).
в основном определяются значением орбитального квантового числа l, при данном n квантовый дефект резко уменьшается при увеличении l (см. табл. 4.1).
Из (5.1) видно, что энергетические уровни щелочного атома расположены ниже соответствующих уровней атома водорода, для которых справедливо соотношение
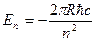 (5.2)
(5.2)
Кроме того, поскольку квантовый дефект 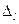 сильно зависит от орбитального квантового числа l, энергия оптического (валентного) электрона в атоме щелочного элемента зависит не только от величины главного квантового числа n, но и от орбитального квантового числа l. Причем зависимость от l будет тем слабее, чем больше l. (см. работу №4).
сильно зависит от орбитального квантового числа l, энергия оптического (валентного) электрона в атоме щелочного элемента зависит не только от величины главного квантового числа n, но и от орбитального квантового числа l. Причем зависимость от l будет тем слабее, чем больше l. (см. работу №4).
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!