
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Отравление М-холиноблокирующими средствами
|
|
|
|
Новые селективные антагонисты М-холинорецепторов
В настоящее время проводятся клинические испытания следующих холиноблокирующих средств:
[ Телензепин (Telenzepine) Аналог пирензепина, обладает такой же селективностью в отношении М1-холинорецепторов, как и пирензепин, однако, превосходит его по силе действия в 4 раза.
[ Трипитамин (Tripitamine) Селективный антагонист М2-холинорецепторов, который предложено использовать для лечения брадиаритмий и блокад.
[ Дарифенацин (Darifenacine) Селективный антагонист М3-холинорецепторов, который предложено использовать для лечения «гиперактивного» мочевого пузыря.
[ Из яда зеленой и черной мамбы были выделены токсины, обладающие ультравысокой селективностью и способностью блокировать М1 и М4-холинорецепторы.
Отравление М-холиноблокирующими средствами может возникать как в случае применения высоких доз собственно М-холиноблокаторов, так и при использовании других лекарственных средств, в спектр активности которых входит холинолитический эффект - противопаркинсонические средства, антигистаминные средства, антидепрессанты. Иногда причиной отравления может быть употребление растений семейства пасленовых (красавки, белены, дурамана и др.).
Следует отметить, что несмотря на причисление атропина к списку особо ядовитых лекарственных средств (venena) он имеет широкий терапевтический индекс и величина LD у человека точно не определена. Для одних пациентов летальная доза атропина составляет около 100 мг, но ряд людей может переносить введение до 400 мг атропина.
В клинической картине отравления различают 2 стадии:
I стадия возбуждения. Проявляется сочетанием 4 синдромов[8]:
[ Нейротоксического: галлюцинации, бред, судороги, одышка.
[ Антисекреторного: прекращается секреция слюнных и слизистых желез верхних отделов дыхательных путей, возникает сухость во рту, нарушается жевание и глотание, появляется першение в горле, пропадает голос (афония). Выключение секреции потовых желез приводит к тому, что теплоотдача путем испарения пота прекращается, температура тела повышается до 41-43°С. Одновременно расширяются кожные сосуды, чтобы скомпенсировать отдачу тепла путем излучения – возникает гиперемия кожи лица, шеи, рук и груди. На коже может появляться скарлатиноподобная сыпь.
[ Атонического: происходит резкое снижение тонуса гладких мышц всех внутренних органов и мышц глаза. Появляется мидриаз, сопровождающийся полной утратой реакции зрачка на свет, фотофобией, нарушается острота зрения (паралич аккомодации), возникает задержка мочеиспускания и дефекации.
[ Кардиального: блокада вагусных влияний на миокард приводит к развитию тахикардии (до 120-160 ударов в минуту) и гипертензии (160/100 мм рт. ст.)
II стадия угнетения. Характеризуется развитием амнезии, комы, выключением рефлексов, параличом дыхательного центра на фоне сохранения симптомов блокады М-холинорецепторов.
Помощь при отравлении. Следует помнить, что М-холиноблокирующие средства снижают моторную функцию желудочно-кишечного тракта, поэтому при пероральном введении яда промывание желудка дает эффект даже через 2-3 часа после его приема (часть токсического вещества остается в желудке). Промывание желудка проводят взвесью активированного угля из расчета 1,0 г угля на килограмм веса. Промывание перманганатом калия менее эффективно, т.к. часть М-холиноблокаторов (например, атропин) не подвергаются окислению и не инактивируются под влиянием перманганата.
Специфическими антидотами при отравлении М-холиноблокаторами являются антихолинэстеразные средства. Физостигмин вводят внутримышечно или внутривенно в дозе 0,5 мг, а затем через 10 мин еще 1,0-1,5 мг. При необходимости инъекции повторяют еще дважды с интервалами 30-40 мин в дозе 1,0-2,0 мг.
Применение М-холиномиметиков для лечения интоксикации неэффективно, т.к. их сродство к рецепторам значительно ниже, чем у большинства М-холиноблокаторов и он не способны вытеснять холиноблокатор из связи с рецептором.
Основой терапии является применение симптоматических средств и ИВЛ до выхода пациента из критического состояния.
Ганглиоблокирующие средства (НН-холиноблокаторы)
Ганглиоблокирующими средствами называют вещества, которые предупреждают влияние ацетилхолина на НН-холинорецепторов вегетативных ганглиев и нарушают передачу импульсов с преганглионарных симпатических и парасимпатических нервов на постганглионарные нервы.
 Гексаметония бензосульфонат (Hexametonium benzosulfonas, Benzohexonium) Является симметричным четвертичным бис-аммонийным соединением. Расстояние между его катионными головками составляет 6 атомов углерода (»0,6-0,7 нм). Такая структура необходимое условие для обеспечения блокады НН-типа холинорецепторов. Если расстояние между катионными центрами увеличивается до 10 атомов углерода (»1,0-1,1 нм), то соединение начинает блокировать НМ-рецепторы скелетных мышц.
Гексаметония бензосульфонат (Hexametonium benzosulfonas, Benzohexonium) Является симметричным четвертичным бис-аммонийным соединением. Расстояние между его катионными головками составляет 6 атомов углерода (»0,6-0,7 нм). Такая структура необходимое условие для обеспечения блокады НН-типа холинорецепторов. Если расстояние между катионными центрами увеличивается до 10 атомов углерода (»1,0-1,1 нм), то соединение начинает блокировать НМ-рецепторы скелетных мышц.
МД: Гексаметоний связывается с натриевыми каналами 2 соседних НН-холинорецепторов и блокирует их. Активный центр НН-холинорецептора остается свободным, т.е. ацетилхолин способен связываться с рецептором, но открытия канала при этом не происходит. Следовательно, действие гексаметония не может быть полностью устранено назначением ацетилхолина, НН-холиномиметиков или антихолинэстеразных средств.
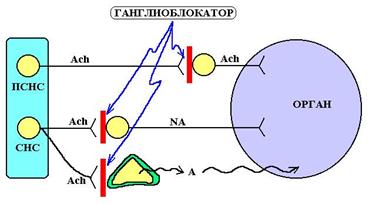
Схема 5. Механизм денервирующего действия ганглиоблокаторов на органы. ПСНС – парасимпатическая нервная система, СНС – симпатическая нервная система, NA – норадреналин, A – адреналин, Ach – ацетилхолин. Ганглиоблокаторы выключают работу НН-холинорецепторов в ганглиях парасимпатической и симпатической систем, а также надпочечниковые рецепторы.
Под влиянием гексаметония происходит блокада НН-холинорецепторов вегетативных ганглиев (симпатических и парасимпатических), мозгового слоя надпочечников и каротидных клубочков.
ФК: Гексаметоний является ионизированным соединением, поэтому его абсорбция из ЖКТ очень плохая и непредсказуемая. Даже при парентеральном введении гексаметоний практически не проникает через ГЭБ и, поэтому, не оказывает центрального действия.
ФЭ: Ганглиоблокаторы (и гексаметоний в том числе) вызывают фармакологическую денервацию тканей, т.к. одновременно блокируют передачу импульсов по симпатическому и парасимпатическому отделам вегетативной нервной системы. Однако, конечный фармакологический эффект зависит от преобладающего тонуса вегетативной нервной системы в каждом из органов: в первую очередь ганглиоблокаторы угнетают функцию того отдела автономной нервной системы, тонус которого выше (см. таблицу).
Таблица 4. Эффекты ганглиоблокаторов в организме человека.
| Орган | Доминирующий тонус | Эффект ганглиоблокаторов |
| Артериолы Вены Миокард Глаз ЖКТ Слюнные железы Потовые железы Мочевой пузырь | Симпатический (адренергический) Симпатический (адренергический) Парасимпатический Парасимпатический Парасимпатический Парасимпатический Симпатический (холинергический) Парасимпатический | Расширение, увеличение органного кровотока, снижение АД, выключение барорефлекса Расширение, депонирование крови в венах, снижение венозного возврата к сердцу и, как следствие, сердечного выброса Повышение ЧСС Мидриаз, циклоплегия Снижение тонуса и перистальтики, запор, снижение секреции желез желудка и поджелудочной железы Снижение секреции, сухость во рту Сухость кожи Снижение тонуса m. detrusor urinae, задержка мочи |
Влияние на уровень АД. Ганглиоблокаторы снижают АД по ортостатическому типу (т.е. вне зависимости от положения тела), вызывая его резкое и глубокое падение, вне зависимости от исходного уровня АД. Снижение давления связано с несколькими механизмами:
· Ганглиоблокаторы нарушают активность НН-холинорецепторов симпатических ганглиев сосудосуживающих нервов, в результате выключается нейрогенный контроль сосудистого тонуса.
· Ганглиоблокаторы не позволяют активироваться НН-холинорецепторам мозгового слоя надпочечников, которые также получают симпатическую иннервацию. В результате уменьшается секреция адреналина и норадреналина, ослабляется гуморальный контроль сосудистого тонуса.
Несмотря на понижение артериального давления, кровоток в скелетных мышцах и ЦНС практически не изменяется. Заметное снижение мозгового кровотока происходит только после падения АД ниже 50 мм рт. ст. Напротив, в сосудах висцерального бассейна и почечных артериях понижение АД сопровождается заметным уменьшением кровотока.
Гипотензивное действие гексаметония сохраняется в течение 3-4 часов.
Влияние на миометрий. Матка находится под контролем преимущественно парасимпатического тонуса. Поэтому, введение гексаметония небеременным женщинам и в первом триместре беременности приводит к снижению тонуса и сократительной активности матки. К концу беременности и во время родов введение гексаметония приводит к повышению сократительной активности матки[9]. Это связано с тем, что в плаценте интенсивно образуется вненейрональный ацетилхолин. Когда гексаметоний блокирует вегетативные ганглии и тонус парасимпатических нервов понижается, в миометрии компенсаторно начинает образовываться избыточное количество М-холинорецепторов, на которые воздействует плацентарный вненейрональный ацетилхолин.
Применение и режимы дозирования. Благодаря способности блокировать все вегетативные пути ганглиоблокаторы являются весьма ценными средствами при проведении экспериментальной исследовательской работы. Однако, эта же низкая избирательность действия привела к тому, что в клинической практике данная группа лекарств применяется все реже и реже, уступая свои позиции более избирательным лекарствам, лишенным ряда нежелательных эффектов ганглиоблокаторов.
В настоящее время гексаметоний применяют в расчете на его вазодилятирующее действие:
] Для быстрого снижения АД при тяжелых, угрожающих жизни гипертонических кризах (кризах I порядка) – например, при расслаивающей аневризме аорты, появлении признаков нарушения мозгового кровообращения.
] Для снижения объема циркулирующей крови у пациентов с отеком легких (острой левожелудочковой недостаточностью) или мозга. Гексаметоний расширяет сосуды нижней половины тела и депонирует в них от 1,5 до 2,0 л крови. В итоге, снижается кровенаполнение мозговых сосудов, снижается приток крови к сердцу и облегчается его работа
] Для экстренного снижения давления у беременных женщин с поздним гестозом (поздним токсикозом) в состоянии эклампсии (состояние, при котором наблюдается нарушение функции почек, резкая тяжелая гипертензия с судорожным синдромом).
При использовании ганглиоблокаторов для снижения давления не следует стремиться резко понизить уровень АД. Оптимальным считают снижение АД со скоростью»20-25% каждые 3 часа. Если обеспечить бóльшую скорость, то падение Ад приведет к быстрому снижению кровотока через системы плацентарных, церебральных, кардиальных сосудов и может привести к ишемии данных органов.
Обычно 12,5-25 мг гексаметония (0,5-1 мл) растворяют в 20 мл стерильного 0,9% раствора хлорида натрия или 5% глюкозы и вводят внутривенно очень медленно в течение 3-5 минут двухмоментно с интервалом 20-30 мин.
Ранее таблетки гексаметония применяли для лечения язвенной болезни желудка и 12-перстной кишки (по 100-200 мг 2 раза в день). Однако, сейчас, в связи с появлением более эффективных лекарственных средств он более не используется по таким показаниям.
Иногда гексаметоний применяют внутрь для купирования болевого синдрома, вызванного поражением вегетативных и чувствительных ганглиев (так называемые каузалгические боли). Он возникает при опоясывающем лишае (инфекция вызванная герпес-вирусами Varicella-Zoster), вертеброгенном радикулите с ущемлением вегетативных нервных веточек. В этом случае его применяют по 100-300 мг 1-2 раза в день.
НЭ: Основным нежелательным эффектом ганглиоблокаторов является ортостатический коллапс – резкое падение АД при переходе в вертикальное положение с развитием обморока.
Симпатическая денервация сосудов сопровождается выключением барорефлекса. В норме, при переходе в вертикальное положение приток крови к голове и шее понижается, это приводит к тому, что уменьшается стимуляция барорецепторных зон дуги аорты и каротидного синуса. Прекращается торможение сосудодвигательного центра и он, через симпатические нервы, посылает сосудосуживающие импульсы на периферию, которые и способствуют восстановлению притока крови к голове. Под влиянием ганлиоблокаторов этот рефлекс не способен реализоваться, т.к. импульсы от симпатических центров не доходят к сосудам. Кровоток остается пониженным и у человека развивается обморочное состояние (синкопе), на фоне резко пониженного давления.
Для профилактики коллапса пациент должен находиться в горизонтальном положении не менее 2,0-2,5 ч после инъекции гексаметония, за это время успевают подключиться альтернативные механизмы регуляции мозгового кровотока.
Кроме того, прием ганглиоблокаторов сопровождается развитием сухости во рту, нарушением остроты зрения (циклоплегия), повышением внутриглазного давления у лиц с предрасположенностью к глаукоме, задержкой мочи у пожилых пациентов с аденомой предстательной железы.
ФВ: раствор 2,5% в ампулах по 1 мл, таблетки по 100 мг.
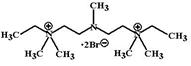 Азаметония бромид (Azamethonium bromide, Pentaminum) По строению, действию и основным эффектам аналогичен гексаметонию. Отличается от него несколько меньшей активностью и более коротким гипотензивным эффектом. После однократного введения эффект сохраняется около 2-3 часов.
Азаметония бромид (Azamethonium bromide, Pentaminum) По строению, действию и основным эффектам аналогичен гексаметонию. Отличается от него несколько меньшей активностью и более коротким гипотензивным эффектом. После однократного введения эффект сохраняется около 2-3 часов.
Применяется по тем же показаниям, что и гексаметоний (гипертонический криз I порядка, отек легких при острой левожелудочковой недостаточности, отек мозга, эклампсия у беременных с гестозом). Азаметоний вводят внутривенно по 15-25 мг (0,3-0,5 мл) в разведении на физиологическом растворе очень медленно или внутримышечно по 100 мг (2 мл).
НЭ: Аналогичны эффектам гексаметония.
ФВ: раствор 5% в ампулах по 1 и 2 мл.
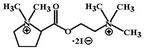 Трепириум йодид (Trepirium iodide, Hygronium) По строению и действию аналогичен гексаметонию. Отличается кратковременным эффектом – действие сохраняется 5-15 мин после введения. В медицинской практике его используют исключительно в расчете на гипотензивное действие:
Трепириум йодид (Trepirium iodide, Hygronium) По строению и действию аналогичен гексаметонию. Отличается кратковременным эффектом – действие сохраняется 5-15 мин после введения. В медицинской практике его используют исключительно в расчете на гипотензивное действие:
] Для купирования гипертонических кризов I порядка, снижения давления у беременных с эклампсией;
] Для уменьшения объема циркулирующей крови при отеке легких (острой левожелудочковой недостаточности), отеке мозга;
] Для создания управляемой гипотензии во время хирургических операций. Управляемой гипотензией называют состояние при котором АД у человека искусственно поддерживают низким и изменяют произвольно, за счет различной скорости введения лекарства. Благодаря снижению АД удается уменьшить кровотечение из операционного поля при операциях на головном мозге, открытом сердце.
Трепириум вводят в виде 0,1% раствора внутривенно медленно капельно. Для этого 100 мг порошка растворяют в 100 мл физиологического раствора и вводят вначале со скоростью 70-100 капель в минуту, непрерывно мониторируя АД. После снижения АД до желаемого уровня скорость введения снижают до 30-40 капель в минуту.
НЭ: Аналогичны эффектам гексаметония. Растворы трепириума нестойки и подвергаются спонтанному гидролизу, поэтому они должны готовиться непосредственно перед применением.
ФВ: порошок по 100 мг во флаконах и ампулах.
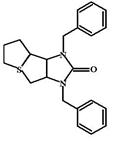 Триметафан (Trimetaphan camsilate, Arfonad) Отличается от других ганглиоблокаторов как строением, так и механизмом действия. Катионный центр триметафана образован не четвертичным азотом, а атомом серы. Молекулы триметафана блокируют, связываясь с активным центром молекулы в том участке, с которым взаимодействует ацетилхолин. При этом сам канал НН-холинорецептора остается свободным. Таким образом, триметафан имеет иную точку приложения действия, чем гексаметоний. Кроме того, действие триметафана может быть полностью устранено при повышении уровня ацетилхолина (например, при введении неостигмина), т.к. ацетилхолин будет вытеснять лекарство из рецептора.
Триметафан (Trimetaphan camsilate, Arfonad) Отличается от других ганглиоблокаторов как строением, так и механизмом действия. Катионный центр триметафана образован не четвертичным азотом, а атомом серы. Молекулы триметафана блокируют, связываясь с активным центром молекулы в том участке, с которым взаимодействует ацетилхолин. При этом сам канал НН-холинорецептора остается свободным. Таким образом, триметафан имеет иную точку приложения действия, чем гексаметоний. Кроме того, действие триметафана может быть полностью устранено при повышении уровня ацетилхолина (например, при введении неостигмина), т.к. ацетилхолин будет вытеснять лекарство из рецептора.
ФЭ: Триметафан характеризуется «мягким» и непродолжительным гипотензивным действием, которое сохраняется в течение 5-15 мин после введения. Кроме того, для триметафана характерен весь спектр ганглиоблокирующих эффектов, о которых упоминалось выше.
Триметафан используют, главным образом, за рубежом. У нас он не применяется в виду высокой стоимости и наличия на рынке трепириума, который обладает аналогичным спектром активности. Применяют триметафан по тем же показаниям, что и трепириум. Вводят триметафан внутривенно медленно со скоростью 0,5-5 мг/мин в течение 1-5 мин, при необходимости прибегают к капельной инфузии (при создании управляемой гипотензии).
ФВ: раствор 5% в ампулах по 10 мл.
Миорелаксанты (НМ-холиноблокаторы)
Миорелаксантами (курареподобными средствами) называют лекарственные вещества, которые нарушают передачу импульсов с окончаний соматических нервных волокон на скелетные мышцы и вызывают их расслабление и временный паралич.
Физиология мышечного сокращения. В целом работа нейро-мышечного синапса организована по тому же принципу, что и в нейро-нейрональных синапсах, однако, она имеет и ряд характерных особенностей.
Нервный импульс, который приходит на пресинаптическое окончание нервного волокна вызывает деполяризацию его мембраны. Под влиянием деполяризации открываются Ca2+-каналы мембраны и ионы кальция поступают в пресинаптическое волокно. Возрастание концентрации кальция в цитоплазме способствует активации белков везикул – синаптобревина и синаптотагмина, которые выполняют роль якоря. Эти якорем везикулы, содержащие медиатор ацетилхолин, способны прикрепляться к белкам пресинаптической мембраны – синтаксину-1 и нейрексину (SNAP-25), в результате образуется поршневой механизм, который выталкивает медиатор в синапс.
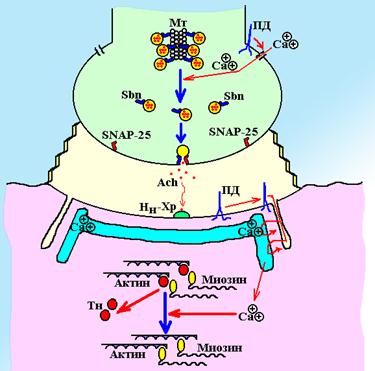
Схема 6. Передача сигнала в нейро-мышечном синапсе. В пресинаптическом нервном окончании везикулы, содержащие медиатор ацетилхолин в покое фиксированы на микротрубочках (Мт) особыми белками синтаксином и синаптобревином. При прохождении потенциала действия (ПД) мембрана нейрона деполяризуется и открываются кальциевые каналы. Это способствует фосфорилированию синаптотагмина и отрыву везикул от микротрубочек. Свободные везикулы путем диффузии приближаются к пресинаптической мембране, где располагаются особые фиксирующие белки нейрексины (SNAP-25). Везикула прикрепляется к мембране, а синаптобревин и нейрексин образуют поршневой механизм, который выталкивает медиатор. Ацетилхолин поступает к постсинаптической мембране мышечного волокна и активирует НМ-холинорецепторы. Это сопровождается генерацией потенциала, распространяющегося по поверхности мембраны. Потенциал вызывает выброс ионов кальция из депо Т-трубочек. Повышение концентрации кальция запускает процесс сокращения.
Путем диффузии ацетилхолин поступает к постсинаптической мембране мышечного волокна (концевая пластинка) и взаимодействует с НМ-холинорецепторами. Если 2 молекулы ацетилхолина занимают 2 активных центра a-субъединицы рецептора, происходит открытие Na+-каналов и ионы натрия поступают в мышечное волокно, вызывая деполяризацию его мембраны. На мембране появляется потенциал действия, который начинает распространяться по ее поверхности и заходит в особые инвагинации мембраны. Почти вплотную к инвагинациям располагаются Т-трубочки саркоплазматического ретикулума, образуя своеобразный «электрический» синапс. Как только мембрана инвагинаций деполяризуется, возникает петля тока, которая захватывает в себя и Т-трубочку. Попавшая в петлю трубочка также деполяризуется и ее кальциевые каналы открываются, выбрасывая депонированные в ретикулуме ионы кальция в цитоплазму.
Попав в цитоплазму, ионы кальция связываются с тропонином и комплекс тропонин-тропомиозин открывает функциональные центры актина и миозина – сократительных белков мышц. Головки миозина начинают взаимодействовать с центрами актина и за счет энергии гидролиза АТФ нити сократительных белков перемещаются вдоль друг друга, вызывая сокращение мышц.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1417; Нарушение авторских прав?; Мы поможем в написании вашей работы!