
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Т е о р и я м е т о д а. Ц е л ь р а б о т ы: определение показателя адиабаты для воздуха
|
|
|
|
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ УДЕЛЬНЫХ ТЕПЛОЕМКОСТЕЙ ГАЗА МЕТОДОМ АДИАБАТИЧЕСКОГО РАСШИРЕНИЯ
Ц е л ь р а б о т ы: определение показателя адиабаты для воздуха
П р и б о р ы: стеклянный сосуд, ручной насос, манометр
Изменение состояния идеального газа связано с изменением его параметров. Согласно 1 закона термодинамики, количество теплоты  , сообщенное системе, идет на увеличение внутренней энергии системы
, сообщенное системе, идет на увеличение внутренней энергии системы 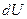 и на совершение термодинамической работы
и на совершение термодинамической работы 
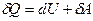 (1)
(1)
Количество теплоты, необходимое для нагревания единицы массы вещества на один градус, называется удельной теплоемкостью:
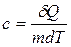 (2)
(2)
Удельная теплоемкость газа зависит от условий, при которых происходит нагревание. Различают теплоемкости (удельную и молярную) при постоянном давлении (cp и  ) и при постоянном объеме (cv и
) и при постоянном объеме (cv и 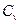 ). Для жидких и твердых тел, объем которых мало изменяется по сравнению с газом, значения
). Для жидких и твердых тел, объем которых мало изменяется по сравнению с газом, значения  и
и 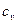 близки друг к другу по величине. Для разного рода практических расчетов их можно считать одинаковым. Сообщенное при постоянном давлении тепло идет на совершение работы и на изменение внутренней энергии, а при постоянном объеме – только на изменение внутренней энергии. Поэтому
близки друг к другу по величине. Для разного рода практических расчетов их можно считать одинаковым. Сообщенное при постоянном давлении тепло идет на совершение работы и на изменение внутренней энергии, а при постоянном объеме – только на изменение внутренней энергии. Поэтому 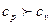 , а их отношение больше единицы и зависит от количества атомов, составляющих молекулу. Теплоемкости могут быть выражены через степени свободы молекул (число независимых переменных, полностью определяющих положение системы в пространстве):
, а их отношение больше единицы и зависит от количества атомов, составляющих молекулу. Теплоемкости могут быть выражены через степени свободы молекул (число независимых переменных, полностью определяющих положение системы в пространстве):
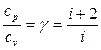 (3)
(3)
Отношение теплоемкостей газа при постоянном давлении и постоянном объеме  играет в термодинамике важную роль. В частности, оно входит в уравнение Пуассона, которое описывает адиабатный процесс.
играет в термодинамике важную роль. В частности, оно входит в уравнение Пуассона, которое описывает адиабатный процесс.
 (4)
(4)
Процесс, при котором отсутствует теплообмен между системой и окружающей средой, называется адиабатным, т.е. 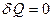 .
.
|
|
|
В случае адиабатного процесса из уравнения (1):
1)  - работа внешних сил увеличивает внутреннюю энергию газа.
- работа внешних сил увеличивает внутреннюю энергию газа.
2) 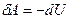 - газ совершает работу за счет убыли внутренней энергии системы
- газ совершает работу за счет убыли внутренней энергии системы

| Одним из простых методов определения пока-зателя адиабаты  является метод Клемана-Дезорма. Экспериментальная установка сос-тоит из стеклянного баллона, соединенного с водяным манометром и насосом. Посредством крана баллон может быть соединен с атмосферой. Если в баллон накачать некоторое количество воздуха, то давление и температура в баллоне повысятся, но в результате теплообмена с внешней средой через некоторое время температура воздуха в баллоне сравнивается с температурой окружа- является метод Клемана-Дезорма. Экспериментальная установка сос-тоит из стеклянного баллона, соединенного с водяным манометром и насосом. Посредством крана баллон может быть соединен с атмосферой. Если в баллон накачать некоторое количество воздуха, то давление и температура в баллоне повысятся, но в результате теплообмена с внешней средой через некоторое время температура воздуха в баллоне сравнивается с температурой окружа-
|
ющей среды  , а давление
, а давление  , где
, где 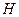 - атмосферное давление,
- атмосферное давление, 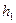 - избыточное давление, измеряемое разностью уровней жидкости в манометре. Таким образом, первое состояние газа определяется параметрами
- избыточное давление, измеряемое разностью уровней жидкости в манометре. Таким образом, первое состояние газа определяется параметрами  ,
,  ,
,  . Если открыть кран на короткое время, то воздух будет расширяться до объема
. Если открыть кран на короткое время, то воздух будет расширяться до объема 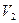 , давление упадет до атмосферного
, давление упадет до атмосферного 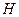 и температура понизится до
и температура понизится до 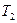 . Это будет второе состояние. Процесс перехода из состояния 1 в состояние 2 протекает очень быстро, поэтому его можно считать адиабатным. Согласно уравнению Пуассона
. Это будет второе состояние. Процесс перехода из состояния 1 в состояние 2 протекает очень быстро, поэтому его можно считать адиабатным. Согласно уравнению Пуассона 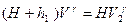 или
или 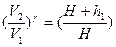 (5)
(5)
Через некоторое время газ нагреется вследствие теплообмена до температуры окружающей среды  и давление возрастет до
и давление возрастет до 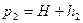 , где
, где  -новая разность уровней жидкости в манометре. Это новое третье состояние газахарактеризуется параметрами
-новая разность уровней жидкости в манометре. Это новое третье состояние газахарактеризуется параметрами 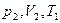 . Так как в первом и третьем состояниях температура одинакова, то параметры этих состояний можно связать уравнением Бойля-Мариотта:
. Так как в первом и третьем состояниях температура одинакова, то параметры этих состояний можно связать уравнением Бойля-Мариотта:
 или
или 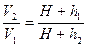 (6)
(6)
Подставляя отношение объемов из уравнения (6) в уравнение (5) получим 

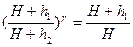
Прологарифмируем это выражение и найдем показатель адиабаты

Так как значения давления мало отличаются друг от друга, в первом приближении разность логарифмов заменим разностью самих величин:
|
|
|
 или
или 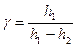 (7)
(7)
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 210; Нарушение авторских прав?; Мы поможем в написании вашей работы!