
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Газовые законы. Уравнение Менделеева-Клапейрона
|
|
|
|
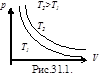 Экспериментальное исследование свойств газов, проведенное в ХVII-XVIII вв. Бойлем, Мариоттом, Гей-Люссаком, Шарлем, привело к формулировке газовых законов:
Экспериментальное исследование свойств газов, проведенное в ХVII-XVIII вв. Бойлем, Мариоттом, Гей-Люссаком, Шарлем, привело к формулировке газовых законов:
1. Изотермический процесс – Т= const. Закон Бойля-Мариотта: pV =const – уравнение изотермы.
График зависимости p от V приведен на рисунке 31.1. Чем выше изотерма, тем более высокой температуре она соответствует, T2>T1.
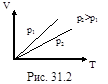 2. Изобарный процесс – p= const. Закон Гей-Люссака:
2. Изобарный процесс – p= const. Закон Гей-Люссака: 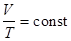 – уравнение изобары. График зависимости V от T приведен на рисунке 31.2. Чем ниже к оси температуры наклонена изобара, тем большему давлению она соответствует, р2 > p1.
– уравнение изобары. График зависимости V от T приведен на рисунке 31.2. Чем ниже к оси температуры наклонена изобара, тем большему давлению она соответствует, р2 > p1.
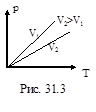 3. Изохорический процесс– V =const. Закон Шарля:
3. Изохорический процесс– V =const. Закон Шарля: 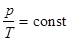 – уравнение изохоры. График зависимости р от Т изображен на рисунке 31.3. Чем ниже к оси температуры наклонена изохора, тем большему объему она соответствует, V 2 > V 1.
– уравнение изохоры. График зависимости р от Т изображен на рисунке 31.3. Чем ниже к оси температуры наклонена изохора, тем большему объему она соответствует, V 2 > V 1.
Комбинируя выражения газовых законов, получим уравнение, связывающее р, V, Т: 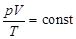 .
.
Постоянная в этом уравнении определяется экспериментально. Для 1 моль газа она оказалась равной R=8,31 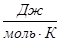 и была названа универсальной газовой постоянной.
и была названа универсальной газовой постоянной.
1 моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. Число молекул (структурных единиц) в 1 моле равно числу Авогадро: NA=6,02.1023моль-1. Для R справедливо соотношение: R= k NA
Итак, для одного моля: 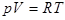 .
.
Для произвольного количества газа n = m/ m (уравнение Менделеева-Клапейрона): 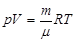 , где m - молярная масса газа.
, где m - молярная масса газа.
Установим связь между уравнением кинетической теории газов и уравнением Менделеева-Клапейрона: 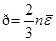 ,
, 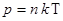 .
.
Так как n =N/V, то 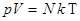 .
.
Для количества вещества справедливо соотношение 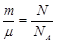 , а для постоянной Больцмана k = R / NA, поэтому последнее уравнение можно записать в виде:
, а для постоянной Больцмана k = R / NA, поэтому последнее уравнение можно записать в виде: 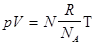 или
или 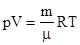 .
.
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 1002; Нарушение авторских прав?; Мы поможем в написании вашей работы!